Clear Sky Science · de
Mitochondriale Bioenergetik–SASP-Querkommunikation bestimmt die Wirksamkeit von Senolytika bei therapieinduzierter Seneszenz
Warum es so schwierig ist, „Zombie“-Krebszellen zu eliminieren
Viele moderne Krebstherapien töten nicht jede Tumorzelle unmittelbar ab. Stattdessen treten einige Zellen in einen Zwischenzustand namens Seneszenz ein: sie hören auf, sich zu teilen, bleiben aber am Leben – ein wenig wie „Zombie“-Zellen. Diese therapieinduzierten seneszenten Zellen können anfangs nützlich sein, doch wenn sie bestehen bleiben, können sie Rückfälle, Therapieresistenz und Nebenwirkungen fördern. Deshalb testen Wissenschaftler Senolytika, Medikamente, die gezielt seneszente Zellen abtöten sollen. Diese Studie stellt eine auf den ersten Blick einfache Frage: Warum sterben manche seneszenten Krebszellen bei Behandlung mit Senolytika, während andere hartnäckig überleben?
Kraftwerke, die sich an ihre Vergangenheit erinnern
Im Zentrum der Untersuchung stehen Mitochondrien, die kleinen Kraftwerke in Zellen. Die Autoren prüften, ob die Art und Weise, wie Mitochondrien verschiedene Brennstoffe verbrennen – etwa Zucker, Fette und Aminosäuren – die Empfindlichkeit seneszenter Krebszellen gegenüber Senolytika beeinflusst, die das Überlebensprotein BCL‑xL angreifen. Mit einem Hochdurchsatztest (MitoPlate S‑1) erstellten sie funktionelle „Fingerabdrücke“ mitochondrialer Aktivität in mehreren Krebszelllinien vor und nach Auslösung der Seneszenz durch verschiedene Behandlungen (DNA-schädigende Mittel, Mitoseblocker, oxidativer Stress oder Zellzyklus‑Inhibitoren). Sie fanden heraus, dass therapieinduzierte Seneszenz keinen einheitlichen mitochondrialen Zustand erzeugt. Stattdessen hinterließ jedes Medikament einen charakteristischen „bioenergetischen Abdruck“ und veränderte, wie breit und intensiv Mitochondrien auf verschiedene Energiequellen zugreifen konnten. Entscheidend war, dass diese Flexibilität auf einer bestehenden Ausgangslage aufbaute: die ursprüngliche mitochondriale Konfiguration der Elternzellen setzte eine Obergrenze – die „Decke“ – dafür, wie stark eine spätere senolytische Reaktion überhaupt sein konnte.
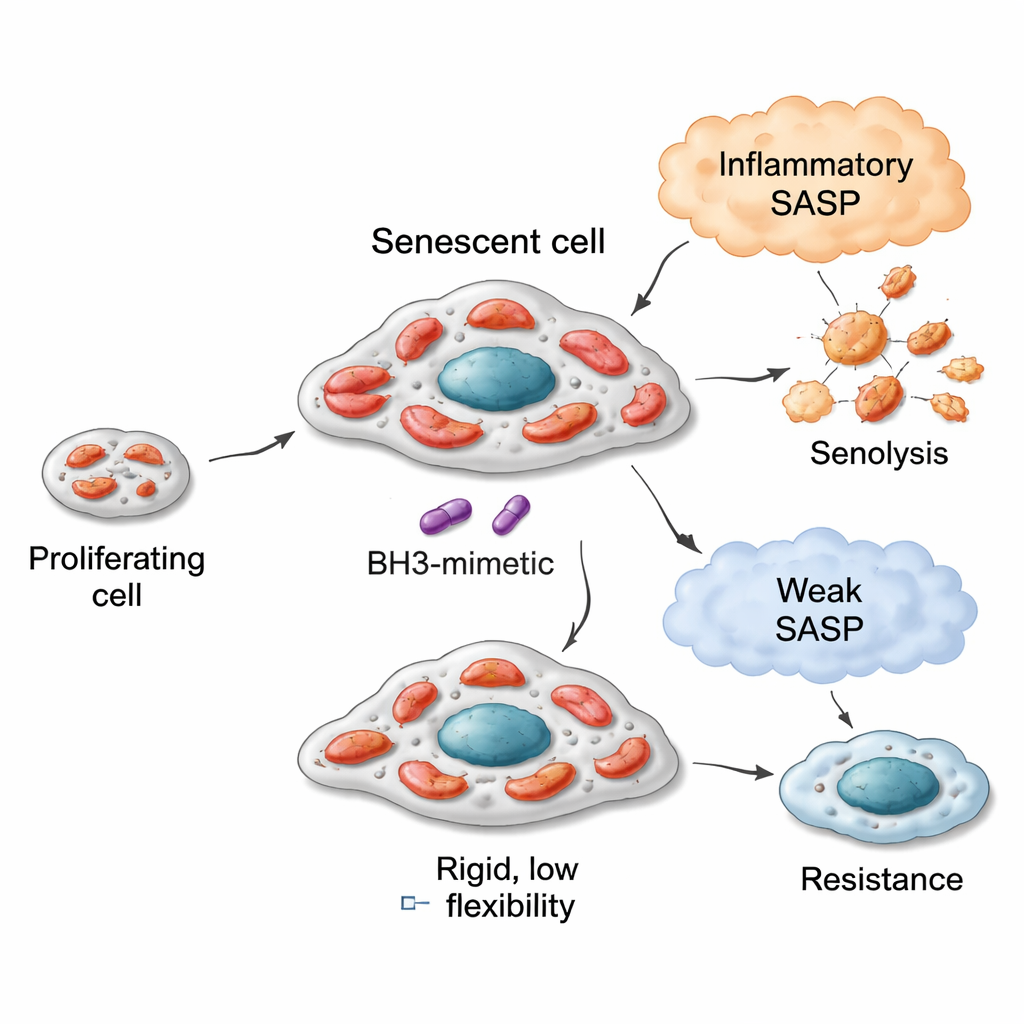
Flexible Motoren, unterschiedliche Brennstoffe und Senolytika-Empfindlichkeit
In Lungen-, Brust- und Darmkrebsmodellen neigten seneszente Zellen mit flexibleren Mitochondrien – die ein breiteres Spektrum an Brennstoffen oxidieren konnten – dazu, anfälliger für BCL‑xL‑gerichtete Senolytika wie Navitoclax (ABT‑263) und A1331852 zu sein. Beispielsweise entwickelten Lungenkrebszellen, die durch das Medikament Bleomycin in Seneszenz gedrängt wurden, Mitochondrien, die viele Substrate besonders intensiv nutzten, vor allem solche, die mit Fettsäureabbau und bestimmten Aminosäurewegen verknüpft sind. Diese Zellen waren hochsensitiv gegenüber Senolytika. Im Gegensatz dazu zeigten Zellen, die durch einen CDK4/6‑Inhibitor (Palbociclib) in Seneszenz versetzt wurden, ein engeres metabolisches Repertoire und sprachen schlecht auf dieselben Senolytika an. Doch diese Beziehung hatte Grenzen: Brustkrebszellen konnten nach Seneszenz ebenfalls metabolisch flexibel werden, doch weil ihre Ausgangs‑Mitochondrien weniger für Apoptose „vorgeprägt“ waren, blieb ihre maximale senolytische Antwort moderat. Darmkrebszellen mit defekter apoptotischer Maschinerie blieben unabhängig von metabolischen Veränderungen resistent. Eine einzelne Messgröße – wie gut Zellen das Brennstoffmolekül Succinat im Ausgangszustand oxidierten – diente als einfacher Indikator für diese vererbte mitochondriale Kapazität.
Wenn Stoffwechsel mit Entzündung spricht
Seneszente Zellen sind berüchtigt für den SASP, einen Cocktail aus sekretorischen Entzündungs‑ und Wachstumsfaktoren, die das umliegende Gewebe beeinflussen können. Das Team untersuchte, wie mitochondrialer Stoffwechsel mit diesem sekretorischen Verhalten verknüpft ist, mithilfe von Zellen, die einen Reporter für miR‑146a tragen, ein MicroRNA, das vom zentralen Entzündungsregulator NF‑κB aktiviert wird. Sie fanden, dass zwar die allgemeinen SASP‑Profile weitgehend durch den Zelltyp bestimmt wurden, nur jedoch bestimmte seneszente Zustände diese NF‑κB/miR‑146a‑Achse aktivierten. Genau diese Zustände sprachen gut auf BCL‑xL‑Senolytika an. Wichtig war, dass diese „entzündlichen SASP‑positiven“ seneszenten Zellen auch eine verstärkte Nutzung der Fettsäureoxidation und eine Transkriptionssteigerung bei Genen zeigten, die langkettige Fette in die Mitochondrien transportieren. Die Blockade des Fettsäureeinstiegs mit dem Medikament Etomoxir dämpfte die miR‑146a‑Aktivierung, ohne die Seneszenz vollständig umzukehren, was darauf hindeutet, dass die Wahl des mitochondrialen Brennstoffs dazu beiträgt, ein entzündliches, für Senolytika zugängliches SASP zu ermöglichen.
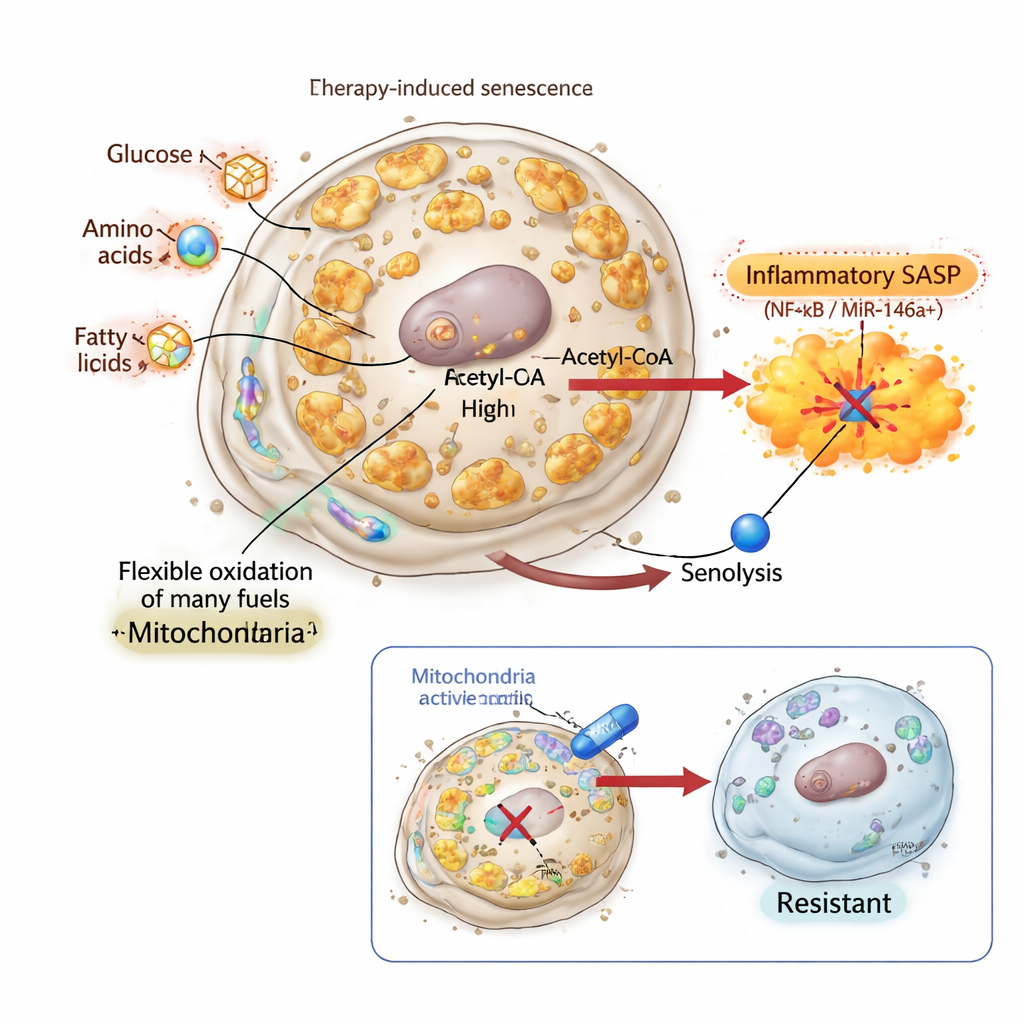
Das Signal ausschalten und untötbare seneszente Zellen erzeugen
Um zu prüfen, ob der entzündliche SASP wirklich für das senolytische Töten erforderlich ist, untersuchten die Forscher Inflachromen, eine Verbindung, die an Chromatinproteine HMGB1 und HMGB2 bindet und deren Rolle bei der Aktivierung von SASP‑Genen blockiert. In Lungen‑ und Brustkrebszellen induzierte Inflachromen ein klares seneszenten Phänotyp: Die Zellen wurden groß, stellten die Teilung ein und akkumulierten Seneszenzmarker. Ihre mitochondriale Masse und bioenergetische Aktivität stiegen deutlich an, und ihre Brennstoffnutzung wurde eindeutig umprogrammiert. Dennoch war ihr SASP abgeschwächt und der miR‑146a‑Reporter blieb weitgehend stumm. Auffallend waren diese SASP‑negativen seneszenten Zellen völlig resistent gegenüber BCL‑xL‑gerichteten Senolytika, obwohl sie bioenergetisch aktive, umprogrammierte Mitochondrien und eine verringerte Expression des klassischen antiapoptotischen Gens BCL2 aufwiesen. Das zeigte, dass mitochondriale Veränderungen allein nicht ausreichen; ohne eine mitochondriengetriebene entzündliche Ausgabe versagt der senolytische „zweite Schlag“.
Was das für zukünftige Krebstherapien bedeutet
Für eine breitere Leserschaft lautet die Schlussfolgerung der Studie, dass das Abtöten therapieinduzierter „Zombie“-Krebszellen von einer geschichteten Schaltung gesteuert wird. Erstens legt die ursprüngliche Gesundheit und Verkabelung der Mitochondrien einer Tumorzelle fest, wie weit Senolytika überhaupt wirken können. Zweitens kann die spezifische Behandlung, die Seneszenz auslöst, den mitochondrialen Stoffwechsel in Richtung mehr oder weniger Flexibilität verschieben und die Zellen näher an oder weiter von der Schwelle zur Apoptose bringen. Drittens – und am entscheidendsten – wirken Senolytika nur gut, wenn die metabolische Umprogrammierung erfolgreich ein entzündliches SASP‑Programm aktiviert, das Rückkopplung an den Zellkern gibt. Ohne diesen entzündlichen Austausch können seneszente Zellen zu einem Sackgassen‑, medikamentenresistenten Zustand werden. Praktisch bedeutet das, dass künftige Therapien durch funktionelle Tests zur mitochondrialen Flexibilität und SASP‑Entzündung in Tumoren optimiert werden könnten, um dann Seneszenz‑auslösende Mittel und Senolytika in Kombinationen auszuwählen, die sicherstellen, dass die „Zombie“-Zellen nicht nur eingefroren, sondern für die Entfernung vorbereitet sind.
Zitation: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Schlüsselwörter: zelluläre Seneszenz, Mitochondrien, Senolytika, Krebsstoffwechsel, entzündlicher SASP