Clear Sky Science · de
SREBP1-Knockdown löst Ferroptose aus, indem er die Nrf2-XCT/GPX4-Achse im Ovarialkarzinom unterdrückt
Die Fettschmiede des Krebses gegen sich selbst richten
Ovarialkarzinome werden oft spät entdeckt und sind schwer zu behandeln. Diese Studie untersucht eine überraschende Schwachstelle dieser Tumoren: ihre Abhängigkeit von der Fettsynthese. Die Forschenden zeigen, dass das Abschalten eines zentralen Schalters für die Lipidproduktion in Krebszellen sowohl ihr Wachstum bremst als auch eine spezielle Form des Zelltods aktiviert und zugleich das Eindringen des Immunsystems in den Tumor erleichtert.
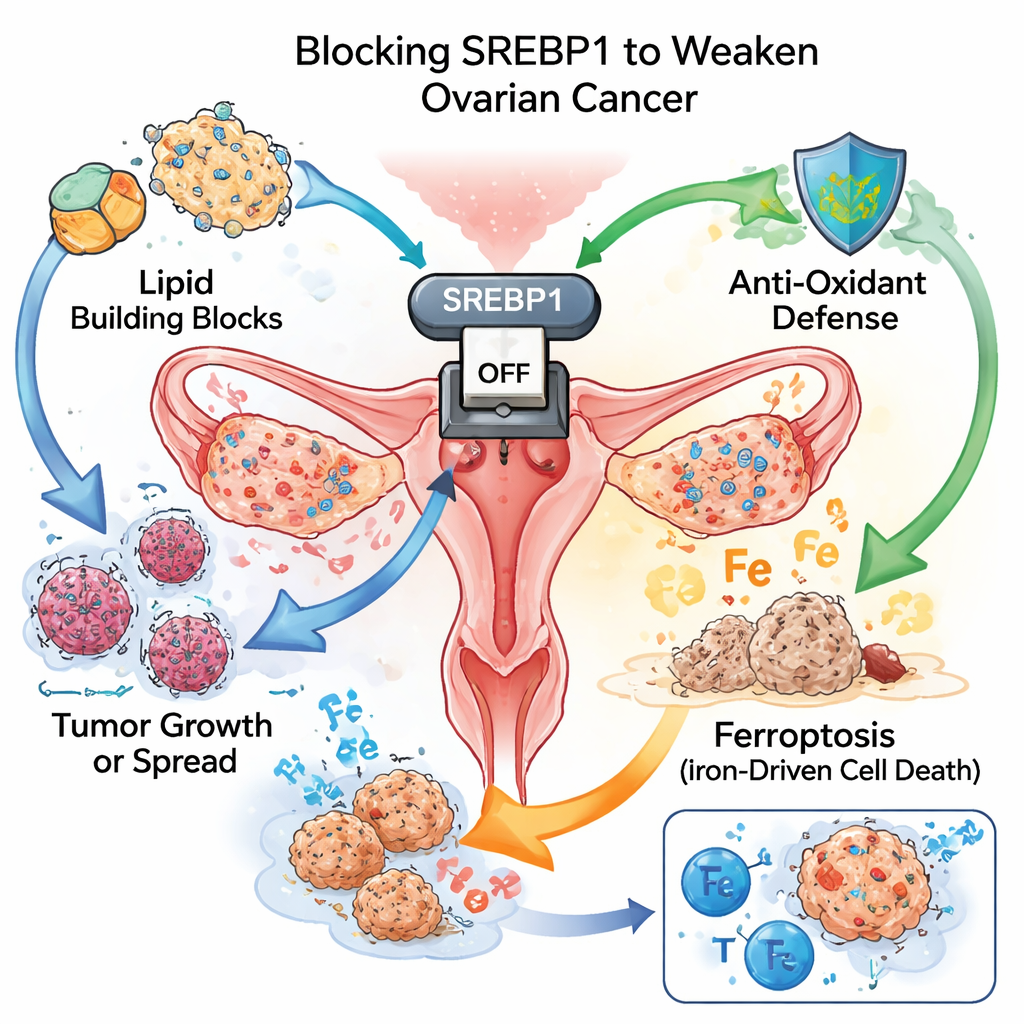
Ein Hauptschalter für Tumorenergie
Wie schnellwachsende Unkräuter benötigen Krebszellen große Mengen an Bausteinen und Energie. Eine Strategie, dieses Bedürfnis zu decken, besteht darin, die Lipidproduktion und -nutzung umzuprogrammieren. Das Team konzentrierte sich auf SREBP1, ein Protein, das als Hauptschalter für die Fettsynthese fungiert. In Gewebeproben von mehr als hundert Patientinnen wiesen die Ovarialtumoren deutlich höhere SREBP1-Spiegel als das umliegende normale Gewebe auf. Frauen, deren Tumoren stärkere SREBP1-Färbung zeigten, hatten tendenziell aggressivere Erkrankungen und kürzere Überlebenszeiten, was dieses Protein sowohl als Treiber des Fortschreitens als auch als Marker für eine schlechte Prognose kennzeichnet.
Wachstum und Ausbreitung durch Fettentzug bremsen
In im Labor kultivierten Ovarialkarzinom-Zelllinien führte die Herunterregulierung von SREBP1 zu einer starken Verringerung der Teilungs- und Koloniebildungsfähigkeit. Die Zellen blieben in bestimmten Phasen des Zellzyklus stecken und konnten sich nicht mehr effizient teilen. Die Forschenden beobachteten zudem weniger Hinweise auf Migration und Invasion: In Wundheilungs- und Transwell-Tests waren Zellen mit reduziertem SREBP1 weniger wanderungsfähig, und Schlüsselmoleküle eines Gestaltwandlungsprozesses namens EMT verschoben sich zurück in einen eher „normalen“ Zustand. Gleichzeitig fielen die Messwerte für Triglyceride und Cholesterin, und Färbungen zeigten weniger Lipidtropfen in den Zellen, was bestätigt, dass ihre interne Fettsynthese heruntergefahren war.
Auslösung eines eisengetriebenen Zelltods
Der auffälligste Effekt der SREBP1-Blockade war die Aktivierung von Ferroptose, einer neu erkannten Form des Zelltods, die durch Eisen und die Peroxidation von Zellmembranen getrieben wird. Nur ein Ferroptoseblocker — nicht jedoch Inhibitoren anderer Todeswege — konnte Zellen mit ausgeschaltetem SREBP1 retten, was Ferroptose als Hauptursache ihres Untergangs nahelegt. Chemische Analysen zeigten mehr Abbauprodukte oxidierter Fette, weniger das Antioxidans Glutathion und höhere Mengen reaktiver Lipidmoleküle. Zwei Proteine, die Zellen normalerweise vor Ferroptose schützen, xCT und GPX4, waren nach SREBP1-Downregulation stark reduziert und entfernten damit eine entscheidende Schutzpuffer gegen diesen zerstörerischen Prozess.
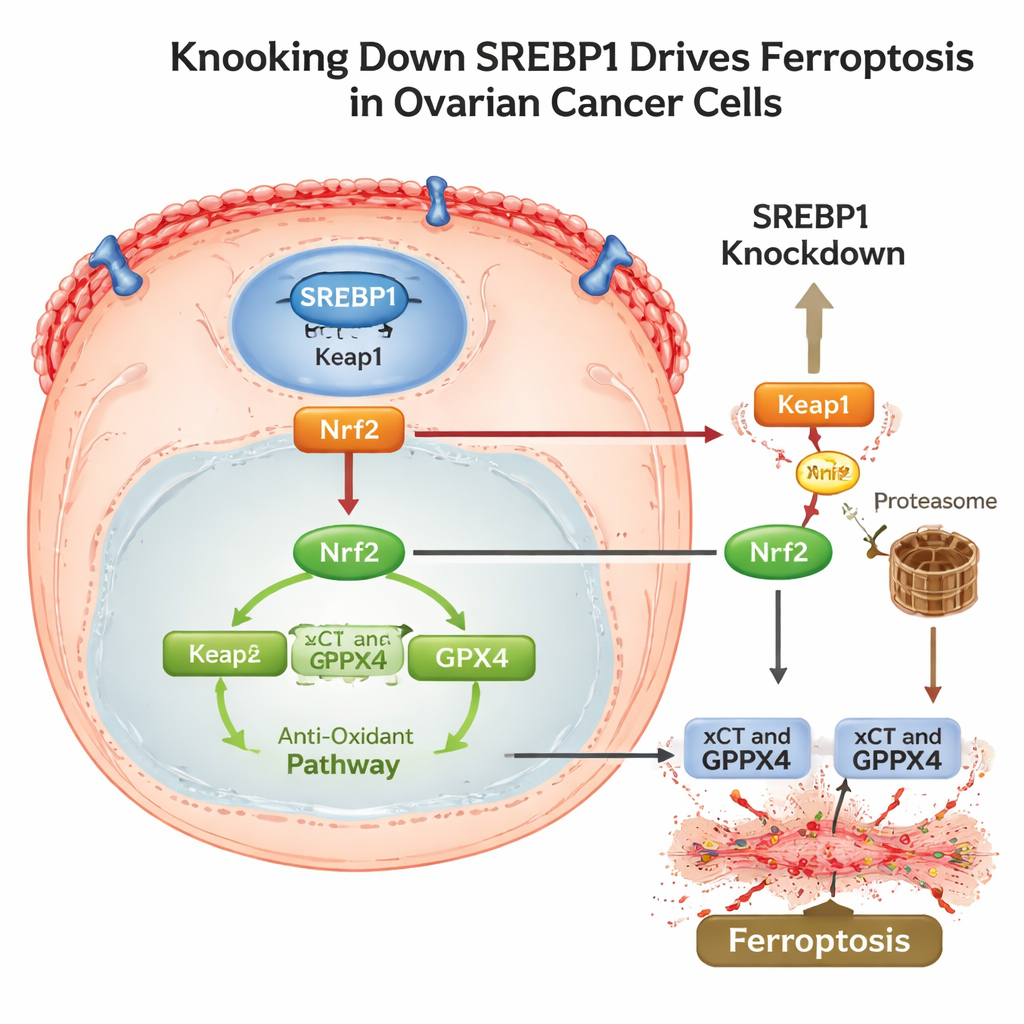
Entwaffnung des zellulären Antioxidansschilds und der Tarnmechanismen
Um zu verstehen, wie SREBP1 mit diesem Todesprogramm verbunden ist, verfolgten die Wissenschaftlerinnen und Wissenschaftler einen Weg über ein weiteres zentrales Stressantwortprotein, Nrf2. Unter normalen Bedingungen hilft Nrf2 Zellen zu überleben, indem es Antioxidansgene wie xCT und GPX4 aktiviert. Die Studie fand, dass die Senkung von SREBP1 die Spiegel von Keap1 erhöhte, einem Protein, das Nrf2 für den Abbau markiert, was zu vermehrtem Nrf2-Abbau und weniger Protein im Zellkern führte. Mit dem Rückgang von Nrf2 schwächten sich die nachgeschalteten Abwehrmechanismen, und Ferroptose setzte ein. Wichtig ist, dass SREBP1-reiche Tumoren auch höhere PD-L1-Spiegel zeigten, ein Oberflächenprotein, das Krebszellen hilft, sich vor angreifenden T-Zellen zu verbergen. Wurde SREBP1 in Maus-Tumoren ausgeschaltet, wuchsen die Tumoren langsamer, zeigten mehr Anzeichen lipidbedingter Schäden, weniger Nrf2 und GPX4 sowie niedrigere PD-L1-Werte und gleichzeitig eine gesteigerte Immunaktivität.
Warum das für künftige Therapien wichtig ist
Vereinfacht gesagt nutzen Ovarialtumoren SREBP1 als zweischneidiges Überlebenswerkzeug: Es fördert ihr Wachstum durch Steigerung der Fettsynthese und rüstet sie zugleich mit einem Antioxidansschild und einer Immunverschleierung aus. Die Arbeit zeigt, dass das Abschalten von SREBP1 den Tumor von Lipiden entzieht, seinen Schutz gegen eisengetriebene Schäden beseitigt und seine Fähigkeit, dem Immunsystem zu entkommen, verringert. Das macht SREBP1 zu einem attraktiven Ziel für neue Wirkstoffe und legt nahe, dass die Kombination von SREBP1-Inhibitoren mit Therapien, die Ferroptose auslösen oder das Immunsystem entfesseln, Patientinnen wirksamere und länger anhaltende Kontrollmöglichkeiten über ihre Erkrankung bieten könnte.
Zitation: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Schlüsselwörter: Ovarialkarzinom, Lipidstoffwechsel, Ferroptose, SREBP1, Tumorimmunität