Clear Sky Science · de
Caspase-Aktivierung treibt anti-Desmoglein-3-induzierte Akantholyse im menschlichen Epidermis an
Wenn der Körper seinen eigenen Hautkleber angreift
Pemphigus vulgaris ist eine seltene, aber gefährliche Erkrankung, bei der das Immunsystem den „Kleber“ angreift, der Hautzellen zusammenhält, was schmerzhafte Blasen und offene Wunden verursacht. Diese Studie schaut unter das Mikroskop, um eine zentrale Frage zu beantworten: Entstehen diese Blasen nur, weil Antikörper diesen Kleber blockieren, oder tragen zusätzliche Signale des Zelltods dazu bei, die Hautzellen auseinanderzureißen? Ein besseres Verständnis könnte zu gezielteren und schonenderen Behandlungen für Patienten führen.
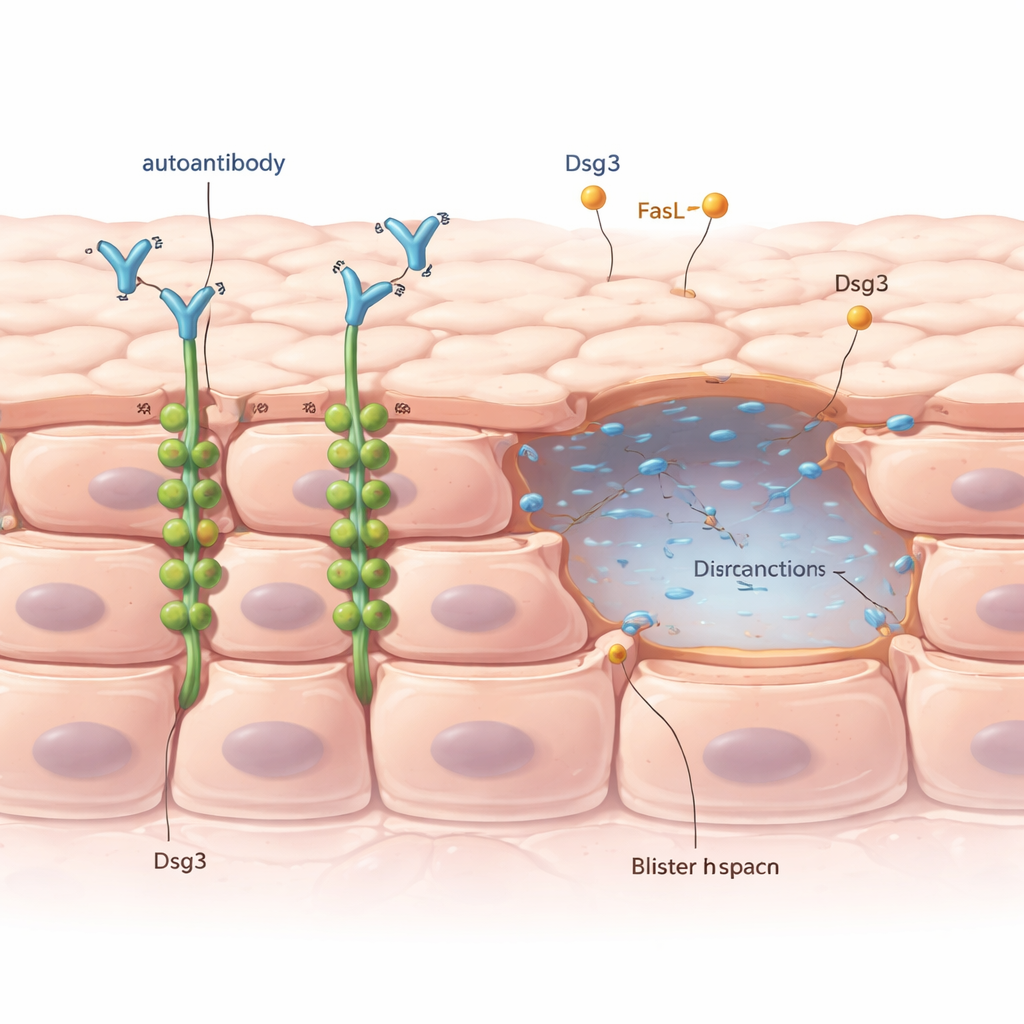
Wie Hautzellen normalerweise zusammenhalten
Die äußere Hautschicht besteht aus dicht gepackten Zellen, die über winzige Strukturen namens Desmosomen verbunden sind und wie Nieten zwischen benachbarten Zellen wirken. Ein wichtiger Bestandteil dieser Nieten ist ein Protein namens Desmoglein 3, kurz Dsg3. Bei Pemphigus vulgaris bilden Patienten Antikörper, die fälschlich an Dsg3 binden. Lange war bekannt, dass dieser Antikörperangriff zu einem Prozess namens Akantholyse führt, bei dem Hautzellen den Kontakt verlieren und Blasen entstehen. Rätselhaft ist jedoch, dass Blasen nur an bestimmten Stellen und zu bestimmten Zeiten auftreten, obwohl die schädlichen Antikörper in der Haut weit verbreitet sind.
Antikörper allein können den Schaden beginnen
Um zu sehen, was die Antikörper selbst bewirken, verwendeten die Forscher Stücke gesunder menschlicher Haut und eine im Labor gezüchtete Hautzelllinie. Sie setzten diese Gewebe einer gut untersuchten anti-Dsg3-Antikörperprobe aus. Sie fanden heraus, dass dieser Antikörper die Zell–Zell-Adhäsion schwächen und Akantholyse auslösen kann, ohne die üblichen zellulären Todesmaschinerien in den Zellen zu aktivieren. Das entscheidende Ereignis war das Wegziehen von Dsg3 von der Zelloberfläche ins Zellinnere, oft verpackt in kleine Vesikel. Dieses Entfernen von Dsg3 aus den „Nieten“ zwischen den Zellen verkürzte und schwächte die Desmosomen, sodass Zellen sich zu trennen begannen.
Wenn Zelltod-Signale hinzukommen, wird es schlimmer
Das Team fragte dann, ob ein bekanntes Zelltod-Signal bei Pemphigus, ein Molekül namens Fas-Ligand (FasL), dieses Bild verändert. FasL kann Enzyme namens Caspasen aktivieren, insbesondere Caspase-8, die normalerweise Zellen zum programmierten Tod führen. In Hautproben von Patienten und in ihrem Hautmodell fanden die Forscher aktive Caspase-8 in Bereichen mit Schäden, aber ohne klassische Anzeichen sterbender Zellen. Wenn sie kleine, nicht-tödliche Mengen FasL zusammen mit dem anti-Dsg3-Antikörper hinzufügten, bildeten sich Blasen schneller und stärker, besonders in den tieferen Schichten der Epidermis. In Zellkulturen schwächte FasL allein die Adhäsion nicht, aber in Kombination mit dem Antikörper verstärkte es die Zellauflösung stark — und dieser Effekt verschwand, wenn Caspase-8 blockiert wurde.
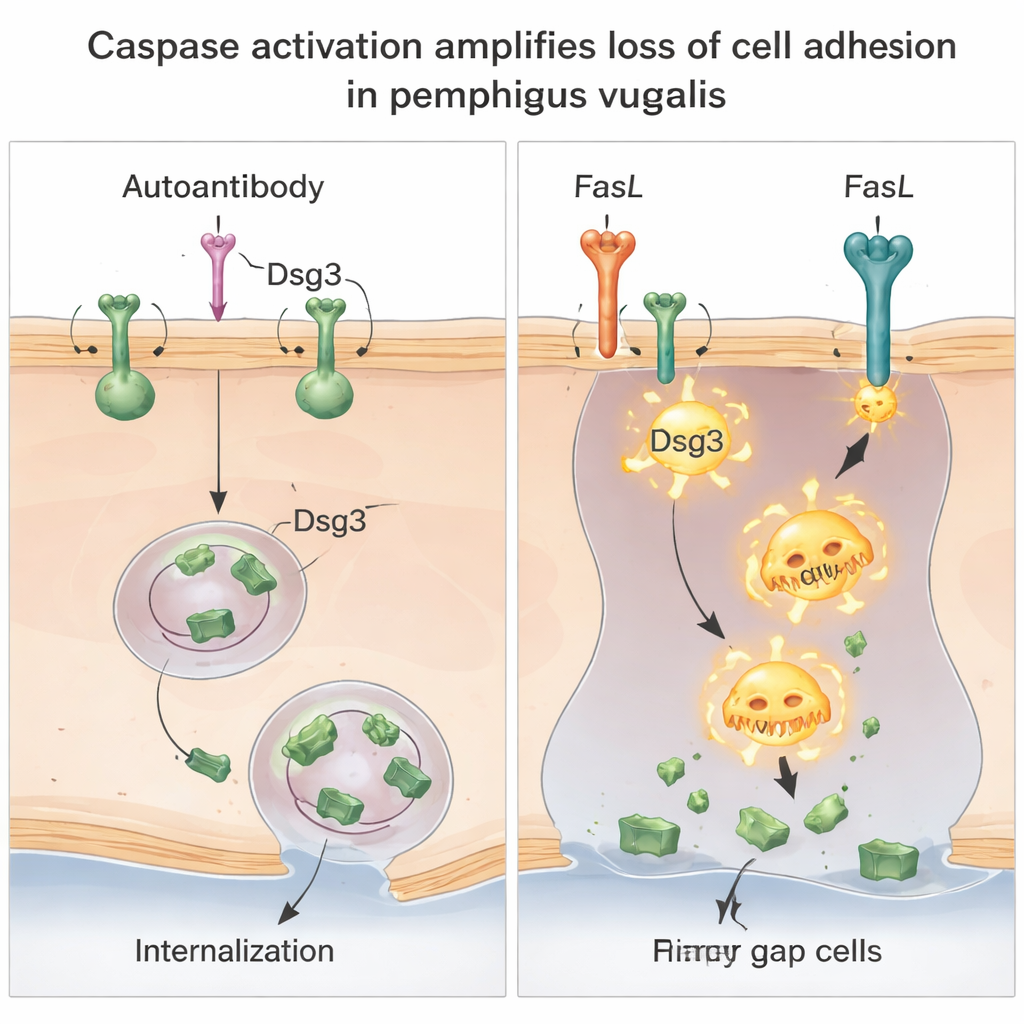
Zwei Wege, dieselbe Verbindung zu zerstören
Tiefergehende Untersuchungen zeigten, dass es tatsächlich zwei verschiedene, aber kooperierende Wege gibt, wie Dsg3 verloren geht. Erstens fördert der Antikörper die Internalisierung intakter Dsg3–Antikörper-Komplexe von der Zelloberfläche in spezialisierte Membrankompartimente und reduziert so die Menge an Dsg3 an Zellverbindungen. Dieser Schritt hing nicht von Caspasen ab und wurde nicht durch das Blockieren üblicher Proteinabbaurouten verhindert, was auf ein spezifisches Umlagern von Dsg3 im Zellinneren hinweist. Zweitens, wenn FasL vorhanden ist, wird Caspase-8 aktiviert und zerschneidet Dsg3 in kleinere Fragmente, besonders an den lockereren Bereichen der Membran. Dieses caspasegetriebene Zerschneiden reduziert weiter die Menge an voll funktionsfähigem Dsg3 und verstärkt den Adhäsionsverlust, der durch die Antikörper ausgelöst wurde.
Was das für Patienten und künftige Therapien bedeutet
Zusammengefasst deuten die Ergebnisse darauf hin, dass bei Pemphigus vulgaris Antikörper gegen Dsg3 den Blasenbildungsprozess einleiten, indem sie Dsg3 von der Zelloberfläche entfernen, während FasL-getriebene Caspase-Aktivierung wie ein Verstärker wirkt, der den Schaden durch das Zerschneiden des verbleibenden Dsg3 deutlich verschlimmert. Wichtig ist, dass vieles davon geschieht, bevor die Hautzellen tatsächlich absterben. Für Patienten bedeutet das, dass wirksame Therapien nicht nur schädliche Antikörper reduzieren müssen, sondern möglicherweise auch FasL oder Caspasen blockieren sollten, um die Bildung oder Ausbreitung von Blasen zu verhindern. Dieser duale Mechanismus könnte erklären, warum die Krankheit von Person zu Person oder von Körperstelle zu Körperstelle so unterschiedlich aussehen und sich so unterschiedlich verhalten kann, und weist auf neue, präzisere Wege hin, den natürlichen Hautkleber zu erhalten.
Zitation: Schmidt, M.F., Feoktistova, M.A., Panayotova-Dimitrova, D. et al. Caspase-activation powers anti-Desmoglein 3-induced acantholysis in human epidermis. Cell Death Discov. 12, 102 (2026). https://doi.org/10.1038/s41420-026-02963-w
Schlüsselwörter: Pemphigus vulgaris, autoimmunes Blasenbild, Desmoglein 3, Caspase-8, Fas-Ligand