Clear Sky Science · de
Vergleichende phänotypische und molekulare Profilierung von replikativer und chemisch-induzierter Seneszenz in Gelenkchondrozyten
Warum verschlissene Gelenkzellen wichtig sind
Schmerzende, steife Gelenke gehören häufig zum Älterwerden, doch Forscher entdecken, dass eine besondere Art von „verschlissener“ Zelle ein zentraler Treiber der Arthrose sein könnte – der weltweit häufigsten Gelenkerkrankung. Diese Zellen, sogenannte seneszente Zellen, hören auf sich zu teilen und beginnen, ein Gemisch irritierender Moleküle freizusetzen, das umliegendes Gewebe schädigen kann. Die Studie stellt eine auf den ersten Blick einfache, aber entscheidende Frage: Wenn Forschende Knorpelzellen im Labor vermehren, um Arthrose zu untersuchen, welche Methoden, diese Zellen „alt“ zu machen, ähneln tatsächlich dem, was in echten Gelenken passiert?
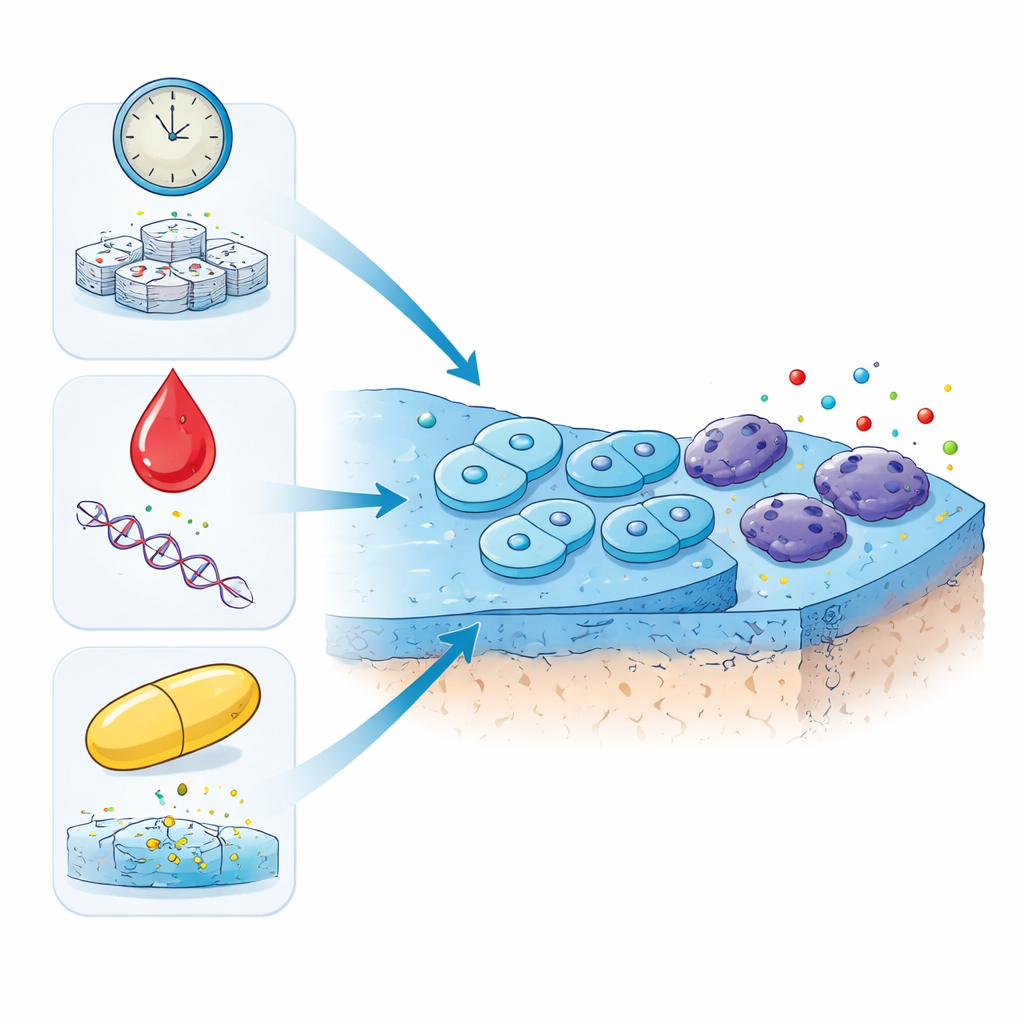
Drei verschiedene Wege zu müden Zellen
Die Forschenden konzentrierten sich auf Chondrozyten, die Zellen, die die glatte Knorpelschicht an den Enden der Knochen erhalten. Mit Zellen aus Schafgelenken brachten sie die Zellen auf drei unterschiedliche Arten in Seneszenz. In einem Ansatz ließen sie die Zellen über viele Generationen hinweg weiter teilen, bis sie einen alten, verschlissenen Zustand erreichten, der das Altern im Zeitverlauf nachahmt. In den beiden anderen Ansätzen setzten sie junge Zellen niedrigen Dosen zweier in der Humanmedizin verwendeter Medikamente aus: Doxorubicin, ein Chemotherapeutikum, das DNA schädigt, und Dexamethason, ein starkes entzündungshemmendes Steroid, das in schmerzende Gelenke injiziert wird. Alle drei Behandlungen wurden so angepasst, dass die Zellen lange genug überleben, um einen stabilen, altersähnlichen Zustand zu entwickeln.
Gemeinsame Zeichen zellulären Alters
Über alle drei Methoden hinweg zeigten die Chondrozyten klassische Kennzeichen der Seneszenz. Sie hörten auf sich zu vermehren, wiesen Veränderungen ihres Zellzyklus auf und entwickelten eine erhöhte Aktivität eines typischen Enzyms, das häufig zur Identifikation seneszenter Zellen verwendet wird. Die Zellen veränderten außerdem ihre interne Struktur, wurden größer und flacher und zeigten Änderungen in der Verpackung ihrer DNA. Tief im Inneren funktionierten ihre Mitochondrien – die kleinen Kraftwerke, die zellaren Treibstoff produzieren – nicht mehr effizient. Durch umfangreiche genetische und proteinbasierte Analysen fand das Team heraus, dass zentrale energieproduzierende Stoffwechselwege und Systeme zum Aufbau neuer Proteine in allen Modellen herunterreguliert waren. Zusammengenommen zeichnen diese Veränderungen ein konsistentes Bild von Knorpelzellen, die aus dem Arbeitsprozess ausgeschieden sind und in einem metabolisch trägen, aber beständigen Zustand verharren.
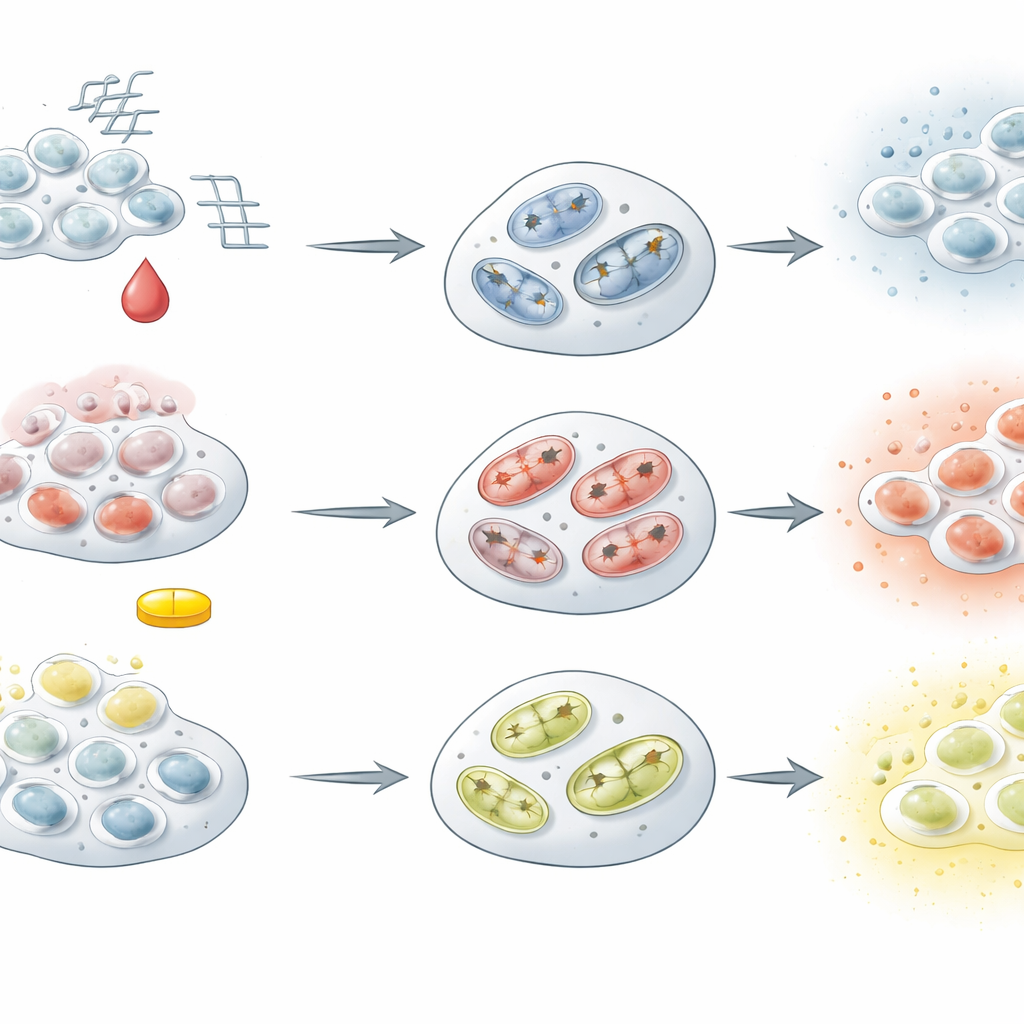
Gleiches Ziel, unterschiedliche Routen
Trotz dieser gemeinsamen Merkmale waren die drei Modelle alles andere als identisch. Zellen, die durch viele Teilungszyklen gealtert waren, zeigten verkürzte Chromosomenenden, sammelten schädliche Sauerstoffnebenprodukte an, verloren Energie und setzten vermehrt strukturelle Knorpelproteine in ihre Umgebung frei – Merkmale, die einem langsamen, altersbedingten Knorpelverschleiß ähneln. Im Gegensatz dazu reagierten doxorubicinbelastete Zellen mit einer starken DNA-Schadensantwort, aktivierten programmierten Zelltodmechanismen und produzierten hohe Mengen an Entzündungsbotenstoffen, was ein härteres, verletzungsähnliches Szenario nahelegt. Dexamethason-behandelte Zellen wurden ebenfalls seneszent, jedoch ohne denselben Anstieg schädlicher Sauerstoffmoleküle oder Apoptose. Stattdessen behielten sie ihre Energieproduktion bei oder steigerten sie sogar und erzeugten eine ausgeprägte Mischung sekretierter Faktoren, die mit Entzündung und Gewebsumbau verknüpft sind – ein Spiegelbild der komplexen, zwiespältigen Effekte von Steroiden auf ansonsten gesunden Knorpel.
Signale, die ins Gelenk gesendet werden
Die Substanzen, die diese seneszenten Zellen freisetzten – zusammengefasst als seneszenzassoziiertes sekretorisches Profil – unterschieden sich stark zwischen den Modellen. Die langgeteilten Zellen sezernierten weniger klassische entzündungs- und stressbezogene Proteine, wurden aber reicher an Knorpelmatrixkomponenten. Im Gegensatz dazu pumpten beide medikamentenbehandelten Gruppen, besonders die steroidexponierten Zellen, viele Moleküle aus, die Immunzellen anlocken, Entzündungen fördern und das umgebende Gewebe umgestalten können. Diese unterschiedlichen „sekretorischen Fingerabdrücke“ sind wichtig, weil sie in einem lebenden Gelenk entweder den Knorpel über Jahrzehnte hinweg stillschweigend schwächen oder nach Verletzung, Chemotherapie oder wiederholten Steroidinjektionen aggressivere, schubartige Schäden auslösen können.
Was das für das Verständnis und die Behandlung von Gelenkerkrankungen bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: Nicht alle gealterten Knorpelzellen sind gleich. Die Studie zeigt, dass verschiedene Laborverfahren Knorpelzellen zwar in einen alten, seneszenten Zustand bringen können, dies aber durch unterschiedliche Stressformen mit unterschiedlichen Folgen geschieht. Durch reine Zeit und wiederholte Teilung gealterte Zellen ähneln am ehesten denen, die bei natürlichem Altern und langjähriger Arthrose beobachtet werden. Durch Chemotherapie oder Steroide gestresste Zellen modellieren besser Situationen, in denen Medikamente oder akute Schäden den Gelenkverfall beschleunigen. Indem man das Labormodell sorgfältig an das reale Szenario anpasst, können Forschende Medikamente besser testen, die seneszente Zellen entfernen oder deren schädliche Sekrete dämpfen. Die Arbeit hebt zudem versagende Mitochondrien und gestörte Energiebilanz als zentrale Schwäche aller seneszenten Knorpelzellen hervor – ein vielversprechendes Ziel für zukünftige Therapien, die unsere Gelenke länger gesund erhalten sollen.
Zitation: Arteaga, M.B., Tarasova, K., Kidtiwong, A. et al. Comparative phenotypic and molecular profiling of replicative and chemically-induced senescence in articular chondrocytes. Cell Death Discov. 12, 106 (2026). https://doi.org/10.1038/s41420-026-02961-y
Schlüsselwörter: Arthrose, zelluläre Seneszenz, Chondrozyten, mitochondriale Dysfunktion, Knorpelabbau