Clear Sky Science · de
Neuer Mechanismus der neuronalen Hypoxieantwort: HIF-1α/STOML2-vermittelte PINK1‑abhängige Mitophagieaktivierung zum Schutz vor neuronaler Schädigung
Warum die Reaktion des Gehirns auf Sauerstoffmangel wichtig ist
Viele häufige Erkrankungen — darunter Schlaganfall, Schlafapnoe, Herzinsuffizienz und selbst Aufenthalt in großer Höhe — berauben das Gehirn seiner Sauerstoffversorgung. Wenn der Sauerstoff abnimmt, sind Gehirnzellen von dauerhaften Schäden bedroht, was zu Gedächtnisproblemen und anderen neurologischen Störungen führen kann. Diese Studie enthüllt ein eingebautes „Selbstschutz“-System, das Neuronen in den frühen Stadien von Sauerstoffmangel aktivieren, um sich am Leben und funktionsfähig zu halten. Das Verständnis dieses Systems könnte neue Behandlungsansätze eröffnen, die das Gehirn schützen, bevor schwerwiegende Schäden eintreten.
Frühes Problem, aber noch keine Katastrophe
Um zu untersuchen, wie das Gehirn auf Sauerstoffmangel reagiert, setzten die Forschenden Mäuse über unterschiedlich lange Zeiträume einer Luft mit etwa 13 % Sauerstoff aus — vergleichbar mit dem Leben auf einem hohen Plateau. In den ersten Tagen verhielten sich die Tiere in Gedächtnis- und Labyrintests normal, und ihre Gehirnzellen wirkten unter dem Mikroskop intakt. Erst nach einer vollen Woche reduzierten Sauerstoffs zeigten die Mäuse deutlichen Gedächtnisverlust und eine gestörte Struktur der Gehirnzellen. Dieses Muster deutet darauf hin, dass Neuronen zumindest in der Anfangsphase nicht passive Opfer des Sauerstoffverlusts sind; vielmehr scheinen sie Schutzreaktionen hochzufahren, die Schäden verzögern oder verhindern.
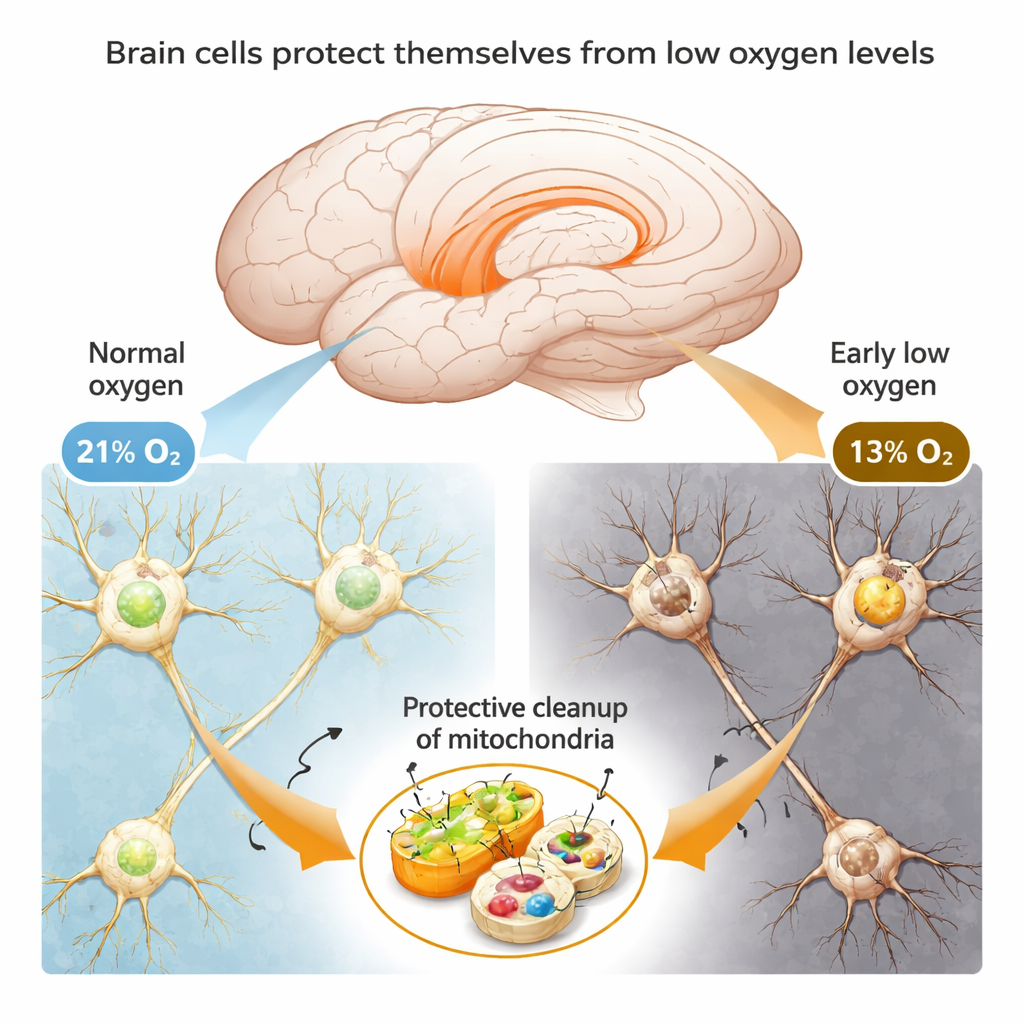
Zelluläre Hausarbeit: Die schlechten Kraftwerke entsorgen
Ein Schwerpunkt der Studie sind die Kraftwerke der Zelle — die Mitochondrien — die in Neuronen besonders wichtig sind, weil Denken und Erinnern große Energiemengen verlangen. Bei Sauerstoffmangel können Mitochondrien versagen und schädliche Nebenprodukte freisetzen, die Zellen verletzen. Das Team fand heraus, dass Neuronen in der frühen Hypoxiephase vorübergehend einen spezialisierten Reinigungsprozess, die Mitophagie, verstärken, der selektiv beschädigte Mitochondrien entfernt und intakte verschont. Sowohl in Mausgehirnen als auch in aus menschlichen Zellen gezüchteten Nervenzellen stiegen die Marker dieses Reinigungsprozesses kurz nach dem Absinken des Sauerstoffs an, genau in dem Zeitraum, in dem die Zellen noch funktionierten. Wenn die Wissenschaftler die Mitophagie chemisch blockierten, sank das Überleben der Zellen und die Schadensanzeichen nahmen zu, was zeigt, dass dieser Aufräumschritt für den Schutz entscheidend ist.
Eine schützende Kettenreaktion in Neuronen
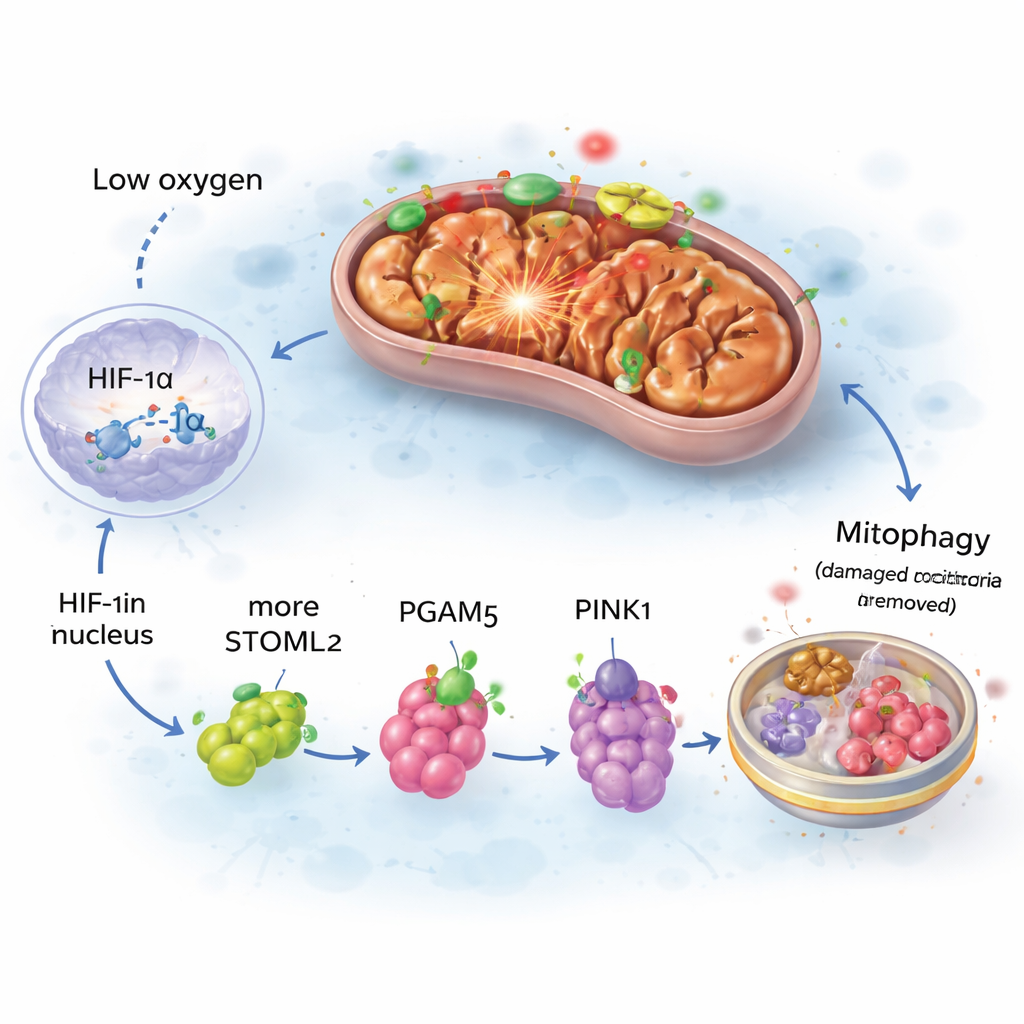
Detaillierter untersucht die Studie, wie diese mitochondriale Reinigung eingeschaltet wird. Sauerstoffmangel stabilisiert ein Sensorprotein namens HIF‑1α, das in den Zellkern wandert und die Genaktivität verändert. Eines seiner Zielgene ist STOML2, ein Protein, das zur Oberfläche der Mitochondrien umzieht. Dort hilft STOML2, ein anderes Protein, PGAM5, in seiner vollwertigen Form zu erhalten. PGAM5 wiederum ermöglicht es einem weiteren Molekül, PINK1, sich an der Außenseite beschädigter Mitochondrien anzureichern. PINK1 markiert diese defekten Kraftwerke dann für den Abbau durch die zellulären Recycling-Mechanismen. Wenn das Team HIF‑1α, STOML2, PGAM5 oder PINK1 selektiv in Mausgehirnen reduzierte, verschwand die frühe Welle der Mitophagie und die Neuronen erlitten bei Sauerstoffmangel größere Schäden. Diese schrittweise Kette — HIF‑1α zu STOML2 zu PGAM5 zu PINK1 — erwies sich als zentraler Schutzweg.
Das Gehirn durch intermittierende Hypoxie trainieren
Die Studie prüfte außerdem eine „Konditionierungs“-Strategie namens intermittierende Hypoxie, bei der Mäuse vor einer länger anhaltenden Sauerstoffreduktion wiederholt kurzen Phasen von niedrigem und normalem Sauerstoff ausgesetzt wurden. Diese Vorbehandlung schaltete denselben HIF‑1α/STOML2/PGAM5/PINK1‑Weg ein und verstärkte die Mitophagie im Gehirn. Bemerkenswerterweise behielten die Mäuse, die intermittierender Hypoxie ausgesetzt waren, ihre Gedächtnisleistung selbst nach einer Woche kontinuierlicher Hypoxie, während unbehandelte Tiere nachließen. Diese Ergebnisse deuten darauf hin, dass sorgfältig kontrollierte Episoden von Sauerstoffmangel Neurone darauf vorbereiten können, ihre eigenen Aufräumsysteme effektiver zu aktivieren — ähnlich wie Bewegung Muskeln auf Belastung vorbereitet.
Bedeutung für den Schutz des Gehirns
Alltagsnah zeigt die Studie, dass Neuronen einen eingebauten Notfallplan für Situationen mit Sauerstoffmangel haben: Sie erkennen die Veränderung schnell, aktivieren eine schützende Proteinkette und räumen fehlerhafte Energieerzeuger aus, bevor diese großflächigen Schaden anrichten. Wenn dieser Plan unterbrochen wird, sind Gehirnzellen deutlich verwundbarer. Indem der Weg im Detail kartiert und gezeigt wurde, dass intermittierende Hypoxie ihn sicher auslösen kann, weisen die Ergebnisse auf künftige Therapien hin, die diese natürliche Abwehr nachahmen oder verstärken könnten. Solche Ansätze könnten eines Tages helfen, das Gehirn vor Schlaganfällen, schlafbezogenen Atmungsstörungen und anderen Zuständen zu schützen, bei denen die Sauerstoffversorgung bedroht ist.
Zitation: Li, Y., Xu, Z., Tian, Z. et al. Novel mechanism of neuronal hypoxia response: HIF-1α/STOML2 mediated PINK1-dependent mitophagy activation against neuronal injury. Cell Death Discov. 12, 104 (2026). https://doi.org/10.1038/s41420-026-02960-z
Schlüsselwörter: Gehirnhypoxie, Mitophagie, neuraler Schutz, intermittierende Hypoxie, Mitochondrien