Clear Sky Science · de
PDHA1 erhöht die Resistenz gegen Ferroptose in anoikis-resistentem Prostatakrebs durch Hochregulierung von AIFM2
Warum einige Prostatakrebszellen sich weigern zu sterben
Wenn Krebszellen sich vom Tumor lösen und in den Blutkreislauf gelangen, sollten die meisten sterben, bevor sie ein neues Organ erreichen. Doch eine gefährliche Minderheit überlebt, wandert weiter und bildet Metastasen, die oft tödlich sind. Diese Studie stellt eine zentrale Frage: Was befähigt bestimmte Prostatakrebszellen, einer Form des Zelltods zu widerstehen, die normalerweise eintritt, sobald sie den Kontakt mit ihrem Gewebe verlieren? Indem sie eine verborgene Überlebensschaltung in diesen Zellen aufdecken, zeigt die Forschung neue Ansatzpunkte, um Metastasen an ihrer Quelle zu verhindern.
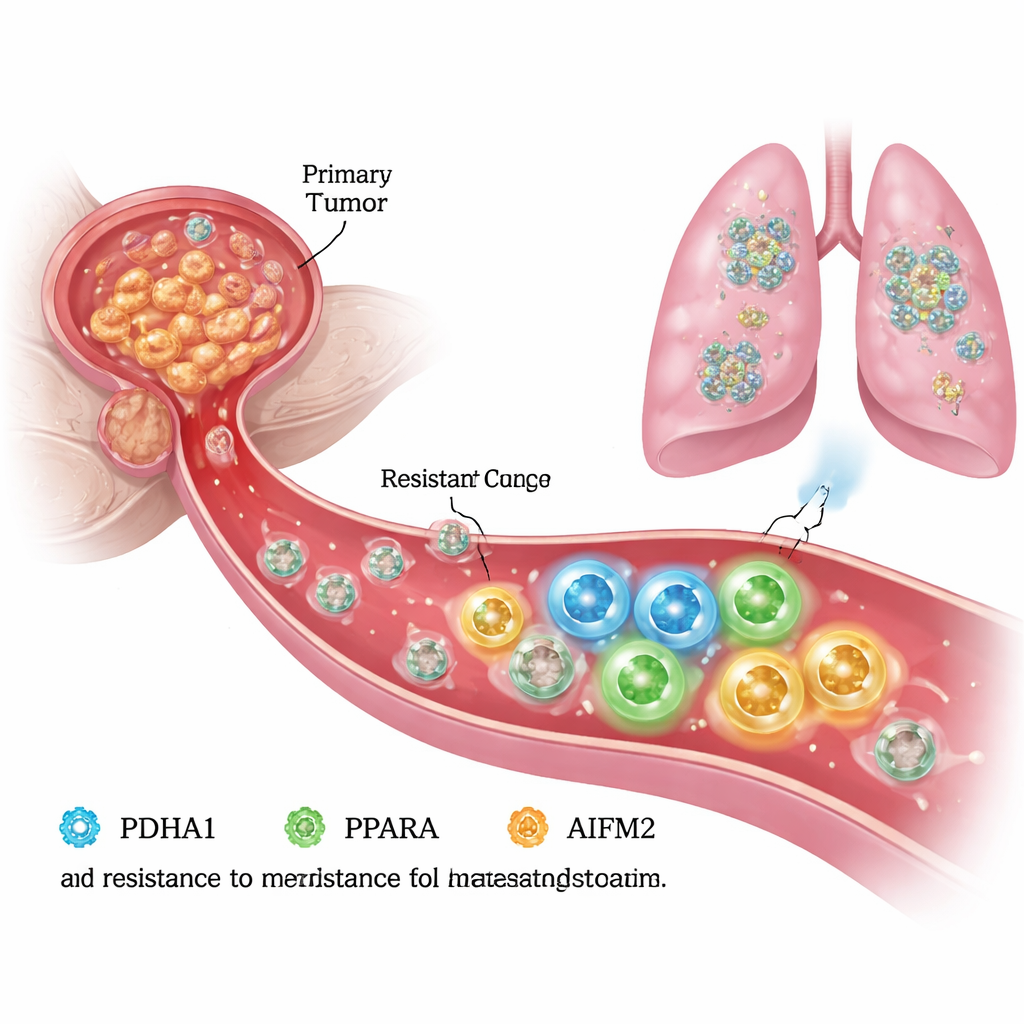
Dem Tod im Blutkreislauf entkommen
Um sich auszubreiten, müssen Prostatakrebszellen ein Leben ohne die Unterstützung des umgebenden Gewebes, der extrazellulären Matrix, aushalten. Unter diesen "gelösten" Bedingungen durchlaufen gesunde Zellen einen programmierten Tod, die Anoikis, und viele Krebszellen sind auch anfällig für einen verwandten, eisenabhängigen Todessignalweg, die Ferroptose. Die Autoren erzeugten im Labor anoikis-resistente Prostatakrebszellen und verglichen sie mit ihren ursprünglichen "parentalen" Zellen. Sie stellten fest, dass die resistenten Zellen nicht nur stärker migrierten und invasiver waren, sondern auch unter Detachment besser überlebten, was darauf hindeutet, dass sie ihre interne Maschinerie umprogrammiert hatten, um Ferroptose zu vermeiden und weiter zu wachsen.
Ein metabolischer Schalter mit zweiter Aufgabe
Bei tieferer Untersuchung konzentrierte sich das Team auf ein Stoffwechselenzym namens PDHA1, das vor allem dafür bekannt ist, Zuckerabkömmlinge wie Pyruvat in Mitochondrien in Acetyl‑CoA umzuwandeln und so die Energieproduktion anzutreiben. In den anoikis-resistenten Zellen waren PDHA1-Spiegel und -Aktivität deutlich erhöht, und Patientenproben zeigten mehr PDHA1 in Primärtumoren von Männern, deren Prostatakrebs in Lymphknoten oder andere Organe metastasiert hatte. Wenn die Forscher PDHA1 reduzierten, verloren die resistenten Zellen einen Großteil ihrer Wander-, Invasions- und Überlebensfähigkeit. Überraschenderweise war ein erheblicher Anteil von PDHA1 in diesen Zellen nicht mehr auf Mitochondrien beschränkt; es hatte seinen Weg in den Zellkern gefunden, wo die DNA mit Histonen verpackt ist, die chemisch verändert werden können, um Gene ein‑ oder auszuschalten.
Genaktivität umschreiben, um Ferroptose zu blockieren
Im Zellkern schien PDHA1 die lokale Produktion von Acetyl‑CoA zu fördern, einem zentralen Baustein für Histonacetylierung. Die Autoren zeigten, dass nukleäres PDHA1 eine spezifische Markierung, die H3K9‑Acetylierung, im Kontrollbereich des Gens PPARA verstärkte. Diese Veränderung wirkt wie das Lockern der Chromatin‑"Spulen" und erleichtert das Anschalten von PPARA. PPARA fungierte seinerseits als Schalter, der die Produktion eines weiteren Proteins, AIFM2, erhöhte, indem es an dessen Promotor bindet und die Transkription steigert. PDHA1 beeinflusste AIFM2 also nicht direkt, sondern arbeitete über PPARA und etablierte somit einen mehrstufigen Weg von verändertem Metabolismus zu veränderter Genregulation.
Ein Schutzschild gegen eisenbedingte Schäden aufbauen
AIFM2 ist als innerer Bremsmechanismus gegen Ferroptose bekannt: Es schützt Lipide in Zellmembranen vor zerstörerischer Oxidation. In den resistenten Prostatakrebszellen hob die Hochregulierung von PDHA1 die AIFM2‑Spiegel an, während PDHA1‑Herunterregulierung sie senkte. Funktionelle Tests zeigten, dass die Reduktion von PDHA1 die Merkmale der Ferroptose verstärkte — mehr reaktive Sauerstoffspezies, stärkere Lipidoxidation, niedriges mitochondriales Membranpotenzial und charakteristische Schrumpfung der Mitochondrien — insbesondere wenn die Zellen dem ferroptoseinduzierenden Wirkstoff Erastin ausgesetzt wurden. Die Überexpression von AIFM2 kehrte diese Effekte um, rettete das Überleben der Zellen in Kultur und stellte Lungenmetastasen in Mäusen wieder her, selbst wenn PDHA1 unterdrückt war. Das bestätigte, dass AIFM2 ein kritischer nachgeschalteter Effektor der von PDHA1 gesteuerten Ferroptose‑Resistenz ist.
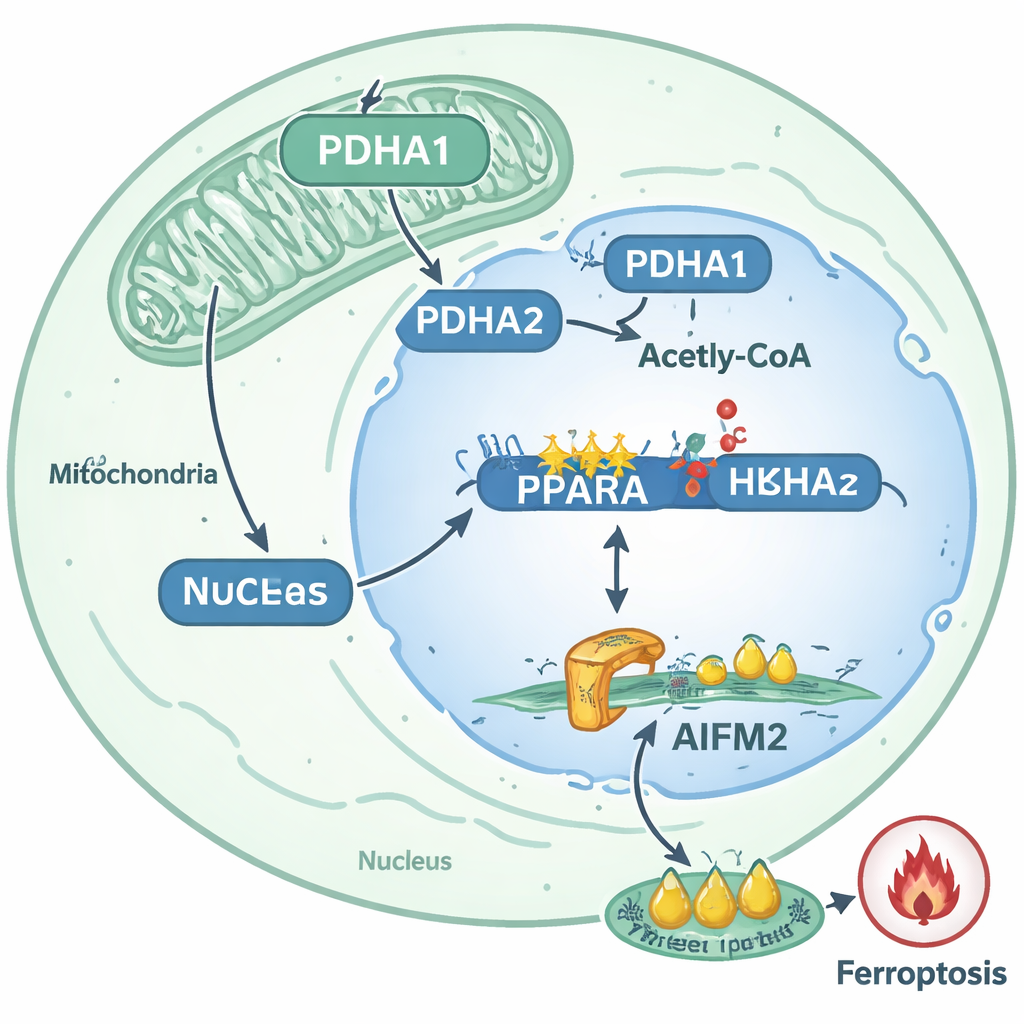
Vom molekularen Schaltkreis zu Behandlungsideen
Durch die Kartierung dieser Abläufe skizziert die Studie einen klaren Weg, wie sich gelöste Prostatakrebszellen schwerer töten lassen: PDHA1 wandert in den Zellkern, erhöht die Histonacetylierung am PPARA‑Gen, steigert die PPARA‑Aktivität und erhöht dadurch die AIFM2‑Spiegel, die Ferroptose blockieren. Dieser Weg steht in starkem Zusammenhang mit metastatischem Verhalten in Patientenproben und Tiermodellen. Für Nicht‑Spezialisten lautet die Kernaussage, dass bestimmte Krebszellen ein normales Stoffwechselenzym als epigenetisches Werkzeug umnutzen, um Genaktivität umzuprogrammieren und einen biochemischen Schutzschild gegen eine kraftvolle Form des Zelltods aufzubauen. Die Autoren schlagen vor, dass Medikamente, die PDHA1, PPARA oder AIFM2 gezielt angreifen — oder Therapien, die gezielt Ferroptose auslösen — eines Tages kombiniert werden könnten, um metastatischen Prostatakrebszellen diesen Überlebensvorteil zu nehmen und sie auf ihrer verwundbarsten Reise, dem Sprung von einem Organ zum anderen, deutlich anfälliger zu machen.
Zitation: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Schlüsselwörter: Prostatakrebs-Metastasen, Ferroptose, Anoikis-Resistenz, PDHA1, AIFM2