Clear Sky Science · de
Modulation metabolischer Signaturen zur Abschwächung von Cabozantinib‑Resistenz in FLT3‑ITD‑Modellen der akuten myeloischen Leukämie
Warum das für die Krebstherapie wichtig ist
Viele moderne Krebsmedikamente zielen auf ein einzelnes defektes Protein in Tumorzellen. Diese zielgerichteten Wirkstoffe können dramatische Remissionen auslösen, doch Krebszellen finden häufig Wege, sich anzupassen und wieder zu wachsen. Diese Arbeit untersucht, wie eine Form von Blutkrebs, die akute myeloische Leukämie (AML), gegenüber einem solchen zielgerichteten Wirkstoff — Cabozantinib — resistent wird und wie ein Umbau des Energiestoffwechsels der Krebszellen Ärztinnen und Ärzten helfen könnte, diese Resistenz zu umgehen.
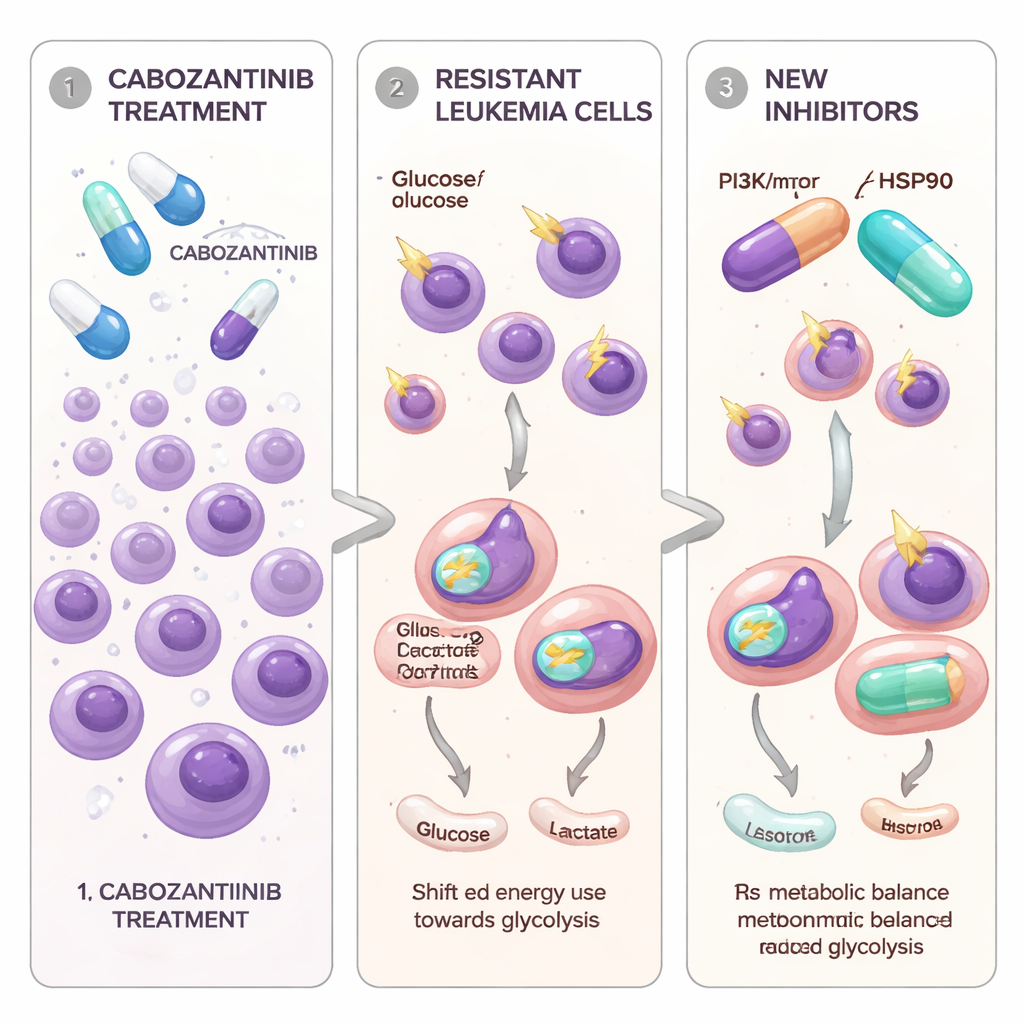
Leukämiezellen, die lernen, einem zielgerichteten Wirkstoff auszuweichen
Die Forscher konzentrierten sich auf AML‑Zellen mit einer Mutation im Wachstumssignal‑Schalter FLT3‑ITD, die für einen besonders aggressiven Krankheitsverlauf bekannt ist. Cabozantinib, ein bereits für mehrere solide Tumoren eingesetztes Tablettenpräparat, kann FLT3‑getriebene Leukämiezellen im Labor stark hemmen. Um zu modellieren, was bei Patientinnen und Patienten über die Zeit passiert, setzten die Wissenschaftler zwei FLT3‑mutierte AML‑Zelllinien schrittweise steigenden Cabozantinib‑Dosen aus, bis einige Zellen überlebten und wieder zu wachsen begannen. Diese neuen Zellpopulationen, Molm13‑XR und MV4‑11‑XR genannt, tolerierten Cabozantinib‑Konzentrationen, die viele Male höher lagen als bei den ursprünglichen „Eltern“zellen. Sie wurden außerdem weniger empfindlich gegenüber zwei anderen zugelassenen FLT3‑gerichteten Medikamenten, Sorafenib und Quizartinib, blieben aber gegenüber einem anderen Inhibitor, Gilteritinib, verwundbar.
Genetische Veränderungen, die dem Krebs das Überleben ermöglichen
Bei näherer Untersuchung fanden die Wissenschaftler, dass diese medikamentenresistenten Leukämiezellen neue Veränderungen im FLT3‑Gen trugen. Beide resistenten Linien hatten dieselbe Punktmutation, D835Y, in einer entscheidenden Region der Kinasedomäne von FLT3 erworben — ein bekannter Hotspot für Resistenz gegenüber mehreren Wirkstoffen. Eine Linie, MV4‑11‑XR, wies zusätzlich eine ungewöhnliche 1,3‑Kilobasen‑Deletion auf, die ein ganzes Exon von FLT3 entfernte und damit einen Teil der Domäne löschte, der für die Wirkstoffbindung wichtig ist. Diese Veränderungen scheinen während der langfristigen Cabozantinib‑Exposition selektiert worden zu sein: Mutante Versionen von FLT3 wurden in den resistenten Zellen deutlich häufiger als in der Ausgangspopulation. Gleichzeitig waren zentrale Signalwege downstream von FLT3 — etwa ERK, STAT5 und AKT — stärker aktiviert, was schnelleres Wachstum und eine erhöhte Koloniebildung der resistenten Zellen unterstützte.
Krebszellen schalten ihr Energiesystem um
Die Forscher fragten dann, ob die Resistenz nicht nur mit genetischen Veränderungen, sondern auch mit der Energieversorgung der Zellen zusammenhängt. Mithilfe von RNA‑Sequenzierung und speziellen Stoffwechseltests fanden sie ein konsistentes Muster: Cabozantinib‑resistente Zellen setzten deutlich stärker auf die Glykolyse — den schnellen Abbau von Glukose im Zytosol — selbst unter ausreichend vorhandenem Sauerstoff. Diese Zellen nahmen mehr Glukose auf, produzierten mehr Laktat, zeigten eine höhere Aktivität des Schlüsselenzyms GAPDH und erhöhten die Expression mehrerer glykolysebezogener Gene. Demgegenüber waren die Mitochondrien, die für eine effizientere Energieproduktion zuständig sind, weniger aktiv und weniger zahlreich. Messungen des Sauerstoffverbrauchs zeigten, dass sowohl die basale als auch die maximale mitochondriale Atmung reduziert waren, und reaktive Sauerstoffspezies in den Zellen erhöht waren — Hinweise auf gestresste, unterperformende Mitochondrien.
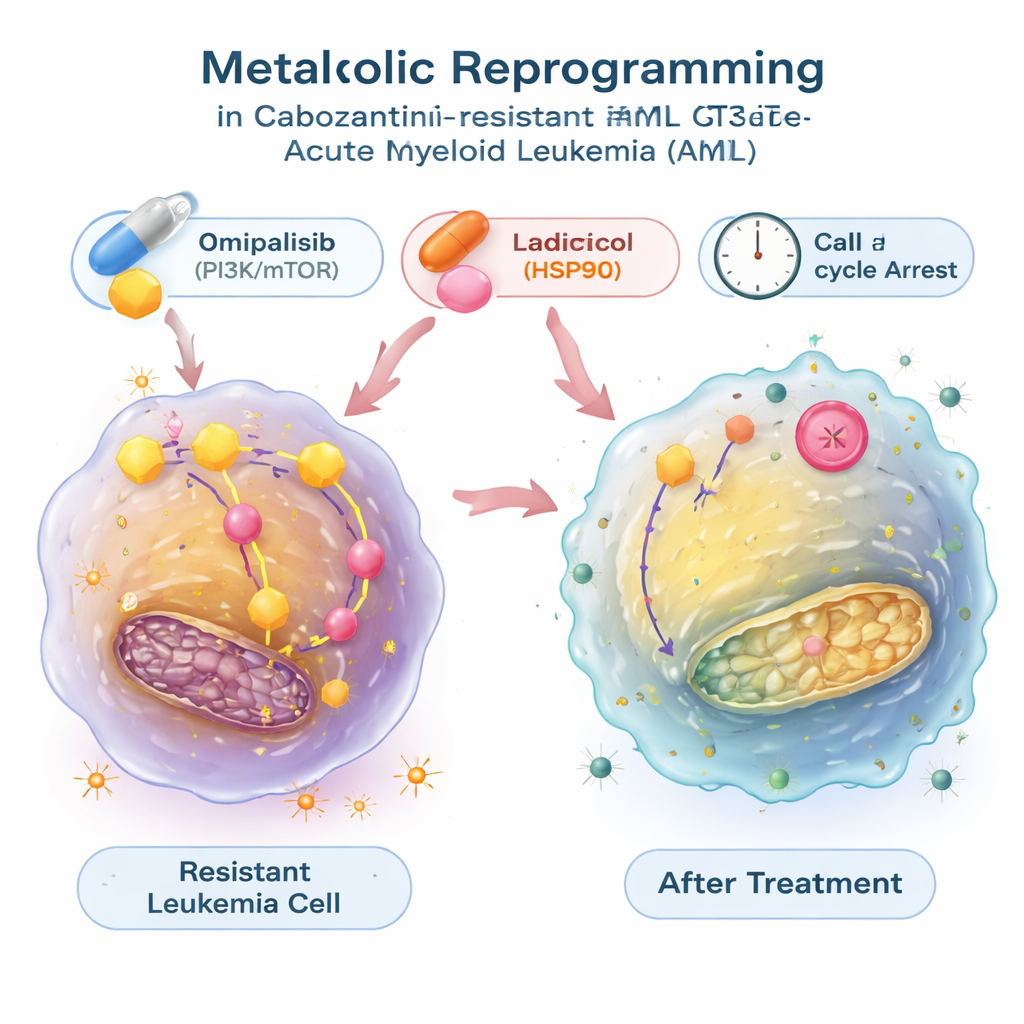
Substanzen, die den metabolischen Schalter zurücklegen
Um zu prüfen, ob sich diese Energiestrategie umkehren lässt, nutzten die Forscher eine große öffentliche Datenbank, die Genexpressionsmuster mit den Effekten tausender Verbindungen verknüpft. Sie suchten nach Wirkstoffen, die das metabolische Profil der resistenten Leukämiezellen vermutlich neutralisieren könnten, und konzentrierten sich auf zwei Kandidaten: Radicicol, ein Hemmstoff des Proteinchaperons HSP90, und Omipalisib, ein Inhibitor des PI3K/mTOR‑Signalwegs, der Wachstum und Stoffwechsel steuert. In Labortests verlangsamten beide Moleküle nicht nur das Wachstum der resistenten Zellen, sondern verringerten auch deren überaktive Glykolyse, normalisierten Glukoseaufnahme und Laktatfreisetzung und senkten die Expression glykolysebezogener Gene. Diese Verbindungen drängten Leukämiezellen in eine Ruhephase des Zellzyklus, und im Fall von Radicicol lösten sie außerdem ausgeprägten programmierten Zelltod aus. In Kombination mit Cabozantinib wirkten Omipalisib — und in einem Modell auch Radicicol — synergistisch und machten die medikamentenresistenten Zellen leichter tödlich zu treffen.
Was das für künftige Leukämie‑Therapien bedeutet
Für Nicht‑Spezialisten lautet die Botschaft: Leukämiezellen können einem zielgerichteten Wirkstoff nicht nur durch Mutationen seines direkten Zielmoleküls entkommen, sondern auch durch eine Veränderung ihrer Energiegewinnung. Die Studie zeigt, dass Cabozantinib‑resistente AML‑Zellen eine „Zucker‑verbrennende“ Strategie annehmen, während ihre Mitochondrien schwächer werden. Durch das Anvisieren der Signalwege, die diesen umgebauten Stoffwechsel stützen — etwa mit Omipalisib oder HSP90‑Inhibitoren — könnte es möglich sein, die Empfindlichkeit gegenüber Cabozantinib und ähnlichen Therapien wiederherzustellen. Obwohl diese Ergebnisse aus Zellmodellen und nicht unmittelbar aus Patientendaten stammen, deuten sie darauf hin, dass die Kombination zielgerichteter Krebsmedikamente mit stoffwechselmodulierenden Substanzen ein vielversprechender Weg sein könnte, Resistenz bei FLT3‑mutierter AML hinauszuzögern oder zu überwinden.
Zitation: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
Schlüsselwörter: akute myeloische Leukämie, Medikamentenresistenz, FLT3‑Mutation, Krebsstoffwechsel, Cabozantinib