Clear Sky Science · de
Osteozytäres Lipocalin‑2 reguliert lokal die Knochenbildung durch eisenabhängige Ferroptose und Wnt‑Unterdrückung
Wenn Knochenzellen still die Ganzkörpergesundheit prägen
Die meisten von uns denken an Knochen als starres Gerüst, doch sie sind lebendig mit Zellen, die das Skelett ständig umbauen und reparieren. Diese Studie zeigt, wie ein kleines Protein, das von Knochenzellen produziert wird — Lipocalin‑2 — die Knochen von innen heraus schwächen kann, indem es den Umgang der Zellen mit Eisen und Energie stört. Das Verständnis dieses verborgenen Prozesses könnte den Weg zu neuen Therapien gegen Osteoporose und altersbedingten Knochenverlust weisen.
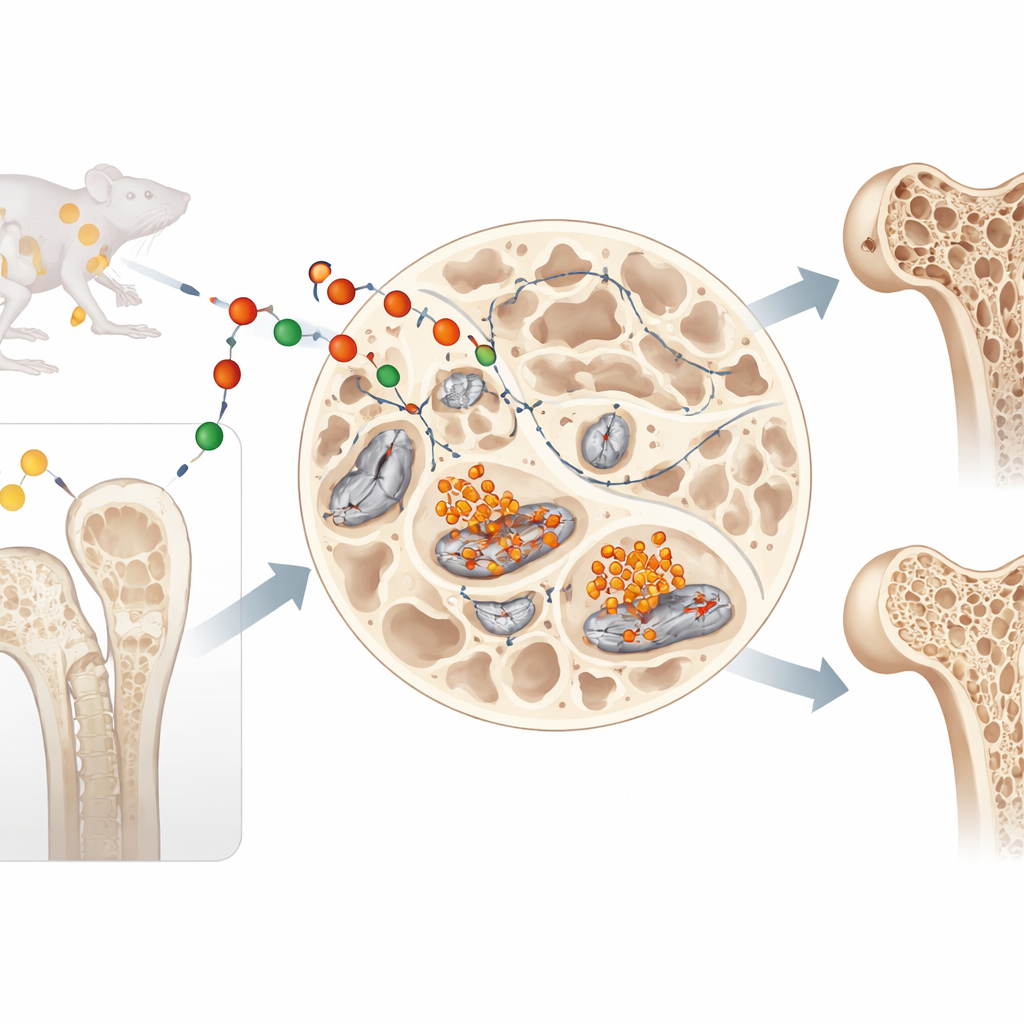
Ein Botenprotein mit doppeltem Leben
Lipocalin‑2 ist als wanderndes Hormon bekannt, das über das Blut reist, Appetit und Körpergewicht mit beeinflusst und durch Eisenbindung bei Infektionen schützt. Die Autoren dieses Papers stellten jedoch eine andere Frage: Was macht Lipocalin‑2 dort, wo es produziert wird — im Knochen selbst? Sie konzentrierten sich auf Osteozyten, die langlebigen Zellen tief im Knochen, die mechanische Kräfte wahrnehmen und den Knochenumbau steuern. Das Team fand heraus, dass Osteozyten Lipocalin‑2 nicht nur weiterhin produzieren, wenn sie reifen, sondern seine Produktion sogar steigern, was auf eine starke lokale Rolle im Skelett hindeutet.
Eisenüberladung und ein rostähnlicher Zelltod
Weil Lipocalin‑2 Eisen transportieren kann, prüften die Forschenden, ob es eine Eisenanreicherung in Osteozyten fördert. In kultivierten Knochenzellen führte die Zugabe von Lipocalin‑2 dazu, dass Eisen in den Zellen akkumulierte, schädliche reaktive Sauerstoffspezies zunahmen und schwere Schäden an fettreichen Zellmembranen auftraten. Das sind Kennzeichen einer jüngst beschriebenen Form des Zelltods, der Ferroptose, bei der Eisen wie Rost wirkt und zerstörerische chemische Reaktionen auslöst. Das Blockieren des Eisens mit einem Chelatbildner verhinderte die Schäden und den Zelltod vollständig, was bestätigte, dass der Prozess eisenabhängig war.
Der Torrezeptor und mitochondriale Folgen
Um zu verstehen, wie Lipocalin‑2 sein Eisen ins Zellinnere der Osteozyten bringt, untersuchte das Team einen spezifischen Rezeptor auf der Zelloberfläche, SLC22A17. Reduzierten sie diesen Rezeptor in osteozytenähnlichen Zellen, so löste Lipocalin‑2 kein Eisenaufnahme, keine oxidative Belastung und keinen ferroptotischen Tod mehr aus, selbst unter Bedingungen von Eisenüberschuss. Die Studie zeigte außerdem, dass Lipocalin‑2 die Kraftwerke der Zelle untergräbt: die Mitochondrien. Übermäßiges Lipocalin‑2 ließ mitochondriale Membranen ihr normales Membranpotenzial verlieren und reduzierte die Energieproduktion, während das Entfernen von Lipocalin‑2 die mitochondriale Funktion wiederherstellte. In Knochen von Mäusen, denen Lipocalin‑2 in Osteozyten fehlte, waren Gene, die die mitochondriale Atmung und Qualitätssicherung unterstützen, hochreguliert, was darauf hindeutet, dass diese Zellen energetisch robuster waren.
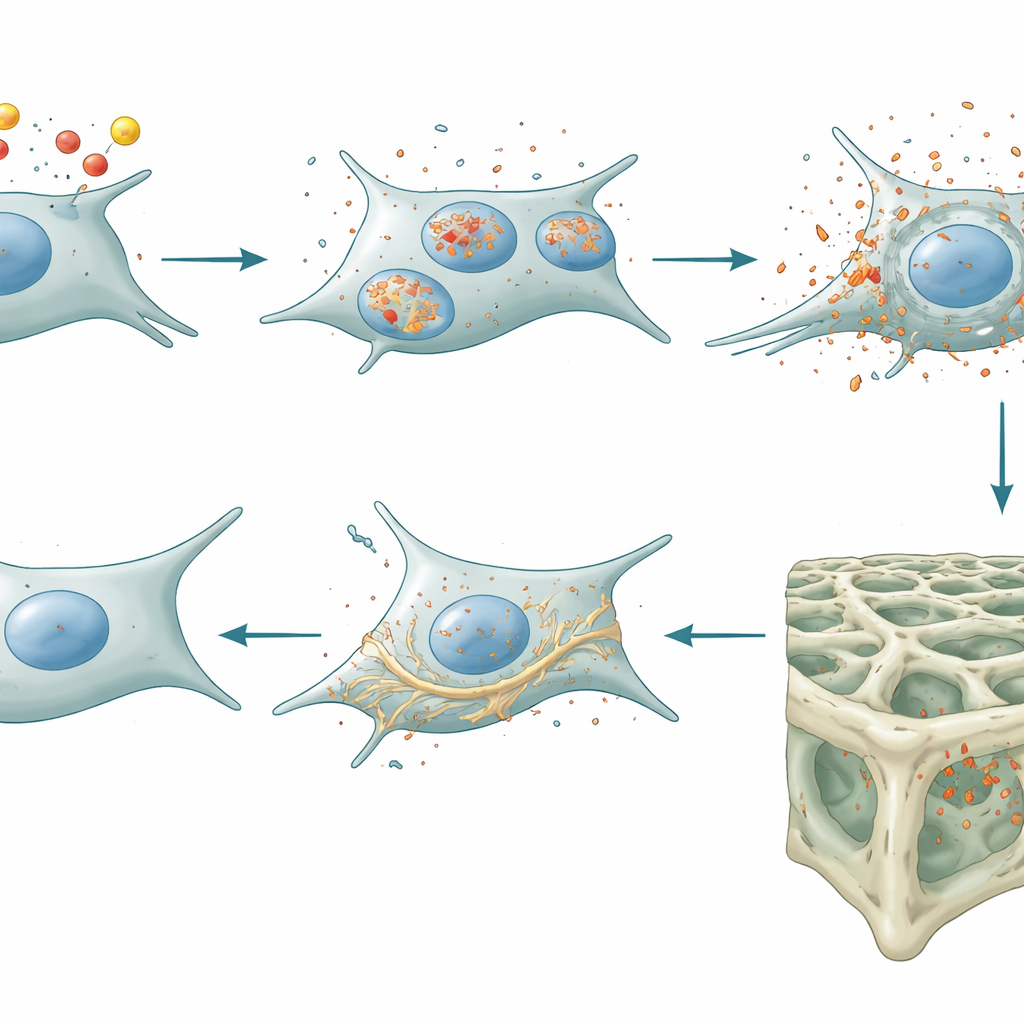
Von Zellstress zu schwächeren Knochen — und wie das Entfernen der Bremse hilft
Die Forschenden untersuchten anschließend intakte Mäuse, bei denen Lipocalin‑2 gezielt in späten Knochenbildungsstadien und in Osteozyten gelöscht worden war. Diese Tiere akkumulierten weniger Eisen in den Knochenzellen und zeigten stärkere antioxidative Abwehrmechanismen, die der Ferroptose entgegenwirken. Wichtig war, dass sie auch niedrigere Mengen zweier Schlüsselproteine — Sclerostin und DKK1 — produzierten, die normalerweise als Bremsen der Wnt/β‑Catenin‑Signalbahn wirken, einem wichtigen Treiber der Knochenbildung. Mit gelockerten Bremsen nahm die Signalgebung zu, die osteoblastische Knochenbildner fördert. Mikro‑CT‑Scans und Knochenmarkierungs‑Experimente bestätigten das Ergebnis: Mäuse ohne osteozytäres Lipocalin‑2 bildeten mehr und besser vernetzte schwammartige (trabekuläre) Knochen, vor allem durch gesteigerte Knochenbildung statt durch verminderte Knochenresorption. Trotz dieser skelettalen Veränderungen blieben Körpergewicht, Blutzuckerregulation, Stoffwechsel und Aktivitätsniveau normal — ein Hinweis darauf, dass der Effekt lokal im Knochen wirkte und nicht als Ganzkörperhormonwirkung.
Was das für den Erhalt starker Knochen bedeutet
Kurz gesagt zeigt diese Arbeit, dass Lipocalin‑2 in Knochenzellen wie ein lokaler Schalter wirkt, der Eisenspiegel erhöht, Mitochondrien belastet, Zellen für ferroptotische Schäden empfänglich macht und einen zentralen Wachstumsweg dämpft — zusammen begrenzt das die Neubildung von Knochen. Wird diese interne Bremse entfernt, bleiben Osteozyten gesünder, senden stärkere beschleunigende Signale für den Knochenaufbau und das trabekuläre Knochengewebe wird dichter und besser vernetzt, ohne den Gesamtstoffwechsel zu stören. Da Lipocalin‑2‑Spiegel und Eisenungleichgewicht mit dem Alter und chronischer Entzündung zunehmen, könnte die gezielte Beeinflussung des Lipocalin‑2‑/Rezeptor‑Systems einen neuen Ansatz bieten, Knochen vor dem von innen heraus „Rosten" zu schützen.
Zitation: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
Schlüsselwörter: Knochengesundheit, Osteozyten, Eisenstoffwechsel, Ferroptose, Wnt‑Signalgebung