Clear Sky Science · de
Mitophagie beim Pankreaskarzinom: Mechanistische Einblicke und Implikationen für neue therapeutische Strategien
Warum die Kraftwerke unserer Zellen beim Pankreaskarzinom wichtig sind
Pankreasduktales Adenokarzinom gehört zu den tödlichsten Krebsarten, unter anderem weil Tumoren sehr schnell lernen, sich gegen fast jede Behandlung zu wehren. Dieser Übersichtsartikel untersucht einen überraschenden Akteur in dieser Resistenzgeschichte: die Mitophagie, das körpereigene System zur Erkennung und zum Recycling verschlissener Mitochondrien, der winzigen „Kraftwerke“, die Energie erzeugen. Zu verstehen, wie Pankreaskrebs diesen Reinigungsprozess kapert, könnte neue Wege zu wirksameren, länger anhaltenden Therapien eröffnen.
Zelluläre Aufräumtruppen und die Überlebenstricks des Krebses
Mitochondrien leisten weit mehr als nur Energieerzeugung; sie steuern auch Stoffwechsel, Zelltod und den Umgang mit schädlichen Molekülen, den reaktiven Sauerstoffspezies. Wenn Mitochondrien beschädigt sind oder im Überschuss vorkommen, nutzen Zellen die Mitophagie, um sie zu markieren und zu entfernen. Das kann über zwei Hauptwege geschehen. Der eine, bekannt als PINK1/Parkin‑Signalweg, beruht auf einem Schadenssensor (PINK1) und einem Markierungsenzym (Parkin), die fehlerhafte Mitochondrien für den Abbau kennzeichnen. Der andere nutzt Rezeptorproteine wie BNIP3, NIX und FUNDC1 auf der Mitochondrienoberfläche, die diese direkt an die zellulären Abfallbehälter, die Autophagosomen, andocken, ohne denselben Markierungsschritt. Diese Wege arbeiten oft zusammen und geben Zellen flexible Möglichkeiten, ihren Mitochondrienbestand an Belastungen wie Sauerstoffmangel oder Medikamentenkontakt anzupassen. 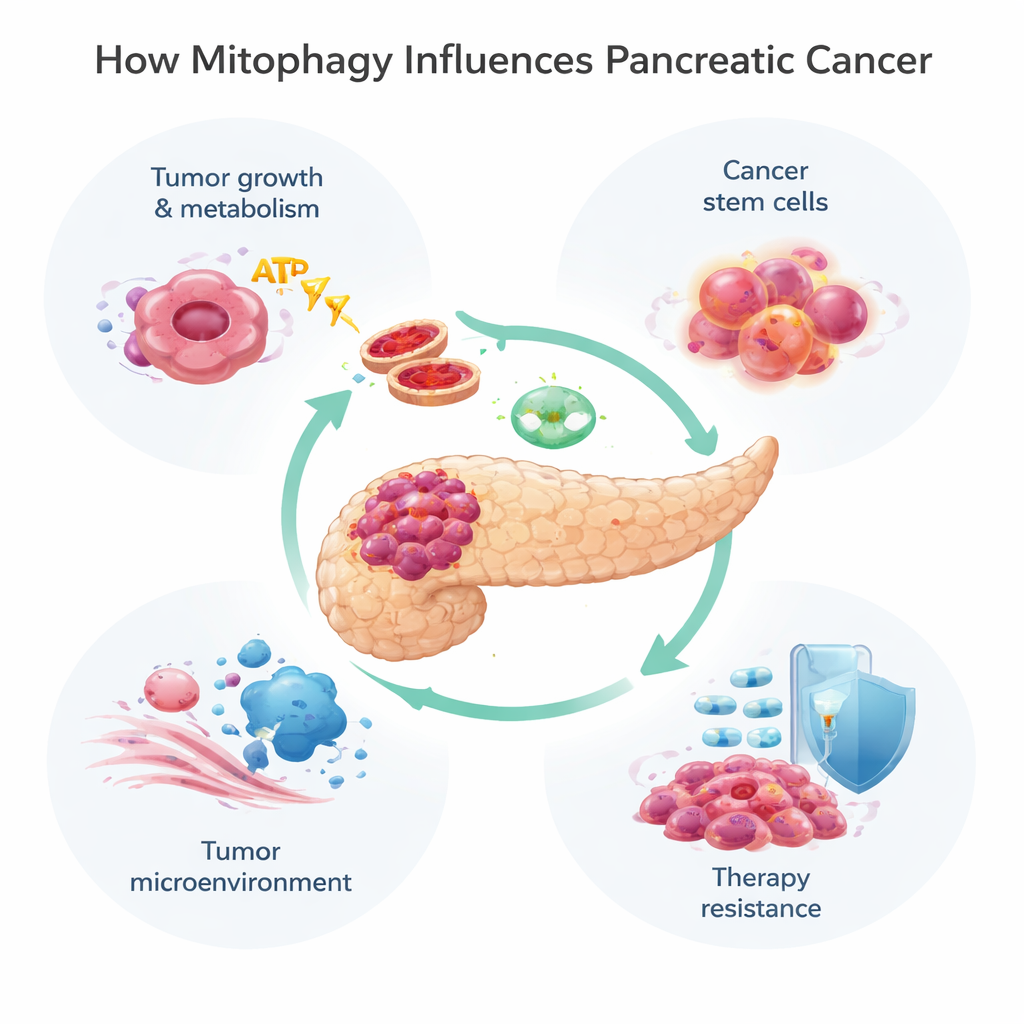
Wie Pankreastumoren ihren Energieeinsatz umgestalten
Pankreastumoren leben in einer harten Umgebung: Sie sind schlecht mit Blut und Sauerstoff versorgt und von dichtem, narbenähnlichem Gewebe umgeben. Um zu überleben, verdrahten Krebszellen ihre Energiesysteme um und verlagern sich oft von der sauerstoffabhängigen Atmung in Mitochondrien hin zu einem primitiveren Zuckerabbauprozess, der Glykolyse genannt wird. Mitophagie hilft, diese Umstellung fein abzustimmen. In frühen Stadien der Tumorentwicklung beschleunigt der Verlust von PINK1 oder Parkin die Krebsentstehung, indem er Eisenansammlungen, vermehrte reaktive Sauerstoffspezies und eine Verschiebung hin zur Glykolyse zulässt. Gleichzeitig kann ein anderes Mitophagieprotein, NIX, auch noch funktionierende Mitochondrien entfernen und Zellen weiter in Richtung glykolytischen Stoffwechsels und schnellerem Wachstum drängen. Im Gegensatz dazu zeigt BNIP3 ein komplexeres Muster: Es tritt früh auf, wird in vielen fortgeschrittenen Tumoren später stillgelegt und kann, wenn es wiederhergestellt wird, das Krebszellwachstum verlangsamen — ein Hinweis darauf, dass manche Mitophagie‑Wege den Krebs bremsen, während andere ihn antreiben.
Krebsstammzellen und das Umfeld des Tumors
Nicht alle Krebszellen sind gleich. Eine kleine Untergruppe, oft Krebsstammzellen genannt, kann sich selbst erneuern, neue Tumoren aussäen und Chemotherapie besonders gut überstehen. Bei Pankreaskrebs sind diese Zellen auf Mitophagie angewiesen, um metabolisch flexibel zu bleiben. Ein Modifikatorprotein namens ISG15 unterstützt diesen Prozess und hilft, ihre stammzellähnlichen Eigenschaften zu bewahren, womit Mitophagie direkt mit Rückfällen und Therapieversagen verknüpft ist. Über die Krebszellen hinaus formt Mitophagie auch das Tumormikromilieu — das Gemisch aus Stütz‑ und Immunzellen sowie Bindegewebe um den Tumor. Krebsassoziierte Fibroblasten können beispielsweise in einen „umgekehrten Warburg‑Effekt“ gedrängt werden, bei dem sie ihre eigene Mitophagie und Glykolyse hochfahren und den Tumor mit energiereichen Nebenprodukten versorgen. Mitophagie beeinflusst zudem, wie Immunzellen den Krebs erkennen und angreifen, indem sie die Präsentation von Immunmarkern wie MHC‑I und Bremsen wie PD‑L1 verändert, die Tumoren zur Tarnung nutzen.
Warum das Blockieren oder Fördern der Reinigung die Medikamentenantwort verändert
Viele Standard‑ und experimentelle Behandlungen gegen Pankreaskrebs, darunter das Chemotherapeutikum Gemcitabin und ein neues zielgerichtetes Medikament gegen die häufige KRAS‑G12D‑Mutation, schädigen Mitochondrien. Tumorzellen reagieren häufig, indem sie die Mitophagie hochfahren, den Schaden beseitigen und dem Zelltod entkommen. Studien zeigen, dass PINK1‑gesteuerte Mitophagie die tödliche Wirkung von Chemotherapie und einigen Naturstoffen abschwächen kann und so das Überleben von Krebszellen fördert. Andererseits kann unter bestimmten Bedingungen das Überstimulieren der Mitophagie — besonders über BNIP3 und NIX — zu einem Verlust zu vieler funktionierender Mitochondrien führen, die Zellen in eine Energiemangellage treiben und den Zelltod begünstigen. Diese doppelte Natur bedeutet, dass Mitophagie Tumoren entweder vor Behandlung schützt oder, wenn sie auf die richtige Weise manipuliert wird, verwundbarer macht. 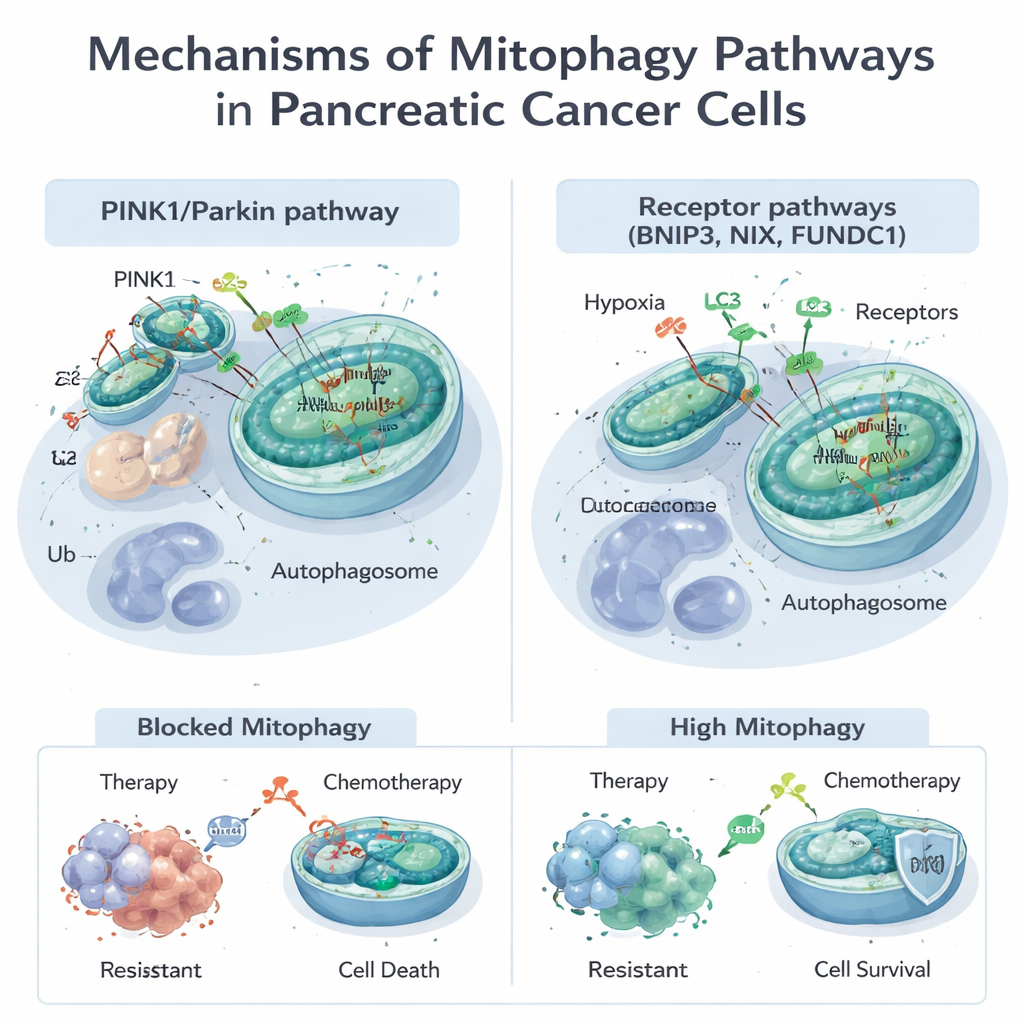
Neue Behandlungsansätze und die Notwendigkeit einer klugen Patientenauswahl
Weil Mitophagie im Schnittpunkt von Stoffwechsel, Stressantworten und Zelltod steht, ist sie ein attraktives Ziel für Kombinations‑Therapien. Aktuelle Arzneimittelstrategien wirken meist indirekt: Einige Verbindungen stören die mitochondriale Spaltung und Fusion; andere, wie Chloroquin und Hydroxychloroquin, blockieren die letzten Stadien des Recyclingprozesses, indem sie die Verschmelzung der Abfallbehälter mit sauren Abbaubereichen verhindern. Mehrere klinische Studien prüfen diese Medikamente in Kombination mit Standardchemotherapie beim Pankreaskrebs. Die Ergebnisse sind jedoch bislang gemischt — manche Patienten profitieren, andere nicht. Teil des Problems ist, dass Tumoren in ihrem Basalniveau an Mitophagie und Stoffwechselprofilen stark variieren: Einige sind stark auf mitochondriale Atmung angewiesen, andere auf Glykolyse. Die Autoren argumentieren, dass künftiger Erfolg von besseren Biomarkern und Gen‑Signaturen abhängen wird, um Patienten nach ihrer Mitophagie‑Aktivität und Energieverwendung zu gruppieren, sowie von der Entwicklung präziserer Arzneimittel, die spezifische Mitophagie‑Wege gezielt anpassen, statt Autophagie pauschal an‑ oder auszuschalten. Für Laien lautet die zentrale Erkenntnis: Das Erlernen des Lesens und sorgfältigen Anpassens dieses mitochondrialen Reinigungssystems könnte dazu beitragen, Pankreaskrebs von einem hartnäckigen Gegner in eine besser beherrschbare Krankheit zu verwandeln.
Zitation: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Schlüsselwörter: Pankreaskarzinom, Mitophagie, Mitochondrien, Chemotherapie‑Resistenz, Tumorstoffwechsel