Clear Sky Science · de
Vom kolorektalen Karzinom stammendes Osteopontin programmiert Makrophagen über die PI3K/AKT/CSF1-CSF1R-Achse in einen pro-metastatischen M2-Zustand um
Warum das für Menschen mit Darmkrebs wichtig ist
Die meisten Todesfälle durch kolorektales (Darm- und Enddarm-)Karzinom gehen nicht vom Primärtumor selbst aus, sondern von dessen Ausbreitung in andere Organe. Diese Studie untersucht, wie Krebszellen mit benachbarten Immunzellen „kommunizieren“, um die Tumorausbreitung zu fördern. Indem sie eine zentrale Botschaft enthüllen, die Krebszellen aussenden, um Immunzellen eher zu Helfern als zu Gegnern umzuprogrammieren, weist die Arbeit auf neue Behandlungsstrategien hin, die Metastasen bei fortgeschrittenem kolorektalen Krebs verlangsamen oder stoppen könnten.
Ein klebriges Protein mit dunkler Seite
Die Forschenden konzentrierten sich auf ein Protein namens Osteopontin (OPN), das sowohl von Krebszellen als auch von bestimmten Immunzellen im Tumor gebildet wird. OPN wird seit langem mit schlechteren Verläufen vieler Krebsarten in Verbindung gebracht, aber wie es die Ausbreitung beim kolorektalen Krebs fördert, war unklar. Durch die Analyse großer Patientendatenbanken und Tumorproben stellte das Team fest, dass die OPN-Spiegel im kolorektalen Tumorgewebe deutlich höher waren als im normalen Darmgewebe, insbesondere bei Patienten mit fortgeschrittener Krankheit und Fernmetastasen. Patienten mit tumoren, die höhere OPN-Werte aufwiesen, hatten im Allgemeinen eine schlechtere Überlebensrate, was darauf hindeutet, dass OPN eng mit aggressivem, schwer behandelbarem Krebs verknüpft ist.
Es sind nicht nur die Krebszellen selbst
Überraschenderweise wurden Kolorektalkrebszellen im Labor, bei denen die OPN-Produktion erhöht oder reduziert wurde, nicht auf eigene Faust invasiver oder mobiler. Ihr Wachstum, ihre Migration und ihre Fähigkeit, sich durch künstliche Membranen zu invasieren, änderten sich kaum. Das stellte die verbreitete Annahme infrage, OPN wirke hauptsächlich durch direkte Stärkung der Krebszellen. Stattdessen untersuchte das Team das Umfeld des Tumors – das sogenannte Tumormikromilieu –, insbesondere eine Gruppe von Immunzellen namens Makrophagen, die Tumore entweder angreifen (ein „M1“-Zustand) oder unterstützen (ein „M2“-Zustand).
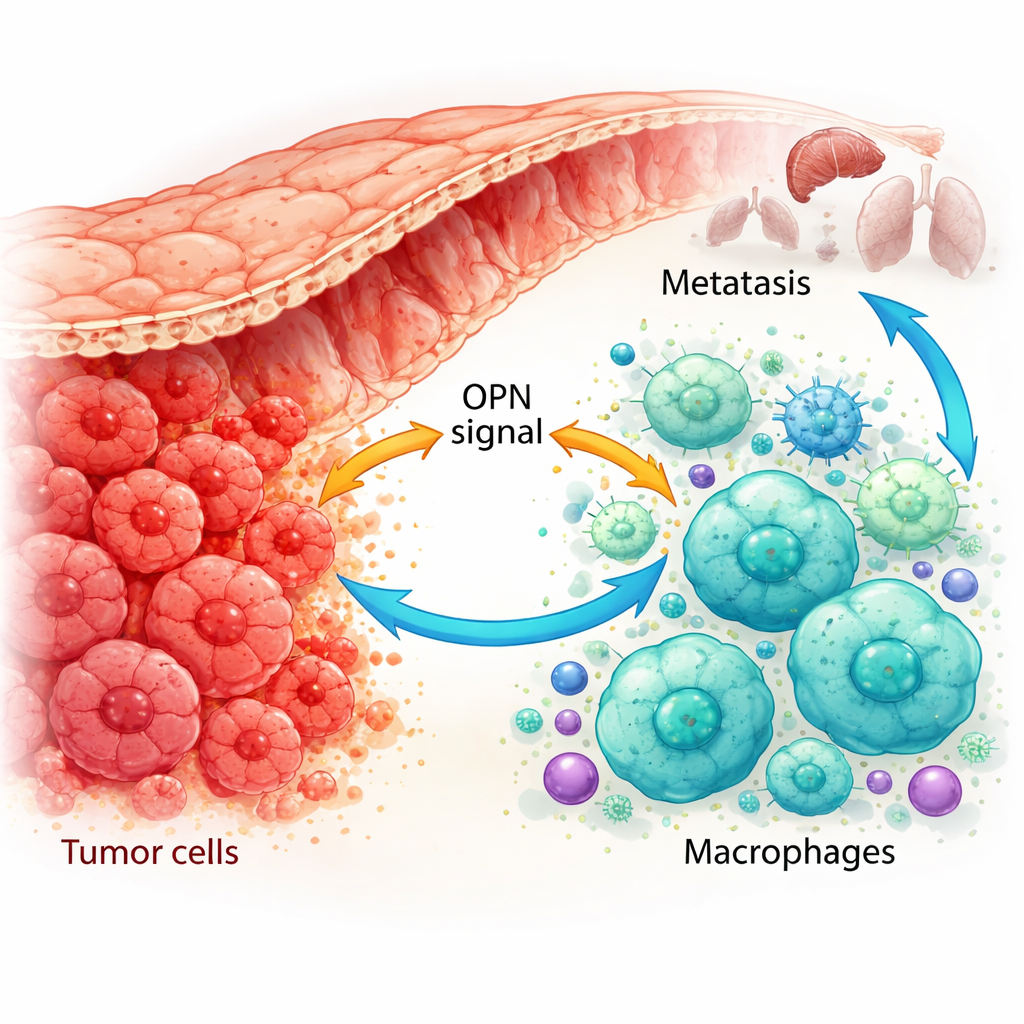
Wie Immunzellen zu Tumorhelfern umprogrammiert werden
Mithilfe von Einzelzell-Genkartierungen und fortgeschrittener Färbung von Patientenproben zeigten die Forschenden, dass OPN nicht nur von Krebszellen, sondern auch von tumorassoziierten Makrophagen produziert wird. In Tumoren, die bereits metastasiert hatten, waren sowohl die Krebszellen als auch ein spezifischer Makrophagen-Untertyp reich an OPN. Diese Makrophagen neigten zu einem M2-ähnlichen, tumorunterstützenden Zustand und waren häufiger, wenn die Tumor-OPN-Spiegel hoch waren. In Mausmodellen zogen Tumoren, die mehr OPN produzierten, mehr dieser M2-ähnlichen Makrophagen an und wuchsen schneller, während Tumoren mit reduziertem OPN weniger M2-Makrophagen hatten und langsamer wuchsen. Das legt nahe, dass OPN ein starker Rekrutierer und Umprogrammierer von Makrophagen im Tumorumfeld ist.
Die verborgene Signalkette: Von OPN zur Metastase
Um die molekulare Abfolge zu klären, kultivierte das Team humane Makrophagen zusammen mit kolorektalen Krebszellen, die unterschiedliche Mengen OPN produzierten. Sie fanden heraus, dass OPN-reiche Krebszellen Makrophagen in Richtung des M2-Zustands drängten und eine bidirektionale Bewegung förderten: Makrophagen wanderten zum Tumor, und Tumorzellen wurden in Reaktion auf Signale dieser Makrophagen invasiver. Bei genauerer Untersuchung entdeckten die Wissenschaftler, dass OPN in Makrophagen einen Signalweg namens PI3K/AKT aktiviert. Diese Aktivierung veranlasst Makrophagen wiederum, große Mengen eines anderen Moleküls, CSF1, freizusetzen und den Rezeptor für dieses Molekül, CSF1R, an ihrer Oberfläche hochzuregulieren. CSF1 wirkt dann in einer Schleife, um den M2-, pro-metastatischen Zustand weiter zu verstärken und weiterhin Makrophagen in den Tumor zu ziehen.
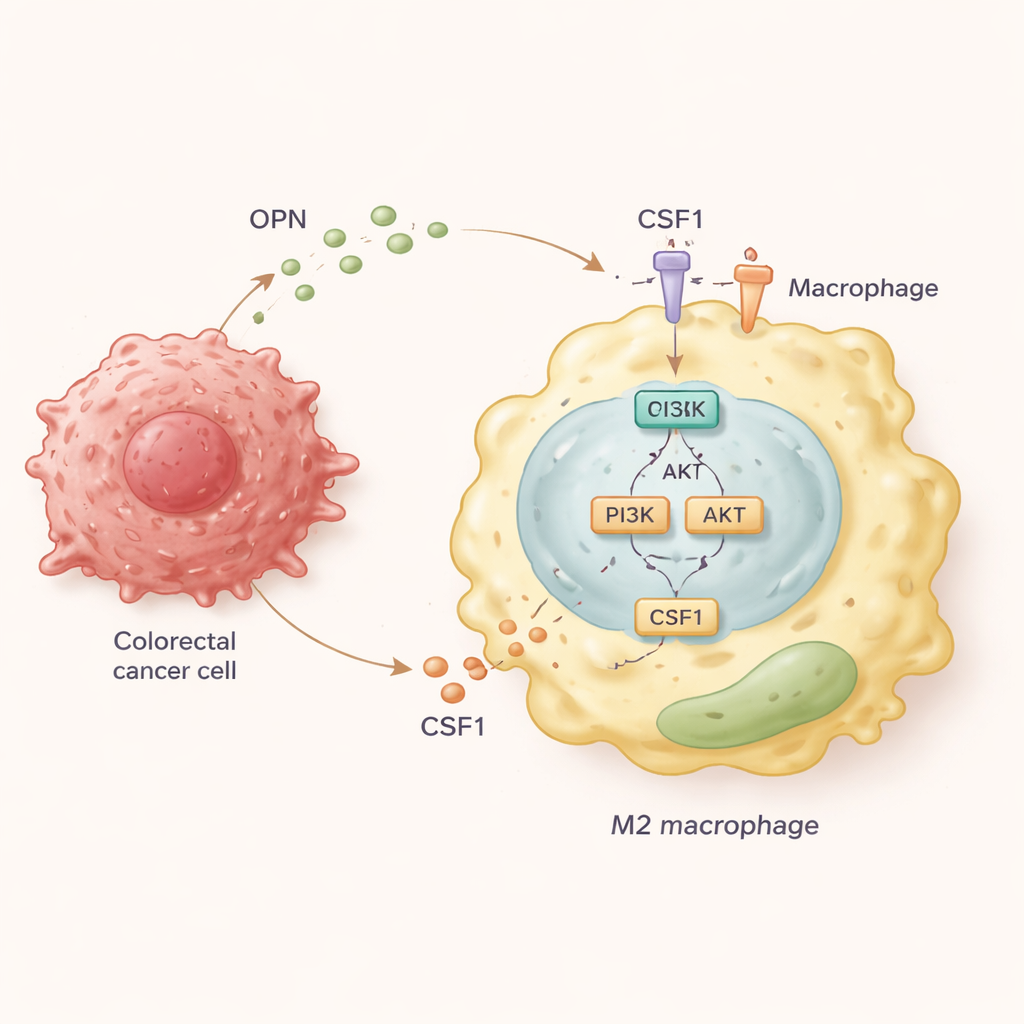
Die Schleife blockieren, um die Ausbreitung zu verlangsamen
In Mausmodellen des kolorektalen Krebses mit intraabdomineller Metastasierung testeten die Forschenden ein CSF1R-blockierendes Medikament namens PLX3397. Mäuse mit OPN-reichen Tumoren entwickelten viele metastatische Knötchen, aber die Behandlung mit dem CSF1R-Inhibitor reduzierte sowohl die Zahl der Metastasen als auch das Vorkommen von M2-ähnlichen Makrophagen in den Tumoren deutlich. Die Tumorzellen zeigten geringeres Wachstum und stärkere Anzeichen programmierter Zellsterblichkeit. Wichtig ist, dass das Medikament hauptsächlich die tumorfördernden Makrophagen dezimierte, ohne die entzündlicheren Typen stark zu beeinträchtigen, was auf eine relativ zielgerichtete Möglichkeit hinweist, das Unterstützungssystem des Tumors zu schwächen.
Was das für künftige Therapien bedeutet
Für Laien ist die Kernbotschaft, dass einige kolorektale Tumore nicht nur deshalb metastasieren, weil die Krebszellen an sich besonders aggressiv sind, sondern weil sie benachbarte Immunzellen kapern und zu Komplizen machen. In dieser Studie wirkt das von Krebszellen stammende OPN wie ein Hauptschalter, der Makrophagen über die PI3K/AKT- und CSF1/CSF1R-Signalkette umprogrammiert und so einen fruchtbaren Boden für Metastasen schafft. Durch das Unterbrechen dieser Kette – insbesondere am CSF1R-Punkt – konnten die Forschenden die Tumorausbreitung bei Mäusen verringern. Das legt nahe, dass die Messung von OPN-Werten dabei helfen könnte, Patienten zu identifizieren, die von Makrophagen-zielenden Medikamenten profitieren, und dass die Kombination solcher Wirkstoffe mit bestehenden Therapien oder Immuntherapien neue Hoffnung für Menschen mit fortgeschrittenem kolorektalem Krebs bieten könnte.
Zitation: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Schlüsselwörter: kolorektales Karzinom, Osteopontin, tumorassoziierte Makrophagen, Metastasen, CSF1R-Inhibition