Clear Sky Science · de
Gezielte Beeinflussung der NXPH4/ALDH1L2‑Signalgebung unterdrückt Enzalutamid‑Resistenz beim Prostatakrebs
Warum das für Prostatakrebs‑Patienten wichtig ist
Viele Männer mit fortgeschrittenem Prostatakrebs sind auf ein starkes Hormonblockerpräparat namens Enzalutamid angewiesen. Anfangs wirkt es oft gut, Tumoren schrumpfen und das Fortschreiten der Krankheit verlangsamt sich. Bei den meisten Patienten findet der Krebs jedoch irgendwann Wege, dem Medikament zu entkommen, und wächst wieder. Diese Studie untersucht, wie dieses Entkommen gelingt, und zeigt eine neue Schwachstelle in medikamentenresistenten Tumoren auf – was einen möglichen Ansatz bietet, bestehende Therapien länger und wirksamer zu machen.
Eine gängige Behandlung trifft auf eine hartnäckige Krankheit
Das Wachstum von Prostatakrebs hängt eng mit männlichen Hormonen, den Androgenen, zusammen, die über das Androgenrezeptor‑Protein wirken. Enzalutamid wurde entwickelt, um diesen Rezeptor zu blockieren, und ist eine Standardtherapie, wenn Tumoren nicht mehr auf die klassische Hormonentzugstherapie ansprechen. Leider passen sich viele Tumoren an und werden zu dem, was Ärztinnen und Ärzte als kastrationsresistenten Prostatakrebs bezeichnen. Die Autorinnen und Autoren dieser Arbeit wollten herausfinden, welche Gene den Krebszellen helfen, Enzalutamid zu überleben, in der Hoffnung, dass das Blockieren dieser Helfer die Wirkung des Medikaments wiederherstellen könnte.
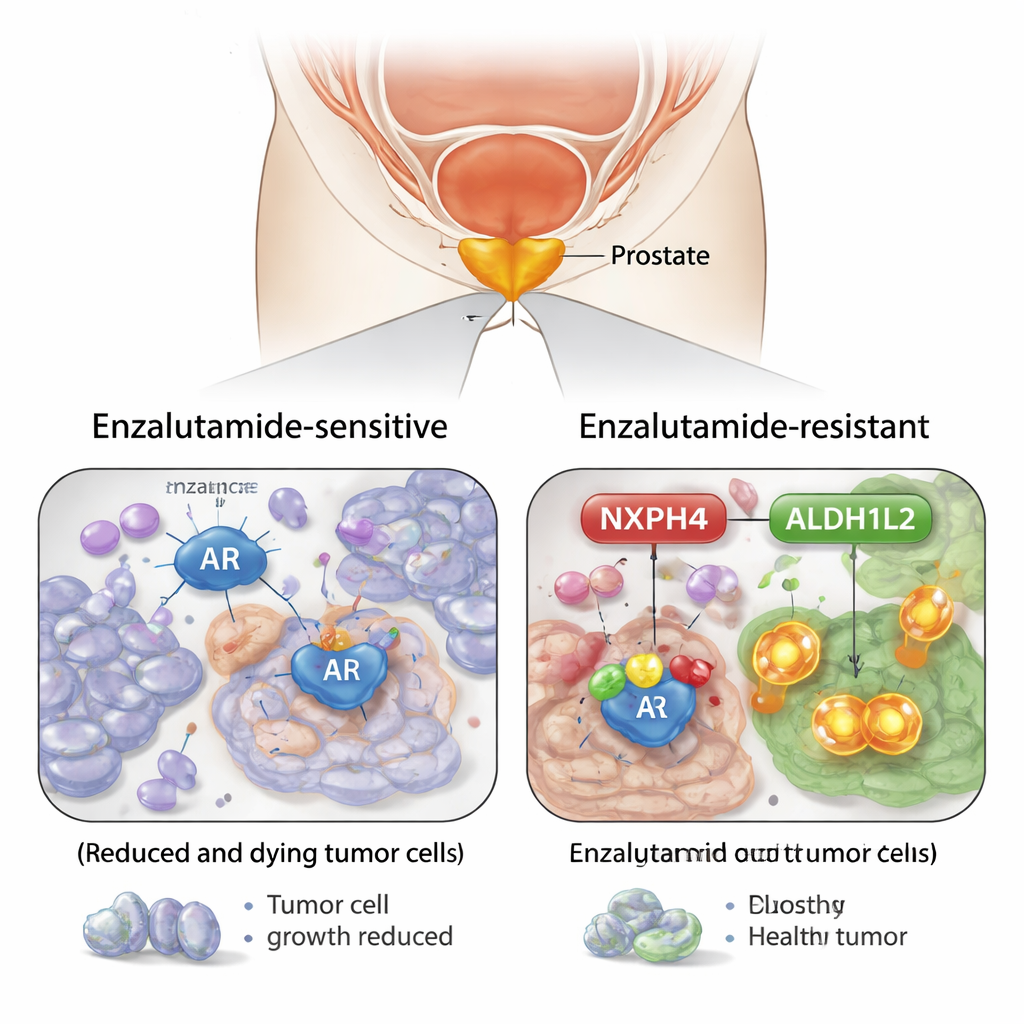
Ein überraschender Helfer im Rampenlicht
Durch den Vergleich von Prostatakrebszellen, die empfindlich auf Enzalutamid reagieren, mit solchen, die resistent geworden waren, identifizierte das Team ein Protein namens NXPH4 als Schlüsselakteur. Resistente Zellen produzierten deutlich mehr NXPH4, und die Menge stieg kontinuierlich an, wenn die Zellen über längere Zeit Enzalutamid ausgesetzt waren. Gewebeproben von Patientinnen und Patienten zeigten dasselbe Muster: höheres NXPH4 in aggressiveren Tumoren und in Krebsen, die nicht mehr auf das Medikament ansprachen. Als die Forschenden NXPH4 in resistenten Zellen reduzierten, wurden diese leichter durch Enzalutamid abgetötet und bildeten weniger Kolonien, sowohl im Kultursystem als auch in Mäusen. Im Gegensatz dazu machten Zellen mit künstlich erhöhtem NXPH4 sich schwerer behandeln.
Wie Hormone NXPH4 in Gang setzen
Die Studie ging auch der Frage nach, warum NXPH4 in diesen Tumoren so reichlich vorhanden ist. Die Antwort führte erneut zum Androgenrezeptor. Die Forschenden zeigten, dass Behandlung mit dem Hormon Dihydrotestosteron die NXPH4‑Spiegel erhöht. Zusätzliche Expression des Androgenrezeptors steigerte NXPH4; das Blockieren des Rezeptors senkte NXPH4. Detaillierte DNA‑Analysen bestätigten, dass der Androgenrezeptor physisch an die Kontrollregion des NXPH4‑Gens bindet und es einschaltet. Das bedeutet, dass dasselbe hormongesteuerte System, das das Prostatatumorwachstum antreibt, auch Zellen mit NXPH4 präpariert und so die Grundlage für spätere Arzneimittelresistenz legt.
Die Kraftwerke der Zelle hochfahren
Bei tiefergehenden Untersuchungen fanden die Forschenden, dass NXPH4 beeinflusst, wie Krebszellen Energie und Stress in ihren Mitochondrien managen, den kleinen Kraftwerken der Zelle. Unter hormonblockierenden Bedingungen wandert ein Teil von NXPH4 in die Mitochondrien und bindet dort an ein anderes Protein, ALDH1L2, das für die Produktion von NADPH wichtig ist — einem Schlüsselmolekül, das schädliche reaktive Sauerstoffspezies (ROS) kontrolliert. In resistenten Zellen bilden NXPH4 und ALDH1L2 einen Komplex, der die mitochondriale Atmung steigert, das Membranpotenzial erhält, NADPH erhöht und ROS‑Werte senkt. Diese Kombination hält die Mitochondrien funktionsfähig und erlaubt es den Krebszellen, den durch Enzalutamid ausgelösten Stress zu überstehen, anstatt wie gewöhnlich zu sterben.
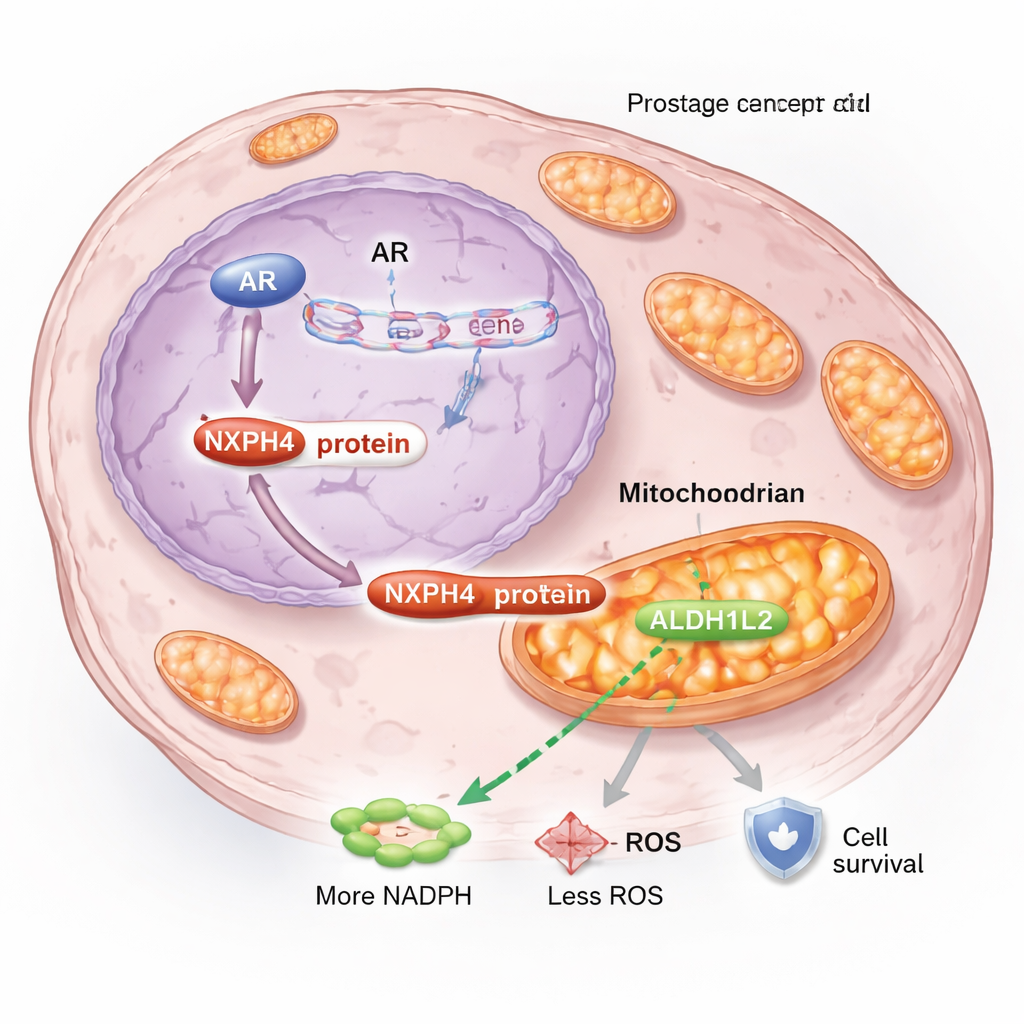
Die Widerstandsschaltung durchbrechen
Als die Forschenden dieses mitochondriale Unterstützungs‑System störten, waren die Ergebnisse deutlich. Das Herunterregulieren von NXPH4 in resistenten Zellen verringerte die mitochondriale Aktivität, erhöhte den oxidativen Stress, verlangsamte das Wachstum und machte die Zellen deutlich anfälliger für Enzalutamid. Das Stilllegen von ALDH1L2 zeigte einen ähnlichen Effekt und beseitigte die schützenden Vorteile von erhöhtem NXPH4, was bestätigte, dass diese beiden Proteine zusammenarbeiten. In Mausmodellen wuchsen Tumoren ohne NXPH4 langsamer, und die Kombination aus NXPH4‑Verlust und Enzalutamid verkleinerte Tumoren stärker als jede der Maßnahmen allein. Diese Befunde deuten darauf hin, dass die NXPH4–ALDH1L2‑Partnerschaft nicht nur ein Begleiteffekt der Resistenz ist, sondern eine treibende Kraft dahinter.
Was das für künftige Behandlungen bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass einige Prostatakrebszellen Enzalutamid überleben, indem sie ihre Energieversorgung umprogrammieren. NXPH4, vom Androgenrezeptor eingeschaltet, arbeitet mit ALDH1L2 in den Mitochondrien zusammen, um deren Funktion aufrechtzuerhalten, vor oxidativem Schaden zu schützen und Tumorzellen das Überdauern der Hormonblockade zu ermöglichen. Das Anvisieren von NXPH4 oder seiner Interaktion mit ALDH1L2 könnte diesen Überlebenskreis schwächen. Zwar gibt es noch keine Medikamente gegen NXPH4, doch hebt die Studie dieses Molekül‑Paar als vielversprechendes neues Ziel hervor. Künftig könnte die Kombination von Enzalutamid mit Wirkstoffen, die die NXPH4‑ALDH1L2‑Signalgebung stören, Patientinnen und Patienten helfen, der resistenten Form des Prostatakrebses länger zuvorzukommen.
Zitation: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
Schlüsselwörter: Prostatakrebs, Enzalutamid‑Resistenz, mitochondriale Stoffwechsel, NXPH4, ALDH1L2