Clear Sky Science · de
Trim15 stabilisiert VDAC3 durch Ubiquitinierung, um Autophagie zu unterdrücken und die Chemosensitivität bei Plattenepithelkarzinom des Hypopharynx zu erhöhen
Warum diese Krebsstudie wichtig ist
Das Plattenepithelkarzinom des Hypopharynx ist ein schwer zu behandelnder Rachenkrebs mit niedrigen Überlebensraten und wenigen wirksamen Optionen, wenn er metastasiert oder nicht mehr auf Medikamente anspricht. Diese Studie deckt einen bislang wenig beachteten zellulären Weg auf, der mitentscheidet, ob Krebszellen unter Therapie absterben oder sich still anpassen und überleben. Indem sie erklärt, wie zwei Proteine, Trim15 und VDAC3, die zelluläre Selbstreinigung und Stressantworten steuern, weist die Arbeit auf neue Ansätze hin, bestehende Chemotherapeutika wirksamer zu machen.
Ein tödlicher Rachenkrebs, der sich im Verborgenen hält
Der Hypopharynx liegt tief im Rachen, sodass Tumoren dort oft unbemerkt wachsen, bis sie ein fortgeschrittenes Stadium erreichen. Dann müssen Ärztinnen und Ärzte zwischen aggressiver Chirurgie, die Sprache und Schlucken stark beeinträchtigen kann, und organerhaltenden Ansätzen wie Chemotherapie und Strahlentherapie wählen, die nicht immer heilen. Da sich die Überlebensraten in den letzten Jahrzehnten kaum verbessert haben, richten Forscher ihren Blick über traditionelle Therapien hinaus auf die zugrundeliegende Biologie, die es diesen Tumoren erlaubt zu wachsen, zu metastasieren und Medikamenten zu widerstehen. Die vorliegende Studie konzentriert sich darauf, wie Krebszellen mit beschädigten Mitochondrien — ihren Energieproduktionsstätten — umgehen und wie das ihre Reaktion auf Stress und Therapie prägt.
Ein Wächterprotein verschwindet
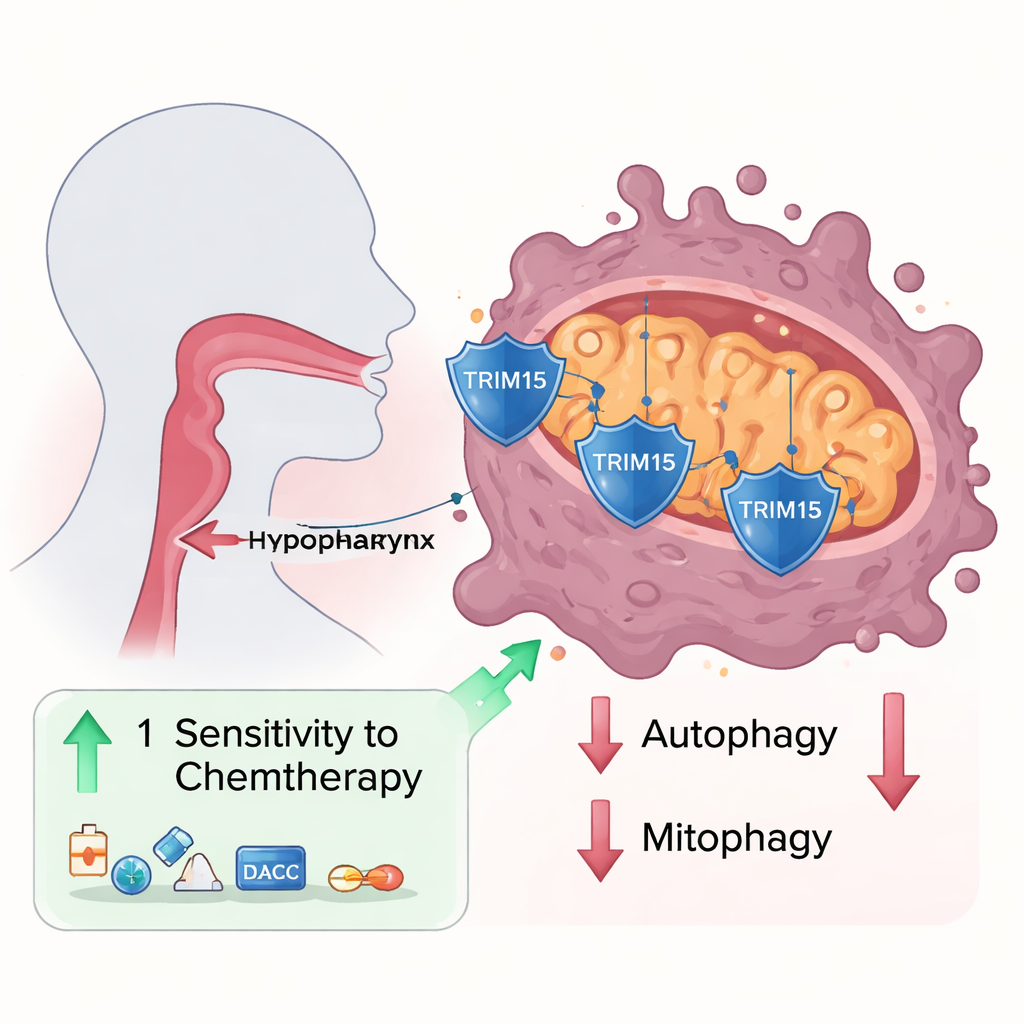
Die Forschenden untersuchten Tumorproben und Zelllinien aus Hypopharynxkarzinomen und stellten fest, dass das Protein Trim15 im Vergleich zum angrenzenden Normalgewebe durchgehend reduziert war. Wenn sie Krebszellen zwangen, mehr Trim15 zu produzieren, wuchsen und wanderten die Zellen langsamer; entfernten sie es, wurden die Zellen aggressiver. Biochemische Pull‑down‑Experimente zeigten, dass Trim15 physisch mit einem anderen Protein, VDAC3, interagiert, das in der äußeren Mitochondrienmembran sitzt und als Tor für den Molekültransport dient. Anstatt VDAC3 für den Abbau zu kennzeichnen, fügt Trim15 eine spezifische molekulare Markierung hinzu, die VDAC3 tatsächlich stabilisiert und dessen Gehalt hochhält.
Wie Krebszellen ihre Kraftwerke recyceln
Mitochondrien werden kontinuierlich überwacht und bei Schäden über einen spezialisierten Recyclingprozess, die Mitophagie, entfernt. Das Team zeigte, dass VDAC3 normalerweise als Bremse für dieses Recycling wirkt. Wenn VDAC3 reichlich vorhanden war, sanken Marker für allgemeine Autophagie und Mitophagie; war VDAC3 reduziert, beschleunigten sich diese Prozesse, und mehr Mitochondrien wurden eingeschlossen und abgebaut. Diese Veränderung beeinflusste auch das Gleichgewicht reaktiver Sauerstoffspezies (ROS) — chemisch reaktive Moleküle, die oft als zellulärer Abgasstrom beschrieben werden. Hoher VDAC3‑Spiegel trieb die ROS‑Werte nach oben und belastete die Zellen stärker, während niedriger VDAC3 den Zellen erlaubte, beschädigte Mitochondrien zu beseitigen, ROS zu senken und unter widrigen Bedingungen besser zu überleben.
Alkohol, oxidativer Stress und Medikamentenresistenz
Chronischer Alkoholkonsum ist ein wichtiger Risikofaktor für Hypopharynxkarzinome, teilweise weil konzentrierter Ethanol die Rachenschleimhaut wiederholt reizt. Als die Forschenden Krebszellen im Labor Alkohol aussetzten, sanken sowohl Trim15‑ als auch VDAC3‑Spiegel. Dieser Abfall schien eine adaptive Reaktion der Krebszellen zu sein: Durch Abschwächung der Trim15–VDAC3‑Achse steigerten sie die Mitophagie, hielten ROS auf sichereren Niveaus und tolerierten alkoholbedingte Schäden besser. Eine ähnliche Reaktion zeigte sich bei der Standardchemotherapie mit 5‑Fluorouracil (5‑FU): Die Behandlung senkte Trim15 und VDAC3, was vermutlich den Tumorzellen hilft, tödlichem oxidativem Stress zu entgehen und zur Chemoresistenz beiträgt.
Selbstschutz abschalten, um die Chemotherapie zu verstärken
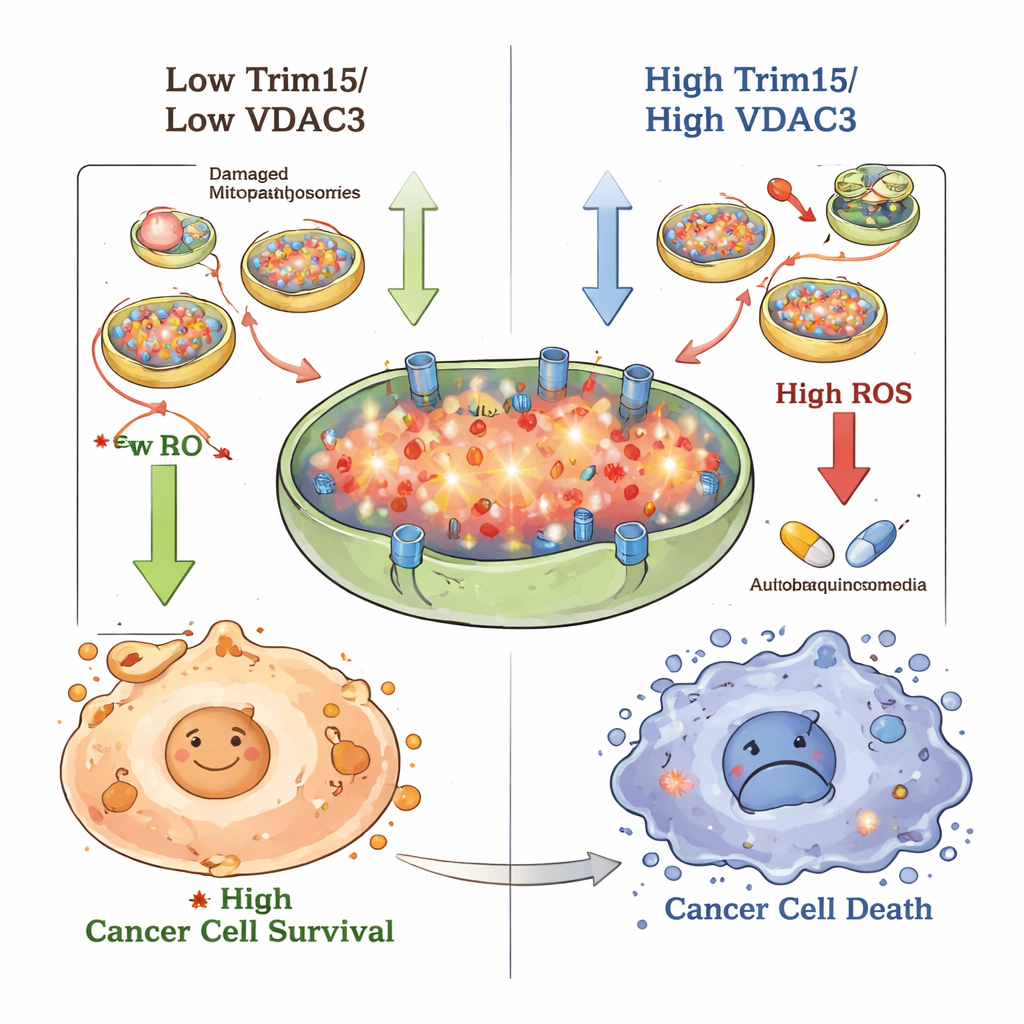
Das Team fragte dann, ob das Blockieren der Autophagie diesen Schutz aufheben könnte. Sie verwendeten Chloroquin, ein lange bekanntes Antimalariamittel, das die letzten Schritte der zellulären Selbstverdauung stört. In Zellkultur verlangsamte Chloroquin allein das Wachstum und die Migration von Hypopharynx‑Krebszellen und nahm den Zellen den Wachstumsvorteil, der durch VDAC3‑Verlust entsteht. Bei Mäusen mit menschlichen Tumortransplantaten verkleinerten sowohl Chloroquin als auch 5‑FU die Tumoren, aber die Kombination wirkte am besten und verringerte Tumorvolumen und ‑gewicht stärker als eines der Medikamente allein, ohne offensichtliche zusätzliche Toxizität. Wichtig ist, dass das erzwungene Überproduzieren von Trim15 oder VDAC3 die Zellen gegenüber 5‑FU empfindlicher machte, teilweise indem ROS auf Werte stiegen, die die Zellen nicht mehr bewältigen konnten.
Was das für künftige Behandlungen bedeutet
Für Laien zeigt die Studie, dass einige Hypopharynx‑Krebszellen Chemotherapie überleben, indem sie bessere Recyclingspezialisten werden: Sie räumen beschädigte Mitochondrien schnell weg und halten den oxidativen Stress gerade noch so niedrig, dass sie nicht absterben. Trim15 und VDAC3 wirken gemeinsam als Gegengewicht zu diesem Verhalten — sind sie vorhanden, begrenzen sie das Recycling und erhöhen den Stress, wodurch Krebszellen leichter zu töten sind. Durch das Anvisieren dieser Trim15–VDAC3–Mitophagie‑Achse, beispielsweise mit Medikamenten wie Chloroquin zusätzlich zur Standardchemotherapie, könnten Ärztinnen und Ärzte möglicherweise hartnäckige Rachentumoren empfänglicher für Behandlung machen und die Patientenergebnisse verbessern.
Zitation: Wang, G., Shen, Y., Wang, L. et al. Trim15 stabilizes VDAC3 via ubiquitination to suppress autophagy and enhance chemosensitivity in hypopharyngeal squamous cell carcinoma. Cell Death Discov. 12, 88 (2026). https://doi.org/10.1038/s41420-026-02943-0
Schlüsselwörter: Hypopharynxkarzinom, Autophagie, Mitochondrien, Chemotherapie‑Resistenz, Chloroquin