Clear Sky Science · de
Rottlerin löst die doppelte Abbau von SLC7A11 und GPX4 aus, um Ferroptose und Chemosensibilisierung beim hepatozellulären Karzinom zu fördern
Warum diese natürliche Verbindung für Leberkrebs wichtig ist
Das hepatozelluläre Karzinom, die häufigste Form des primären Leberkrebses, wird oft spät diagnostiziert und ist weiterhin schwer zu behandeln. In dieser Studie wird untersucht, ob ein pflanzlich gewonnenes Molekül namens Rottlerin, das seit langem für seine breit gefächerten antitumoralen Wirkungen bekannt ist, genutzt werden kann, um eine neuere Form des Zelltods namens Ferroptose in Leberkrebszellen auszulösen. Durch das Verständnis der molekularen Wirkungsweise von Rottlerin hoffen die Forschenden, neue Wege für effektivere und weniger leicht umgehbare Behandlungen zu eröffnen.
Ein neuer Weg, Krebszellen zu töten
Konventionelle Krebsmedikamente treiben Tumorzellen meist in bekannte Todesprogramme wie die Apoptose. Ferroptose ist anders: Sie ist ein eisenabhängiger Prozess, der durch die Anhäufung toxischer Fette in Zellmembranen angetrieben wird. Leberkrebszellen sind besonders anfällig für solche Schäden, weil sie stark auf Antioxidantien angewiesen sind, um diese fettbasierten Toxine in Schach zu halten. Das Team fragte, ob Rottlerin diese Abwehrmechanismen sabotieren und so Leberkrebszellen in die Ferroptose treiben kann.
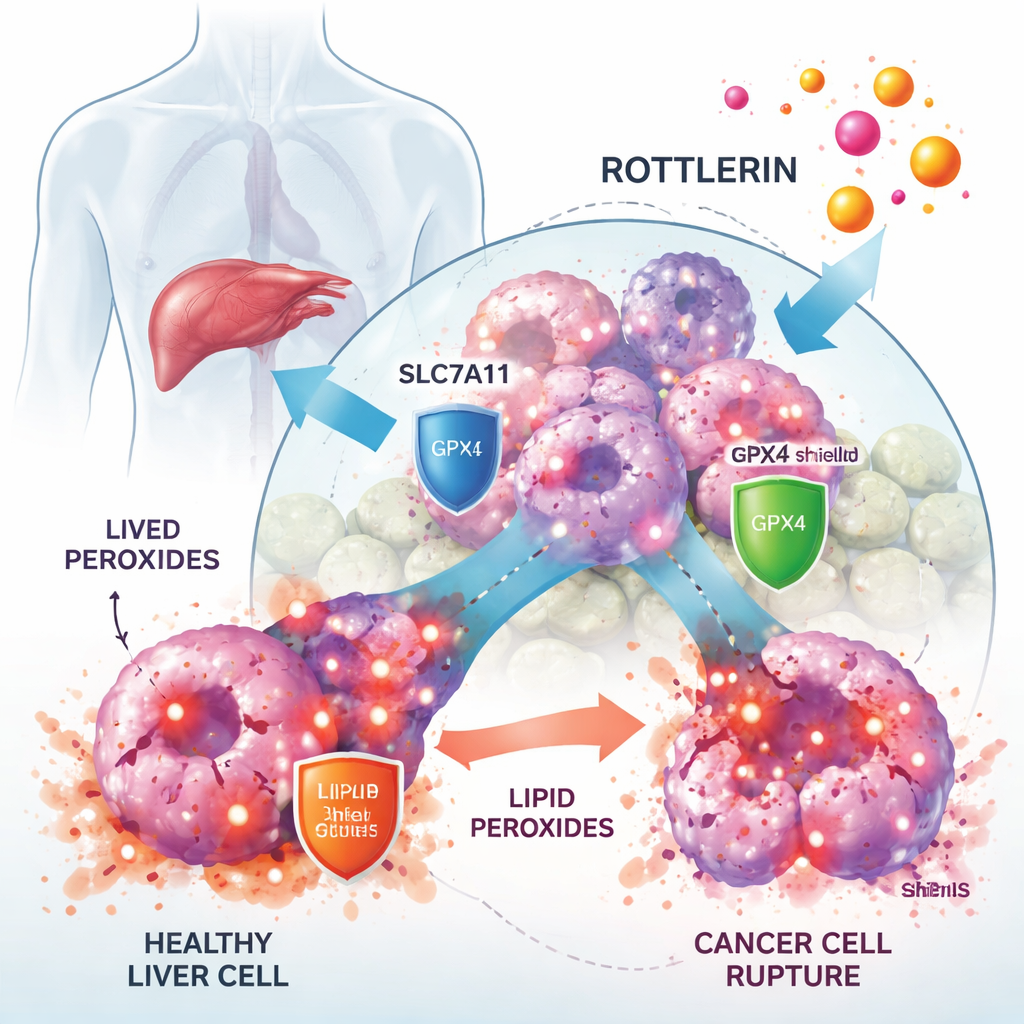
Wie Rottlerin das Tumorwachstum verlangsamt
An hand von humanen Leberkrebszelllinien zeigten die Forschenden, dass Rottlerin das Wachstum der Krebszellen bereits in niedrigen Mikromolaren Dosen stark reduzierte, während normale leberbezogene Zellen weniger betroffen waren. Als sie einen spezifischen Ferroptose‑Blocker namens Ferrostatin‑1 zusetzten, wurde ein großer Teil des durch Rottlerin ausgelösten Zelltods verhindert, was stark darauf hinweist, dass Ferroptose der hauptsächliche Todesmodus war. Mikroskopie und biochemische Tests stützten diese Beobachtungen: Rottlerin‑behandelte Zellen häuften hohe Spiegel von Lipidperoxiden an, zeigten veränderte Mitochondrien und wiesen verringerte Mengen des Antioxidans Glutathion auf — alles Merkmale der Ferroptose.
Die antioxidativen Schilde der Zellen entwaffnen
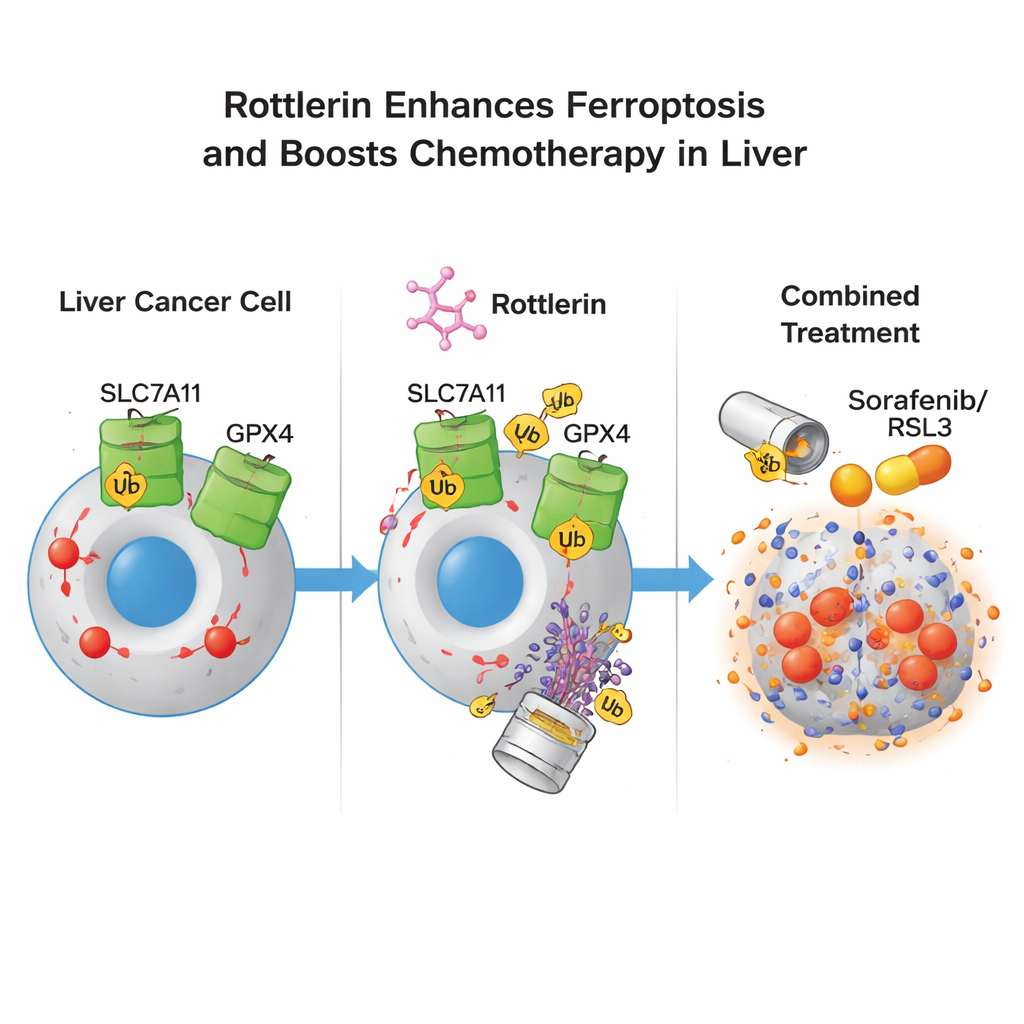
Leberkrebszellen überleben, indem sie auf eine zentrale Abwehrachse aus dem Transporter SLC7A11 und dem Enzym GPX4 bauen. SLC7A11 importiert Cystin, einen Baustein für Glutathion, während GPX4 Glutathion verwendet, um Lipidperoxide zu neutralisieren, bevor sie Membranen schädigen. Die Studie fand heraus, dass Rottlerin sowohl die Proteinmengen von SLC7A11 als auch von GPX4 im Laufe der Zeit verringerte. Dies lag nicht daran, dass die Zellen weniger davon produzierten, sondern weil die Proteine mit kleinen „Zerstöre mich“-Markern (Ubiquitin) versehen und in die eiweißzerstörende Maschinerie der Zelle, das Proteasom, eingeschleust wurden. Das Blockieren des Proteasoms kehrte diesen Verlust um, und das künstliche Anheben von SLC7A11 oder GPX4 in den Zellen schützte sie teilweise vor Rottlerin. Zusammengenommen zeigen diese Befunde, dass Rottlerin als Doppel‑Degrader von zwei zentralen Ferroptose‑Schutzfaktoren wirkt.
Bestehende Leberkrebsmedikamente verstärken
Viele Patientinnen und Patienten mit fortgeschrittenem Leberkrebs erhalten Sorafenib, ein Standard‑Erstlinienmedikament, das selbst Ferroptose auslösen kann, dessen Nutzen jedoch häufig durch Resistenz eingeschränkt wird. Die Autorinnen und Autoren testeten, ob niedrige, sonst schwache Dosen von Rottlerin Tumorzellen empfindlicher für Ferroptose‑induzierende Wirkstoffe wie Sorafenib und RSL3 machen könnten. In Zellkultur führte die Kombination von Niedrigdosis‑Rottlerin mit einem der beiden Wirkstoffe zu deutlich mehr Krebszelltod und verschob die Dosis‑Wirkungs‑Kurven zugunsten stärkerer Wirksamkeit. Wichtig ist, dass dieser sensibilisierende Effekt bestehen blieb, selbst wenn das klassische Rottlerin‑Zielprotein PKCδ genetisch reduziert wurde, was zeigt, dass die Schlüsselfunktion nicht über diese Kinase, sondern über den Abbau von SLC7A11 und GPX4 vermittelt wird. In Mausmodellen mit humanen Lebertumoren verlangsamte die kombinierte Behandlung mit Rottlerin und Sorafenib das Tumorwachstum stärker als Sorafenib allein und senkte zusätzlich die SLC7A11‑ und GPX4‑Spiegel in den Tumoren.
Was das für künftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten lautet die Botschaft: Rottlerin wirkt wie ein „Doppel‑Dietrich“ an Leberkrebszellen — es entfernt gleichzeitig zwei entscheidende Schlösser, SLC7A11 und GPX4, die Zellen normalerweise vor einer tödlichen Welle fettbasierter Oxidation schützen. Sind diese Schlösser erst weg, werden Krebszellen deutlich anfälliger für Ferroptose, insbesondere in Kombination mit vorhandenen Medikamenten, die sie in diese Richtung treiben. Obwohl noch mehr Forschung nötig ist, bevor Rottlerin oder verwandte Verbindungen beim Menschen eingesetzt werden können, bietet diese Doppel‑Degrader‑Strategie einen vielversprechenden Ansatz, um die adaptiven Abwehrmechanismen zu umgehen, die Lebertumoren so schwer behandelbar machen.
Zitation: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Schlüsselwörter: Leberkrebs, Ferroptose, Rottlerin, SLC7A11, GPX4