Clear Sky Science · de
Aktivierung von GCN2 und anschließend der „Unfolded Protein Response“ mit dem kleinen oralen Wirkstoff NXP800 verzögert das Tumorwachstum beim Osteosarkom
Den Stress von Krebs in eine Schwäche verwandeln
Osteosarkom ist ein seltener, aber aggressiver Knochentumor, der vor allem Kinder und junge Erwachsene trifft. Jahrzehntelang basierten die Behandlungen auf intensiver Chemotherapie und Operationen, doch die Überlebenschancen bei fortgeschrittener Erkrankung haben sich kaum verbessert. Diese Studie untersucht eine neue Tablette namens NXP800, die eine verborgene Schwäche von Krebszellen ausnutzen soll: ihren ständigen Kampf mit innerem Stress. Indem NXP800 diesen Stress über einen Kipppunkt hinaus steigert, könnte es Tumorzellen zur Selbstzerstörung zwingen und dabei die meisten gesunden Zellen schonen.
Ein hartnäckiger Knochenkrebs, der neue Optionen braucht
Osteosarkome wachsen meist in den langen Röhrenknochen von Armen und Beinen und können rasch in die Lunge streuen. Die Standardbehandlung kombiniert mehrere starke Chemotherapeutika mit operativem Tumorentfernen. Während dieses Vorgehen viele Patientinnen und Patienten mit lokal begrenzter Erkrankung heilt, sind die Aussichten bei wiederkehrenden oder bereits metastasierten Tumoren schlecht. Da die aktuellen Medikamente an ihre Grenzen gestoßen sind, suchen Forscher nach Therapien, die Osteosarkome auf völlig neue Weise angreifen—ideal wären Ansätze, die Eigenschaften nutzen, die Krebszellen von gesundem Gewebe unterscheiden.
Den Stress gegen Tumorzellen wenden
Krebszellen leben unter ständigem Druck: Sie teilen sich schnell, verbrauchen viel Energie und Sauerstoff und sind oft widrigen Bedingungen wie Sauerstoffmangel oder Chemotherapie ausgesetzt. Um das zu überstehen, verlassen sie sich auf Notfall-Systeme, die helfen, Proteine korrekt zu falten und den Stoffwechsel anzupassen. Eines dieser Systeme ist die „Unfolded Protein Response“ (UPR), die ausgelöst wird, wenn die Proteinfabrik der Zelle, das endoplasmatische Retikulum, überlastet ist. Ein anderes ist die „integrierte Stressantwort“, die verschiedene Stressarten erkennt und die Proteinproduktion drosselt. Normalerweise helfen diese Wege Krebszellen beim Überleben—werden sie jedoch zu stark und zu lange aktiviert, können sie vom Schutzmechanismus zur Auslöserin des Zelltods umschlagen.
NXP800 trifft einen zentralen Stresstaster
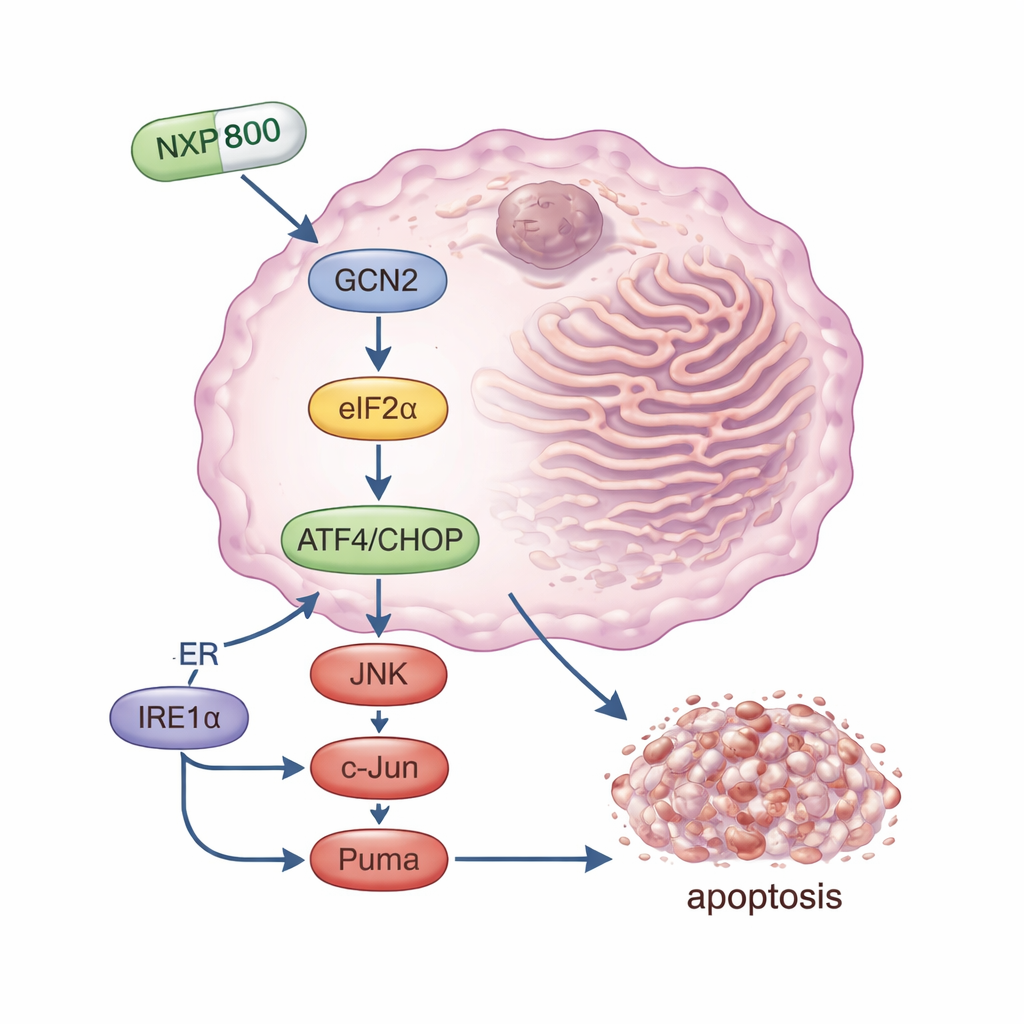
NXP800 ist ein oral verfügbarer kleiner Wirkstoff, der ursprünglich entwickelt wurde, um einen Hitzeschock-Weg zu blockieren, der am Überleben von Krebs beteiligt ist. In dieser Studie entdeckten die Forschenden, dass seine Hauptwirkung in Osteosarkomzellen eine andere ist: Er aktiviert stark ein stressdetektierendes Protein namens GCN2. Einmal eingeschaltet, modifiziert GCN2 den Faktor eIF2α, wodurch die Gesamtproteinproduktion rasch sinkt, während die Konzentration bestimmter Stress‑„Master‑Schalter“ ansteigt—insbesondere das Protein ATF4 und dessen Partner CHOP. Zusammen treiben diese Moleküle die Zelle in Richtung programmierten Zelltods. Das Team zeigte, dass bei Blockade von GCN2—entweder durch Stilllegung des Gens oder mit einem separaten Inhibitor—NXP800 diese Reaktionskette nicht mehr effektiv auslösen konnte und die Krebszellen deutlich weniger empfindlich gegenüber dem Wirkstoff waren. Das macht GCN2 in Osteosarkomen zu einem entscheidenden Ziel von NXP800.
Mehrere Todeswege im Tumor aktivieren
Über den GCN2‑Arm des Stressnetzwerks hinaus schaltete NXP800 auch einen anderen zelltodverknüpften Weg an. Es aktivierte den Sensor IRE1α, der seinerseits die Signalmoleküle JNK und c‑Jun stimulierte. Dieser Zweig fördert die Produktion von Puma, einem starken pro‑apoptotischen Molekül, das die inneren Überlebensmechanismen der Zelle schädigt. In Laborversuchen verlangsamte NXP800 das Wachstum von Osteosarkomzellen, stoppte ihren Zellzyklus und aktivierte Enzyme sowie Proteinveränderungen, die für Apoptose, also kontrollierten Zelltod, charakteristisch sind. Wichtig ist, dass normale, knochenbezogene Stammzellen deutlich weniger betroffen waren, was auf eine gewisse Selektivität gegenüber Tumorzellen hindeutet, die bereits am Rande des tolerierbaren Stresses leben.
Vom Labortisch zu lebenden Modellen
Um zu prüfen, ob diese zellulären Effekte in echte Tumorkontrolle übersetzen, testeten die Forschenden NXP800 an Mäusen, die mit menschlichen Osteosarkomzellen in der Nähe der Tibia transplantiert worden waren. Mäuse, die NXP800 peroral erhielten, entwickelten deutlich langsamer wachsende Tumore, die am Studienende in etwa halb so groß waren wie die Tumore unbehandelter Tiere. Tumorproben aus behandelten Tieren zeigten eindeutige Hinweise auf den Wirkmechanismus: erhöhte Werte der Stressmarker eIF2α und ATF4, weniger sich teilende Zellen und mehr Zellen unter Apoptose. Separate Sicherheitsstudien an gesunden Mäusen ergaben keinen größeren Organschaden, und Leberwerte verschlechterten sich nicht, was für ein handhabbares Sicherheitsprofil bei den verwendeten Dosen spricht.
Was das für Patientinnen und Patienten bedeuten könnte
In der Summe zeigen diese Daten, dass NXP800 das Wachstum von Osteosarkomen verzögern kann, indem es die eigenen Stressabwehrmechanismen der Krebszelle so stark überdreht, dass sie zur Selbstzerstörung führen. Durch die gezielte Ansprache des GCN2‑Sensors und verwandter Wege bietet der Wirkstoff einen ganz neuen Ansatz, Tumore zu schwächen, die gegen klassische Chemotherapien resistent sind. Da NXP800 bereits in frühen klinischen Studien für andere Krebsarten geprüft wird, eröffnen sich Möglichkeiten, den Wirkstoff für Osteosarkome neu zu positionieren—entweder allein oder in Kombination mit bestehenden Therapien. Obwohl klinische Studien am Menschen nötig sind, um Nutzen und Sicherheit zu bestätigen, liefert diese Studie einen überzeugenden Proof‑of‑Principle dafür, dass das Umdrehen zellulären Stresses gegen den Tumor einen neuen therapeutischen Weg für diese schwere Knochentumorerkrankung eröffnen kann.
Zitation: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
Schlüsselwörter: Osteosarkom, NXP800, Stressreaktion, GCN2-Signalweg, Apoptose