Clear Sky Science · de
Von BMSC stammende extrazelluläre Vesikel fördern Proliferation und Metastasierung von Osteosarkomen über den circRNA-0010220/β‑Catenin‑Weg
Warum diese Knochenkrebs‑Geschichte wichtig ist
Das Osteosarkom ist der häufigste Knochentumor bei Kindern und jungen Erwachsenen und metastasiert häufig in die Lunge. Selbst mit moderner Chemotherapie und Operation treten bei vielen Patienten Rückfälle und lebensbedrohliche Metastasen auf. Diese Studie untersucht die verborgenen „Gespräche“ zwischen Knochenkrebszellen und benachbarten Stammzellen im Knochenmark und deckt einen winzigen molekularen Botenstoff auf, der Tumoren beim Wachsen und Ausbreiten hilft — und der zu einem neuen therapeutischen Ziel werden könnte.
Kleine Pakete mit großer Wirkung
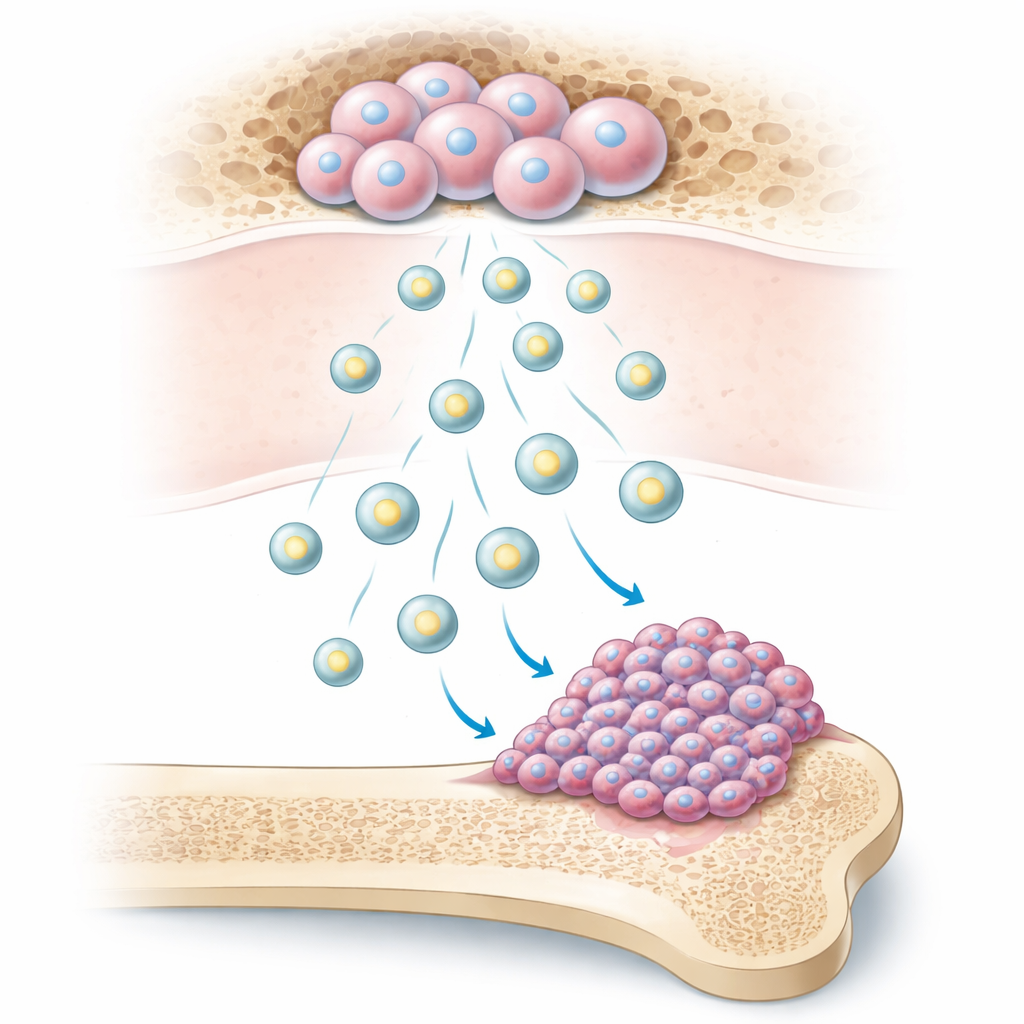
In unseren Knochen befinden sich mesenchymale Stammzellen des Knochenmarks, vielseitige Zellen, die den Knochen erhalten und reparieren. Diese Stammzellen geben winzige, membranumhüllte Bläschen ab, so genannte extrazelluläre Vesikel. Die Forschenden zeigen, dass Osteosarkomzellen diese Vesikel leicht aufnehmen. Sobald das geschieht, teilen sich die Krebszellen schneller, bilden mehr Kolonien, bewegen sich schneller über Oberflächen und dringen in In-vitro‑Tests leichter durch Barrieren. In Mäusen wuchsen Tumoren, die diesen Vesikeln ausgesetzt waren, größer und erzeugten mehr Lungenmetastasen, was darauf hinweist, dass diese mikroskopischen Pakete die Aggressivität des Tumors stark erhöhen.
Eine zirkuläre Botschaft, die den Krebs stärkt
Das Team untersuchte anschließend, welche genetischen Botschaften innerhalb der Vesikel die Osteosarkomzellen am stärksten veränderten. Sie konzentrierten sich auf zirkuläre RNAs, eine kürzlich entdeckte Klasse von RNA‑Molekülen, die geschlossene Schleifen bilden und ungewöhnlich stabil sind. Die Sequenzierung ergab einen herausragenden Kandidaten, genannt circRNA‑0010220, der in mit Stammzell‑Vesikeln behandelten Osteosarkomzellen und in Tumorproben von Patienten stark erhöht war. Wenn die Forschenden die circRNA‑0010220‑Spiegel in den Stammzellen reduzierten, verloren deren Vesikel einen großen Teil ihrer Fähigkeit, Krebszellwachstum, -bewegung und -invasion zu stimulieren — sowohl in kultivierten Zellen als auch in Mausmodellen. Damit wurde circRNA‑0010220 als Schlüsseltreiber der schädlichen Effekte identifiziert.
Eine epigenetische Bremse wird abgeschaltet
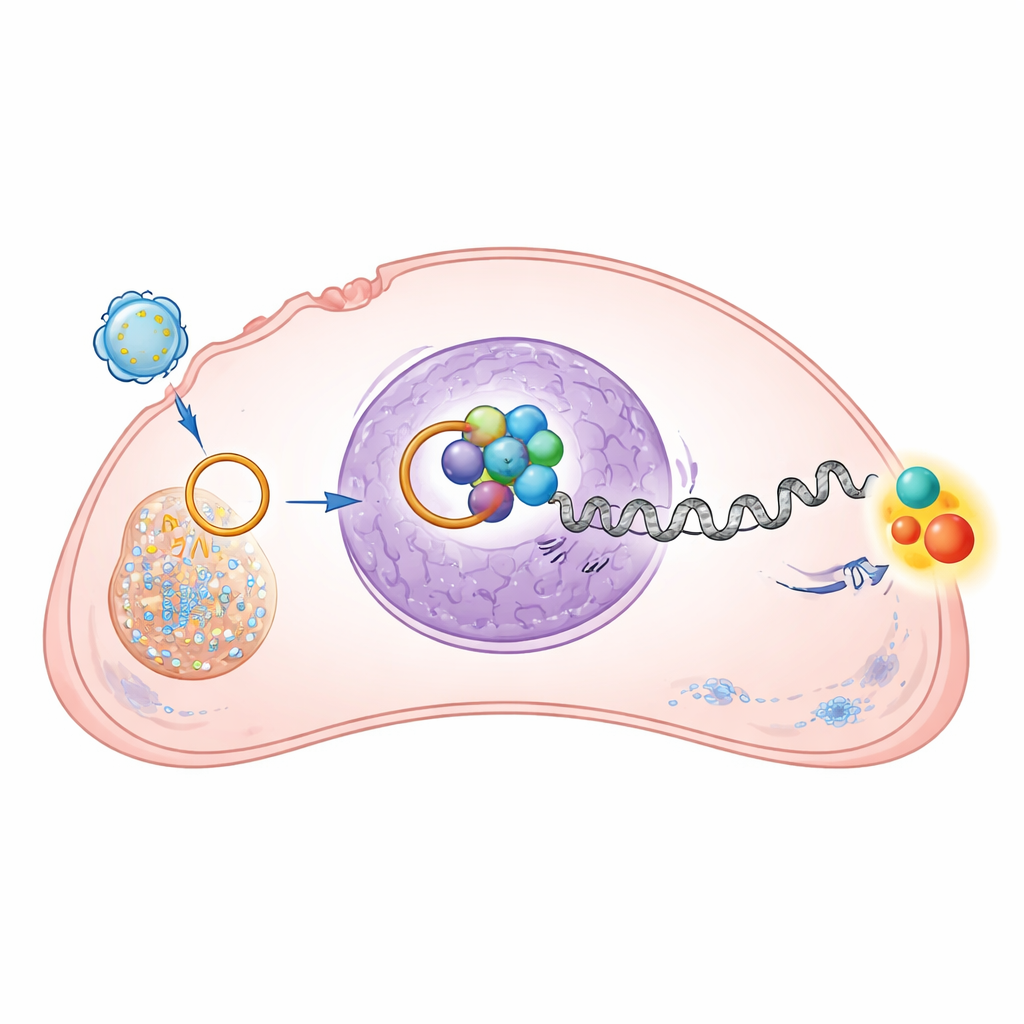
Bei genauerer Betrachtung kartierten die Forschenden, wie diese zirkuläre RNA das Verhalten der Krebszellen umprogrammiert. In Osteosarkomzellen gelangt circRNA‑0010220 in den Zellkern, das Kontrollzentrum der Zelle. Dort bindet sie an ein Protein namens EZH2, ein Enzym, das chemische Markierungen an Histonen anbringt — den spool‑artigen Proteinen, um die die DNA gewickelt ist. Zusammen führen circRNA‑0010220 und EZH2 zu einer Zunahme einer spezifischen Markierung, bekannt als H3K27me3, in der DNA‑Kontrollregion des Gens CTNNBIP1. Diese Modifikation verdichtet das Chromatin in diesem Bereich stark und schaltet das Gen effektiv aus. Da CTNNBIP1 normalerweise als Bremse auf einem kraftvollen wachstumsfördernden Signalweg wirkt, beseitigt seine Stilllegung eine wichtige Schutzvorrichtung gegen unkontrolliertes Krebsverhalten.
Aktivierung eines starken Wachstumswegs
CTNNBIP1 hemmt den Wnt/β‑Catenin‑Signalweg, ein bekanntes System, das bei Überaktivierung Zellen zur Teilung, Migration und zum Überleben anregt. Durch die Abschaltung von CTNNBIP1 erhöht circRNA‑0010220 indirekt die Konzentration und die nukleare Aktivität von β‑Catenin in Osteosarkomzellen. Die Studie zeigte, dass Gene, die von diesem Weg reguliert werden — verbunden mit Zellzyklusfortschritt, stammesähnlichen Eigenschaften und Invasion — stärker aktiv waren, wenn vesikelvermitteltes circRNA‑0010220 vorhanden war. Als die Forschenden ein Medikament einsetzten, das β‑Catenin spezifisch blockiert, wurden die pro‑Wachstums‑ und pro‑Migrations‑Effekte von circRNA‑0010220 weitgehend aufgehoben. Das bestätigt, dass die zirkuläre RNA über diesen Wachstumsweg wirkt, um das Tumorwachstum voranzutreiben.
Was das für künftige Therapien bedeutet
Insgesamt skizziert die Arbeit eine vollständige Ereigniskette: Knochenmark‑Stammzellen senden Vesikel mit circRNA‑0010220 an Osteosarkomzellen; die zirkuläre RNA geht im Zellkern eine Partnerschaft mit EZH2 ein, um CTNNBIP1 chemisch zu stilllegen; dies löst die Bremsen des Wnt/β‑Catenin‑Wegs und fördert dadurch schnelleres Tumorwachstum und Ausbreitung. Für Patientinnen und Patienten ergeben sich daraus mehrere neue therapeutische Ansätze. Das Unterbrechen des Vesikeltransfers, das Blockieren von circRNA‑0010220, das Stören ihrer Interaktion mit EZH2 oder das Abschwächen der β‑Catenin‑Signalgebung könnten jeweils helfen, die Progression des Osteosarkoms zu verlangsamen. Obwohl diese Ideen klinisch noch geprüft werden müssen, legt die Studie ein zuvor verborgenes Kommunikationsnetzwerk im knöchernen Tumorumfeld offen und hebt eine konkrete Reihe molekularer Ziele für künftige Wirkstoffe hervor.
Zitation: Pan, R., Pan, Y., Ruan, W. et al. BMSC-derived extracellular vesicles enhance osteosarcoma proliferation and metastasis via the circRNA-0010220/β-catenin pathway. Cell Death Dis 17, 376 (2026). https://doi.org/10.1038/s41419-026-08655-8
Schlüsselwörter: Osteosarkom, extrazelluläre Vesikel, zirkuläre RNA, Wnt β‑Catenin, epigenetische Regulation