Clear Sky Science · de
Verlust von DIAPH3 beschleunigt die Gliom-Entstehung bei Mäusen
Warum diese Hirnstudie wichtig ist
Glioblastom gehört zu den tödlichsten Hirntumoren, und trotz Operation, Bestrahlung und Chemotherapie überleben die meisten Patientinnen und Patienten kaum länger als ein Jahr. Diese Studie stellt eine grundlegende, aber entscheidende Frage: Welche frühen Veränderungen in Gehirnzellen treiben sie in Richtung solcher aggressiven Tumoren, und warum sind diese Tumoren so schwer mit Strahlung zu zerstören? Indem die Forschenden ein einzelnes Strukturprotein in Maus-Hirnzellen verfolgen, zeigen sie, wie dessen Verlust Chromosomen destabilisiert, das Auftreten von Tumoren beschleunigt und stammzellähnlichen Krebszellen ermöglicht, eine Strahlenbehandlung zu überstehen, die sie eigentlich vernichten sollte.
Ein zellulärer „Bauer“, der die Teilung in Schach hält
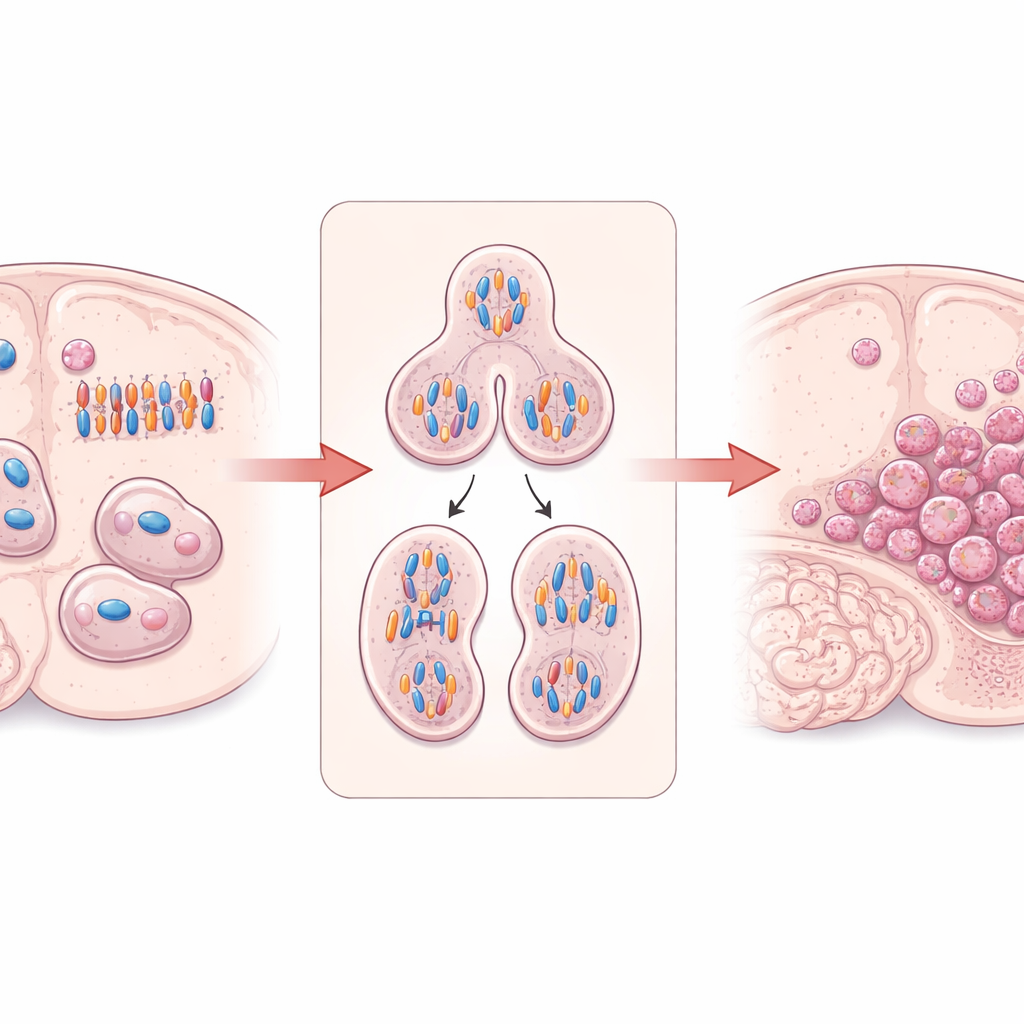
Die Arbeit fokussiert auf DIAPH3, ein Protein, das beim Aufbau und der Organisation des zellulären Innenrahmens aus Aktinfilamenten und Mikrotubuli hilft. In teilenden Hirnstammzellen ist DIAPH3 entscheidend für die Ausbildung einer funktionalen Spindel — der Struktur, die die duplizierten Chromosomen auseinanderzieht — und für das Abtrennen einer Zelle in zwei Tochterzellen. Frühere Forschungen zeigten, dass bei fehlendem DIAPH3 in sich entwickelnden Mausgehirnen teilende Zellen häufig Chromosomen fehlerhaft handhaben, was zu abnormalen Chromosomenzahlen (Aneuploidie), gestoppten Zellzyklen und Zelltod führt. Auffällig ist, dass ein kleiner Abschnitt auf humanem Chromosom 13, der das DIAPH3-Gen enthält, bei Glioblastomen häufig deletiert ist, und höhere DIAPH3-Werte in einigen Patientengruppen mit besserem Überleben verknüpft wurden — ein Hinweis darauf, dass dieses Protein im Gehirn als Tumorsuppressor wirken könnte.
Mausgehirne so verändern, dass Tumoren wachsen
Um zu testen, ob der Verlust von DIAPH3 tatsächlich Hirnkrebs fördert, erzeugte das Team Mäuse, bei denen zwei Gene selektiv in cortexbildenden Stammzellen gelöscht werden konnten: Diaph3 und Trp53, letztere kodiert für den bekannten Wächter des Genoms, p53. Mäuse, denen nur Diaph3 in diesem Bereich fehlte, entwickelten selbst nach zwei Jahren keine Tumoren, was darauf hindeutet, dass p53 weiterhin hochgradig abnorme Zellen eliminieren kann. Im Gegensatz dazu bildeten Mäuse, denen nur Trp53 oder sowohl Trp53 als auch Diaph3 fehlten, schließlich diffus-wachsende hochgradige Gliome, die unter dem Mikroskop dem menschlichen Krankheitsbild sehr ähnelten. Mithilfe wiederholter Ultra-Hochfeld-MRT-Aufnahmen zeigten die Forschenden, dass Tiere ohne beide Gene früher nachweisbare Tumoren entwickelten und bis zur Lebensmitte häufiger große Gliome, besonders in den Riechkolben, aufwiesen als Mäuse ohne nur Trp53. Die Tumorwachstumsrate war, einmal begonnen, in beiden Gruppen ähnlich — verändert hat sich vor allem der Zeitpunkt, zu dem Tumoren erstmals auftraten.
Chromosomales Chaos und umgeschaltete Genaktivität
Um zu ergründen, warum der Verlust von DIAPH3 das Tumorauftreten beschleunigt, untersuchten die Forschenden die Genaktivität in den Riechkolben junger Mäuse, bevor Tumoren sichtbar waren. In Tieren ohne sowohl Diaph3 als auch Trp53 wurden 126 Gene anders exprimiert im Vergleich zu Nur-Trp53-Mutanten, und fast die Hälfte dieser Gene hatte bereits zuvor Verbindungen zum Krebs gezeigt. Viele Veränderungen gruppierten sich in Signalwegen, die Zellwachstum, Migration und Gefäßbildung antreiben, darunter VEGF-, MAPK-, RAS-, Rap1- und cAMP-Signalisierung sowie G‑Protein‑gekoppelte Rezeptornetzwerke. Diese veränderte molekulare Landschaft deutete darauf hin, dass Zellen früher in einen krebsähnlichen Zustand gedrängt werden. Die Kopienzahl-Analyse ganzer Genome von voll entwickelten Tumoren zeigte, dass DIAPH3-Mangel nicht stark die kleinen, fokalen DNA-Veränderungen erhöhte, sondern vielmehr großflächige Gewinne und Verluste ganzer Chromosomen förderte — genau die Aneuploidie, die man bei fehlerhafter Chromosomensegregation erwarten würde.
Eingebauter DNA-Schaden und robustere Tumorstammzellen
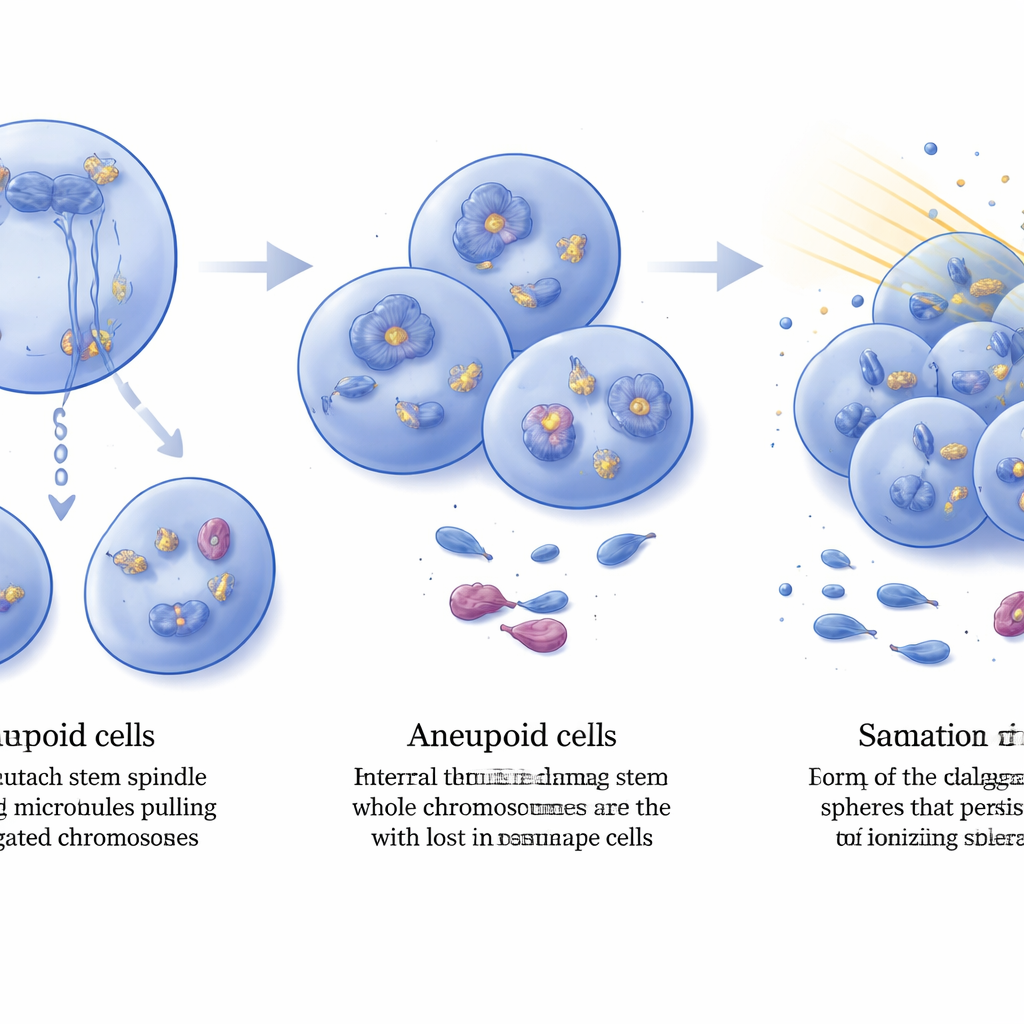
Aneuploidie-tragende Tumorzellen wiesen mehr intrinsischen DNA-Schaden auf, nachgewiesen durch erhöhte Werte des DNA-Bruch-Markers γ‑H2AX, der über Zellkerne verteilt war. Dennoch wuchsen diese Tumoren weiter, was darauf hindeutet, dass sie Wege entwickelt hatten, solchen Stress zu tolerieren. Beim Vergleich der Genexpression in etablierten Tumoren fanden die Forschenden Hunderte von durch DIAPH3-Verlust veränderten Genen, darunter eine auffällige Amplifikation und Überproduktion des Wachstumsfaktor-Rezeptors FGFR2 in vielen Doppelmutanten-Tumoren. FGFR2 ist bekannt dafür, die DNA-Reparaturmechanismen in Glioblastomzellen zu stärken, und seine Aktivierung wurde mit Strahlenresistenz in Verbindung gebracht. Das Team isolierte gliom-stammzellähnliche Zellen aus Maus-Tumoren und testete deren Reaktion auf eine klinisch relevante Dosis ionisierender Strahlung. Vor der Behandlung war die Häufigkeit stammzellähnlicher Zellen in beiden Genotypen ähnlich, doch nach der Bestrahlung behielten Kulturen aus DIAPH3‑defizienten Tumoren etwa doppelt so viele aktive stammzellähnliche Zellen wie jene aus Nur‑Trp53-Tumoren — ein Hinweis auf erhöhte Radioresistenz.
Was das für Hirnkrebs bedeutet
In der Summe zeichnet die Studie DIAPH3 als eine Art Wächter, der Hirnstammzellen hilft, mit der richtigen Chromosomenzahl zu teilen. Fehlen sowohl DIAPH3 als auch p53, wird die Zellteilung fehleranfällig, ganze Chromosomen gehen verloren oder werden gewonnen, und DNA-Schäden häufen sich an. Anstatt zu sterben, passen sich einige Zellen an, indem sie reparaturverknüpfte Faktoren wie FGFR2 amplifizieren, und verwandeln sich in aneuploide, hochgradige Gliome, deren stammzellähnliche Zellen ungewöhnlich strahlenresistent sind. Auch wenn Mausmodelle nicht jedes Merkmal des menschlichen Glioblastoms abbilden, stützen diese Befunde die Idee, dass DIAPH3 sowohl als potenzieller Prognosemarker als auch als zentraler Knotenpunkt in den Prozessen fungiert, die Tumorinitiation, Genomstabilität und Therapierespons steuern — und damit neue Ansätze eröffnen könnten, um diesen verheerenden Hirnkrebs empfindlicher für vorhandene Behandlungen zu machen.
Zitation: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Schlüsselwörter: Glioblastom, chromosomale Instabilität, stammzellartige Hirntumorzellen, Strahlenresistenz, Tumorsuppressorgene