Clear Sky Science · de
Glioblastomzellen, die dem durch Chemo- und Strahlentherapie ausgelösten Zelltod entgehen, zeigen ein zweigleisiges glycolytisches Programm
Warum diese Studie zu Hirntumoren wichtig ist
Das Glioblastom ist einer der tödlichsten Hirntumoren bei Erwachsenen und wächst nach Operation, Chemotherapie und Bestrahlung fast immer wieder nach. Diese Studie stellt eine zentrale Frage: Was ist besonders an der kleinen Gruppe von Tumorzellen, die die Behandlung überleben und später die Erkrankung erneut entfachen? Indem die Forschenden über die Zeit verfolgen, wie diese Zellen Zucker verarbeiten, legen sie eine verborgene Überlebensstrategie offen, die erklären könnte, warum aktuelle Therapien so häufig versagen — und schlagen neue Wege vor, die lebenswichtige Energiezufuhr des Tumors abzuschneiden.
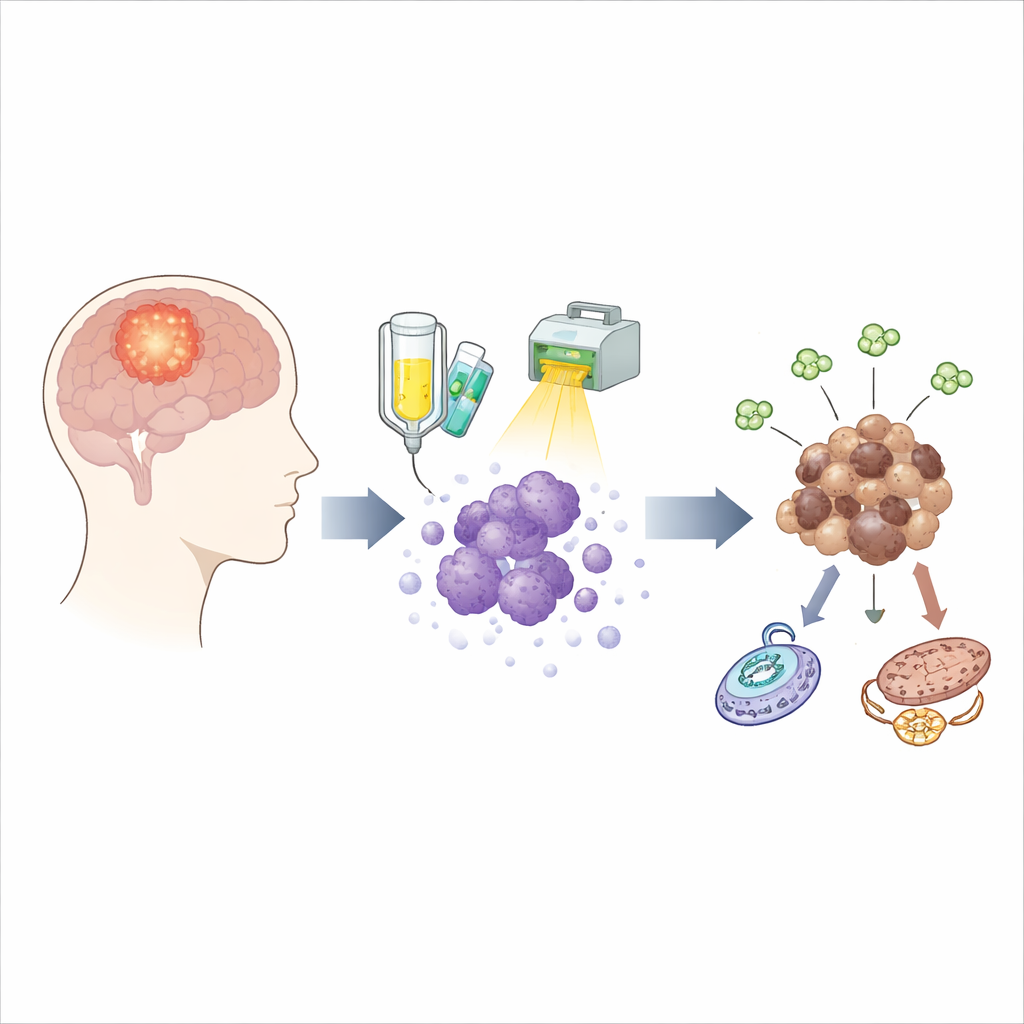
Die verborgenen Überlebenden nach der Behandlung
Die Standardbehandlung für Glioblastom kombiniert ein Medikament namens Temozolomid mit Bestrahlung. Während diese Kombination den Großteil der Tumorzellen abtötet, überlebt eine hartnäckige Minderheit und kann Monate später einen neuen Tumor bilden. Um diese Überlebenden in Aktion zu erwischen, verwendete das Team Tumorzellen, die direkt von zehn verschiedenen Patientinnen und Patienten stammten, und setzte sie einem Behandlungsplan aus, der dem klinischen Ablauf eng nachempfunden ist. Sie entnahmen lebende Zellen zu mehreren Zeitpunkten während und nach der Therapie und untersuchten außerdem übereinstimmende Tumoren, die in Mäusen herangezogen wurden, sodass sie verfolgen konnten, wie sich die Überlebenden im Zeitverlauf verändern, anstatt nur Tumoren vor und nach dem Rückfall zu vergleichen.
Wie Tumorzellen den Umgang mit Zucker verändern
Gehirngewebe verbraucht einen bemerkenswert großen Anteil des körpereigenen Zuckers, und Glioblastomzellen sind besonders hungrig danach. Die Forschenden fanden heraus, dass die überlebenden Zellen im Verlauf der Behandlung noch mehr Glukose aus ihrer Umgebung aufnehmen. In einer Wendung verbrannten sie diese zusätzliche Energie jedoch nicht einfach schneller. Stattdessen reduzierten diese Zellen ihre Produktion von Laktat, dem typischen Abfallprodukt schneller Zuckerzersetzung bei Krebs. Messungen zentraler Proteine zeigten ein markantes gespaltenes Muster: Komponenten, die Zucker in die Zelle bringen und den Abbau einleiten, wurden hochreguliert, während solche, die die späteren Schritte übernehmen und Laktat produzieren, zurückgingen. Dieses „zweigleisige“ Programm bedeutet, dass Zucker aufgenommen und begonnen wird zu verarbeiten, der übliche Ausweg über die Laktatbildung jedoch teilweise blockiert ist.
Umlenkung von Brennstoff in Bausteine und Energiezentralen
Wohin fließt der umgeleitete Zucker? Mithilfe speziell markierter Glukose und fortschrittlicher Metabolitmessungen zeigte das Team, dass überlebende Zellen einen Großteil dieses Kohlenstoffs in zwei Hauptziele lenken. Das eine ist eine Nebenstrecke, der Pentosephosphatweg, der die Rohmaterialien zur Herstellung von DNA- und RNA-Bausteinen bereitstellt. In diesen Zellen waren viele Nukleotidbestandteile und zugehörige Gene verstärkt, was auf eine starke Ausrichtung auf Reparatur und Vorbereitung für erneutes Wachstum hindeutet. Das zweite Ziel sind die Kraftwerke der Zelle, die Mitochondrien. Enzyme des mitochondrialen Energiestoffwechsels nahmen zu, und frühere Arbeiten derselben Gruppe zeigten eine stärkere Einfuhr von zuckerbasiertem Brennstoff in diese Strukturen. Zusammen ergibt das ein koordiniertes Umbauprogramm: weniger verschwenderische Fermentation zu Laktat, mehr Investition in Reparatur, Wachstumsbausteine und flexible Energieerzeugung.
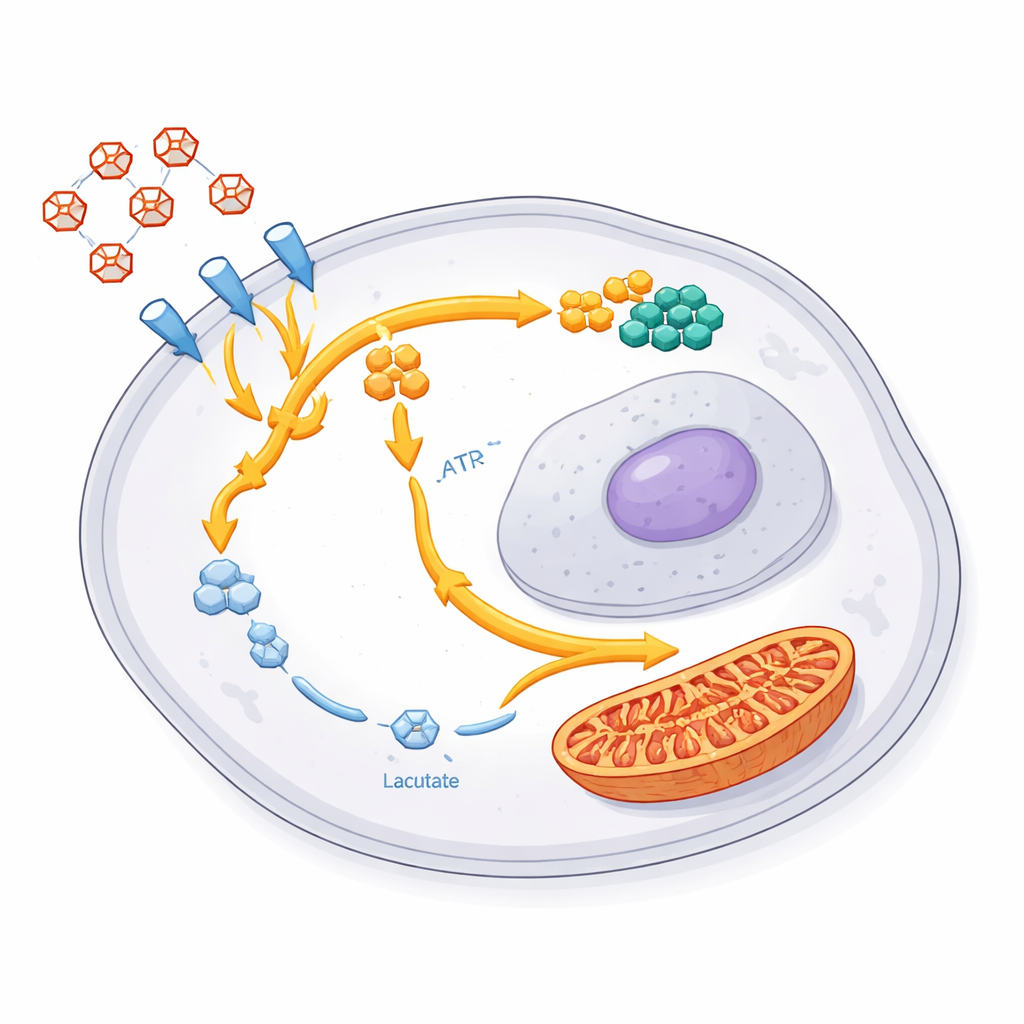
Ein gemeinsames Überlebenshandbuch über Tumoren und Tiere hinweg
Glioblastomtumoren unterscheiden sich stark von Patient zu Patient, was standardisierte Therapien oft scheitern lässt. Trotz dieser Vielfalt zeigte jedes der zehn patientenabgeleiteten Modelle dieselbe grundlegende Verschiebung nach Chemo- und Strahlentherapie: erhöhte frühe Schritte der Zuckerverarbeitung, verringerte späte Schritte und Laktatausstoß sowie erhöhte mitochondriale Aktivität. Wichtig ist, dass dieselbe Signatur in in Mäusen herangezüchteten Gehirntumoren aus Patientenstammzellen auftauchte, die mit angepassten Versionen der Standardtherapie behandelt wurden. Rezidivierende Tumoren in diesen Tieren trugen weiterhin das veränderte Zuckerprogramm, was darauf hinweist, dass es sich nicht um einen kurzlebigen Effekt, sondern um ein stabiles Merkmal der Zellen handelt, die die Behandlung überdauern und den Krebs wiederaufbauen können.
Was das für zukünftige Behandlungen bedeutet
Für Laien ist die zentrale Botschaft, dass überlebende Glioblastomzellen sich nicht einfach vor der Behandlung „verstecken“; sie verdrahten aktiv um, wie sie Zucker nutzen, um am Leben zu bleiben. Sie nehmen mehr Glukose auf, vermeiden es, sie zu Abfall zu verarbeiten, und lenken sie stattdessen in die Herstellung von DNA-Bausteinen und in die Versorgung der Mitochondrien — wodurch sie Schäden reparieren, einen flexiblen, stammazellähnlichen Zustand aufrechterhalten und schließlich den Tumor wieder wachsen lassen können. Indem die Studie diesen gemeinsamen metabolischen Überlebenszustand offenlegt, liefert sie neue therapeutische Ideen: Die gezielte Blockade der frühen Schritte der Zuckerverarbeitung, des DNA-Baustein-Zweigs oder der mitochondrialen Abhängigkeit dieser Zellen könnte die Standard-Chemoradiotherapie vervollständigen und weniger Überlebende zurücklassen, die die Erkrankung neu entfachen.
Zitation: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Schlüsselwörter: Glioblastom, Krebsstoffwechsel, Glukoseverwertung, Therapieresistenz, Pentosephosphatweg