Clear Sky Science · de
Von CAFs stammendes LAM332 fördert die Bildung und das Überleben von CTCs über ITGA3 und trägt zur Metastasierung des duktalen Adenokarzinoms des Pankreas bei
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Pankreaskrebs ist berüchtigt dafür, früh und still zu streuen, sodass Betroffene oft nur wenige Behandlungsmöglichkeiten haben, wenn die Krankheit entdeckt wird. Diese Studie untersucht einen der gefährlichsten Schritte dieses Prozesses: wie Krebszellen sich vom Primärtumor lösen, im Blut überleben und in Organen wie Leber und Lunge neue Tumoren begründen. Indem die Autorinnen und Autoren eine spezifische „Kommunikation“ zwischen Tumorzellen und ihren umgebenden Stützzellen aufdecken, zeigen sie neue Ansätze zur Vorhersage und potenziellen Blockade tödlicher Metastasen auf.
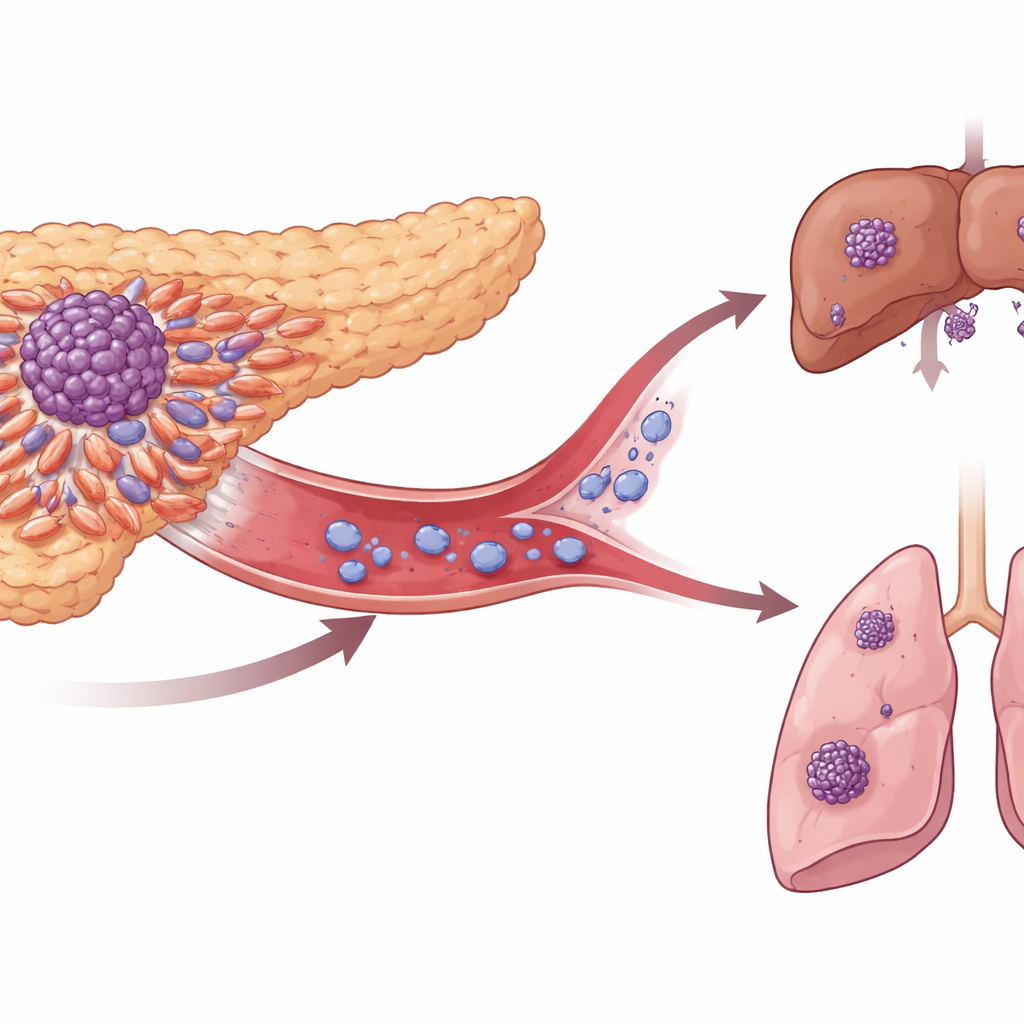
Verborgene Reisende im Blut
Wenn Pankreastumoren streuen, geschieht dies über zirkulierende Tumorzellen – abtrünnige Zellen, die ins Blut entweichen. Das Team untersuchte Tumorproben sowie umfangreiche Gen- und Proteindaten von Patientinnen und Patienten mit und ohne solche Zellen in ihren Gefäßen und von Personen mit lokal begrenzter versus metastasierter Erkrankung. Immer wieder fiel ein Oberflächenmolekül namens ITGA3 besonders auf. Tumoren und zirkulierende Zellen mit höherer ITGA3-Expression waren bei fortgeschritteneren Tumoren häufiger, besonders am invasiven Rand des Tumors, wo Zellen sich zuerst ablösen. Patientinnen und Patienten, deren Tumoren mehr ITGA3 aufwiesen, hatten tendenziell mehr zirkulierende Tumorzellen, aggressivere Merkmale wie Einwachsen in umliegendes Gewebe und Blutgefäße sowie eine kürzere Überlebenszeit.
Wie Tumorzellen die Fähigkeit zum Ablösen erlangen
Um zu verstehen, was ITGA3 tatsächlich bewirkt, veränderten die Forschenden dessen Expression in Pankreaskrebszelllinien und setzten diese Zellen in Mäuse ein. Bei verminderter ITGA3-Wirkung wuchsen die Krebszellen langsamer, bewegten sich weniger und waren weniger in der Lage, umliegendes Gewebe zu durchdringen. Die Zellen kehrten zudem eher in einen geordneten, „epithelialen“ Zustand zurück, gewannen enge Zell‑zu‑Zell-Kontakte zurück und verloren die flexiblen, wanderungsfähigen Eigenschaften, die ihnen das Entkommen erleichtern. In Mäusen waren Tumoren ohne ITGA3 kleiner und zeigten weniger invasive Merkmale. Diese Befunde deuten darauf hin, dass ITGA3 als Schalter wirkt, der Tumorzellen hilft, sich vom Tumorverband zu lösen, in Blutgefäße einzudringen und ihre Reise als zirkulierende Tumorzellen zu beginnen.
Zusammenklumpen, um die Reise zu überstehen
Das Leben im Blut ist für einzelne Krebszellen hart, aber Zellcluster scheinen deutlich besser zu überleben und Metastasen zu bilden. Die Studie zeigte, dass ITGA3 besonders reichlich auf Zellen in solchen Clustern vorkommt. In Laborversuchen, die verhindern sollten, dass Zellen am Plastik haften, bildeten Krebszellen mit normaler ITGA3-Expression bereitwillig dichte Cluster und widerstanden dem Zelltod, während Zellen ohne ITGA3 überwiegend isoliert blieben und leichter abstben. In Mausmodellen mit Tumoren in der Bauchspeicheldrüse führte der Verlust von ITGA3 zu weniger zirkulierenden Clustern, weniger metastatischen Herden in Leber und Lunge und einer geringeren Gesamtlast an Fernmetastasen. Das zeigt, dass ITGA3 nicht nur beim Ablösen hilft, sondern auch beim Zusammenkleben der Zellen und darin, den widrigen Bedingungen im Blut zu trotzen.
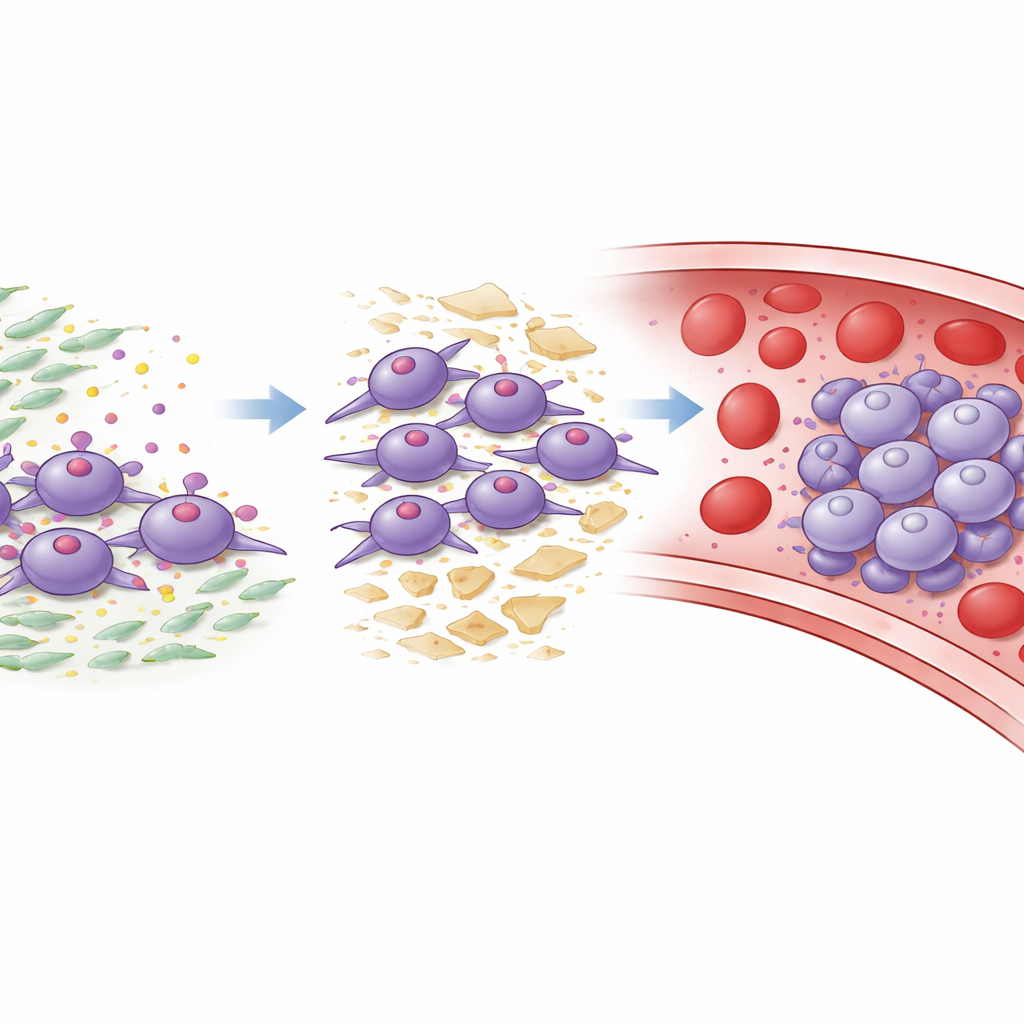
Die Rolle der unterstützenden Stromazellen
Pankreastumoren sind reich an krebsassoziierten Fibroblasten, einer Art Stützzellen, die das Gewebegerüst um den Tumor aufbauen und umgestalten. Die Autorinnen und Autoren fanden heraus, dass diese Fibroblasten eine Hauptquelle eines klebrigen Proteins namens Laminin‑332 sind. Tumorzellen mit ITGA3 nutzen dieses Protein als Andockstelle für Laminin‑332. In Zell‑ und Tierexperimenten löste die Bindung von Laminin‑332 an ITGA3 Signale in den Tumorzellen aus, die Wachstum, Bewegung, Gewebeinvasion und die Umstellung in einen beweglicheren, aggressiveren Zustand förderten. Außerdem begünstigte sie das Clusterbilden und verringerte den Zelltod, wenn Zellen in Suspension waren, was die Bedingungen im Blut nachahmt. Das Blockieren von Laminin‑332 mit Antikörpern oder das Eingreifen in ITGA3 oder seine nachgeschalteten Signalpartner kehrte diese malignen Eigenschaften größtenteils um und reduzierte Metastasen in Mäusen.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeichnet die Arbeit eine klare Abfolge von Ereignissen nach: Fibroblasten in und um Pankreastumoren setzen Laminin‑332 frei; dieses Protein bindet an ITGA3 auf Tumorzellen; das folgende Signal hilft den Zellen, sich zu lösen, sich zu schützendem Cluster‑Verhalten zusammenzuklümpen, im Kreislauf zu überleben und entfernte Organe zu kolonisieren. Für Laien ist die Kernbotschaft, dass die Forschenden eine spezifische „Versorgungsleitung“ kartiert haben, die Tumoren nutzen, um ihre streuenden Zellen zu starten und zu schützen. Weil dieser Weg von Komponenten abhängt, die vornehmlich im Tumor und seinem Stroma vorkommen, bietet er ein attraktives Ziel für neue Therapien. Wirkstoffe oder Antikörper, die Laminin‑332, ITGA3 oder die von ihnen ausgelösten Signale blockieren, könnten helfen, die Anzahl und Belastbarkeit zirkulierender Tumorzellen zu reduzieren und so das Fortschreiten oder die Entstehung tödlicher Metastasen beim Pankreaskrebs zu verlangsamen oder zu verhindern.
Zitation: Tang, H., Shi, W., Tan, S. et al. CAFs-derived LAM332 promotes CTCs formation and survival via ITGA3 and contributes to the metastasis of pancreatic ductal adenocarcinoma. Cell Death Dis 17, 369 (2026). https://doi.org/10.1038/s41419-026-08642-z
Schlüsselwörter: Pankreaskrebs, Metastase, zirkulierende Tumorzellen, Tumormikroumgebung, krebsassoziierte Fibroblasten