Clear Sky Science · de
Die HNF4α-HKDC1-Achse orchestriert ein metabolisches Umlernen, um Migration und Metastasen bei fortgeschrittenem Magenkrebs zu fördern
Warum das für Patienten wichtig ist
Die meisten Todesfälle durch Magenkrebs treten nicht wegen des ursprünglichen Tumors auf, sondern weil Krebszellen in entfernte Körperregionen wandern und dort Wurzeln schlagen. Diese Arbeit enthüllt einen verborgenen molekularen „Ein‑/Ausschalter“, der Magenkrebszellen dabei hilft, ihre Energieverwertung umzustellen und mobiler zu werden. Noch wichtiger: Sie verweist auf ein bereits von der FDA zugelassenes Medikament, das möglicherweise umgenutzt werden kann, um diesen Schalter auszuschalten und das Fortschreiten oder die Ausbreitung zu verlangsamen oder zu verhindern.
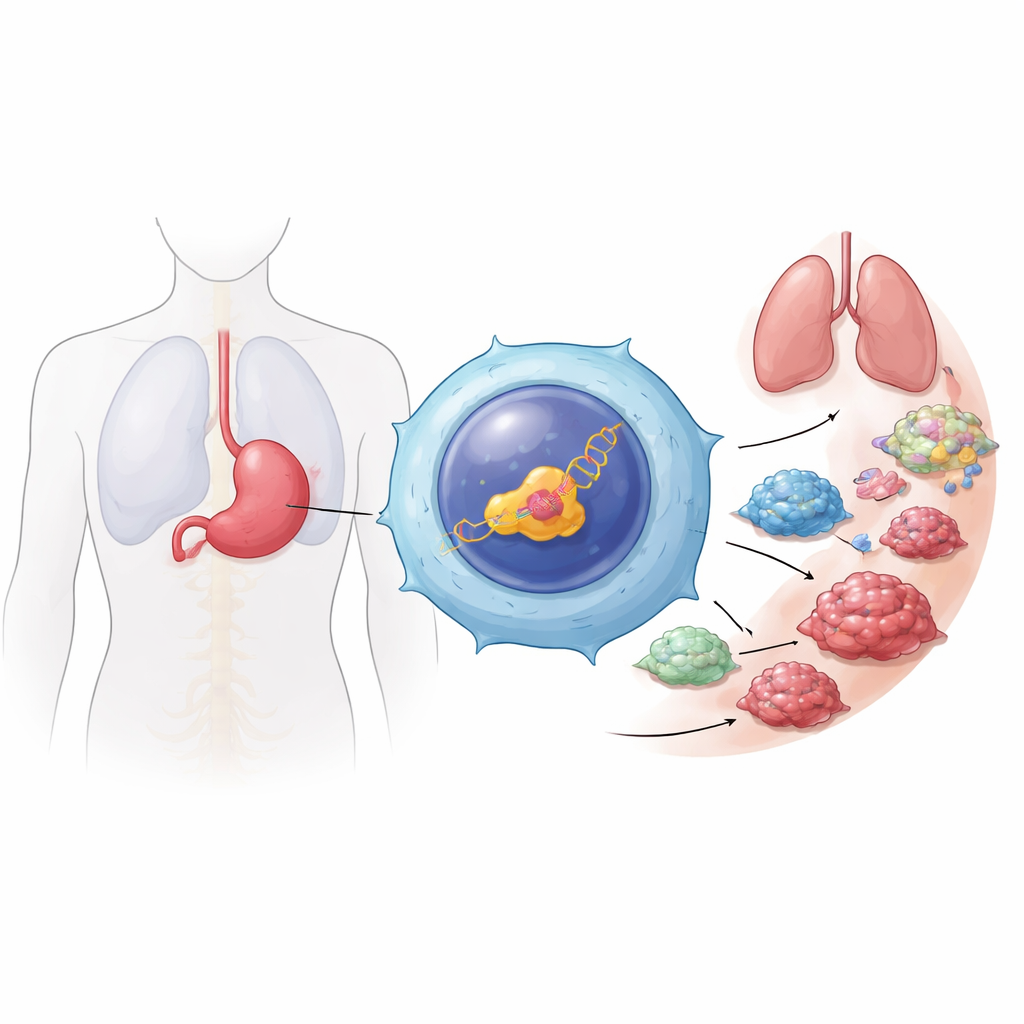
Eine gefährliche Verschiebung beim Magenkrebs
Magenkrebs ist weltweit die fünfthäufigste Krebserkrankung und wird oft spät entdeckt, nachdem er sich bereits ausgebreitet hat. Die Autoren konzentrierten sich auf die Metastasierung — den Schritt, in dem Tumorzellen sich ablösen, durch die Bauchhöhle oder den Blutkreislauf wandern und neue Orte besiedeln. Durch Auswertung großer öffentlicher Krebsdatenbanken und Untersuchung von Gewebeproben von Patientinnen und Patienten fanden sie, dass eine spezifische Variante des Genregulators HNF4α, angetrieben durch seinen P2‑Promotor (P2‑HNF4α), in fernliegenden Metastasen deutlich häufiger vorkommt als im Primärtumor und im benachbarten nicht‑tumorösen Gewebe. Diese Variante wurde hauptsächlich innerhalb der Tumorzellen und nicht in den umliegenden normalen Zellen gefunden, was darauf hindeutet, dass sie eng mit dem invasiven Verhalten des Tumors verknüpft ist.
Ein Hauptschalter, der Zellbewegung verstärkt
Um Ursache und Wirkung zu prüfen, veränderten die Forschenden die P2‑HNF4α‑Spiegel in einer Reihe menschlicher Magenkrebszelllinien, die die wichtigsten molekularen Subtypen der Erkrankung repräsentieren. Reduzierten sie HNF4α in Zellen, die es normalerweise exprimieren, sank die Fähigkeit der Zellen, durch künstliche Membranen zu migrieren und zu invasieren oder Wunden in Kultur zu verschließen, deutlich. Erzeugten sie in Zellen mit niedrigem HNF4α‑Spiegel eine repräsentative P2‑HNF4α‑Isoform, wurden diese Zellen merklich mobiler und invasiver — auch in dreidimensionalen Sphäroid‑Assays, die echte Tumoren nachahmen. In Mäusen bildeten Zellen, die P2‑HNF4α überexprimierten, deutlich mehr metastatische Knötchen in der Bauchhöhle, was zeigt, dass dieser Faktor die Ausbreitung in lebenden Organismen aktiv vorantreibt.
Ausbreitung antreiben durch Umlenken der Energieverwertung
Krebszellen verändern häufig ihre Nährstoffverarbeitung, um Wachstum und Bewegung zu unterstützen. Mithilfe kombinierter RNA‑Sequenzierung und Metabolitprofilierung entdeckte das Team, dass das Herunterregeln von HNF4α einen zentralen energieerzeugenden Pfad dämpft: die Glykolyse, also den Abbau von Glukose. Die Mengen mehrerer glykolytischer Enzyme und ihrer Zwischenprodukte sanken ebenso wie Kennzahlen der Energieproduktion wie Sauerstoffverbrauch, Säurebildung und ATP‑Erzeugung. Weitere Analysen hoben ein Enzym, HKDC1, als am stärksten und konsistentesten mit HNF4α verknüpft hervor. HKDC1 liegt am allerersten Schritt der Glukoseverarbeitung und lenkt Zucker sowohl in die Laktatproduktion als auch in die mitochondriale Atmung — zwei Outputs, die zusammen Energie bereitstellen und ein chemisches Umfeld schaffen, das Zellbewegung begünstigt.
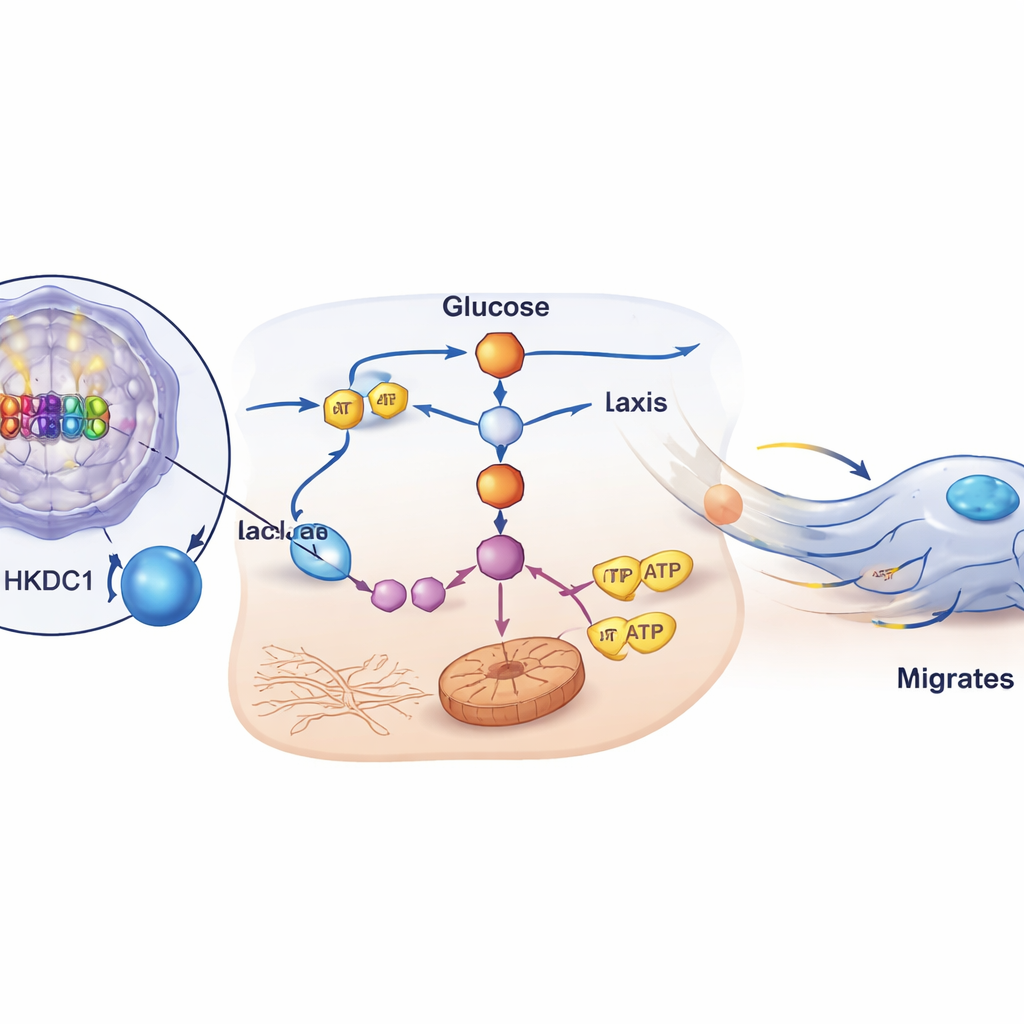
Eine direkte molekulare Verbindung und ein zentraler Komplize
Die Forschenden zeigten, dass P2‑HNF4α nicht nur mit HKDC1 korreliert, sondern dieses Gen direkt aktiviert. Mithilfe genomweiter Bindungsdaten, DNA‑Reporterassays und Protein‑DNA‑Bindungstests kartierten sie spezifische Stellen in einer Enhancer‑Region des HKDC1‑Gens, an denen HNF4α sitzt und die Transkription anregt. Wurde HKDC1 in Zellen reduziert, brach deren Fähigkeit zu migrieren und Peritonealmetastasen in Mäusen zu bilden drastisch ein, obwohl ihr kurzzeitiges Überleben nicht betroffen war. Entscheidend: Die Wiederherstellung von HKDC1 in Zellen mit herunterreguliertem HNF4α rettete die glykolytische Aktivität, Energieproduktion und das Migrationsverhalten; auch das Ergänzen von Stoffwechselendprodukten wie Laktat oder α‑Ketoglutarat stellte die Beweglichkeit wieder her. Zusammengenommen deuten diese Ergebnisse darauf hin, dass HKDC1 ein zentraler downstream‑Förderer ist, durch den P2‑HNF4α den Stoffwechsel umprogrammiert, um Metastasen anzutreiben.
Den Schalter mit einem vorhandenen Medikament ausschalten
Da HNF4α zu einer Familie von Proteinen gehört, die häufig pharmakologische Ziele sind, prüfte das Team, ob ein zugelassenes Medikament diese pro‑metastatische Achse blockieren könnte. Zuvor hatten sie Mycophenolsäure, die aktive Form des Transplantationsarzneimittels Mycophenolat‑Mofetil (MMF), als HNF4α‑Antagonisten in der Lungenkrebsforschung identifiziert. Hier reduzierte MMF die HKDC1‑Spiegel und die Zellmigration in Magenkrebszelllinien mit hoher HNF4α‑Expression, hatte jedoch kaum Einfluss in Zellen mit niedrigem HNF4α. In Mäusemodellen schränkte MMF die abdominalen Metastasen deutlich ein und senkte die HKDC1‑Expression — aber nur, wenn Tumoren hohe P2‑HNF4α‑Spiegel aufwiesen. Dies legt nahe, dass HNF4α sowohl als therapeutisches Ziel als auch als Biomarker dienen könnte, um Patientinnen und Patienten auszuwählen, die am ehesten von MMF‑basierten Strategien profitieren.
Was das für die zukünftige Versorgung bedeutet
Einfach gesagt identifiziert diese Studie ein molekulares Treibstoff‑Kontrollsystem — P2‑HNF4α, das über HKDC1 wirkt — das Magenkrebszellen dabei hilft, ihre Energiemaschinerie hochzufahren und besser metastasieren zu können. Indem gezeigt wird, dass ein vorhandenes Medikament dieses System stören und in präklinischen Modellen die Metastasierung reduzieren kann, eröffnet die Arbeit einen realistischen Weg zu neuen Behandlungsansätzen für fortgeschrittenen Magenkrebs. Bestätigen künftige klinische Studien diese Befunde, könnte die Untersuchung von Tumoren auf HNF4α‑Aktivität helfen, den Einsatz von MMF oder verwandten Wirkstoffen zur Verlangsamung oder Verhinderung der tödlichen Ausbreitung dieser Erkrankung zu steuern.
Zitation: Xu, X., Wu, H., Shang, J. et al. HNF4α-HKDC1 axis orchestrates a metabolic rewiring to promote migration and metastasis in advanced gastric cancer. Cell Death Dis 17, 347 (2026). https://doi.org/10.1038/s41419-026-08627-y
Schlüsselwörter: Magenkrebs-Metastasen, HNF4A, HKDC1, Krebsstoffwechsel, Mycophenolat-Mofetil