Clear Sky Science · de
Die DAG/PKC/CREB1/TGF-β1-Achse treibt die Steifigkeit bei Shear-Wave-Elastographie und das maligne Fortschreiten im triple-negativen Mammakarzinom über Umprogrammierung des Lipidstoffwechsels
Warum Tumorsteifigkeit wichtig ist
Ärztinnen und Ärzte haben schon lange beobachtet, dass sich manche Brusttumoren härter anfühlen als andere und dass diese Steifigkeit häufig auf ein aggressiveres Krebsverhalten hindeutet. Beim triple-negativen Mammakarzinom, einer aggressiven Form, die keine gängigen Angriffspunkte für Medikamente bietet, scheint Adipositas Tumoren zu verhärten und die Wahrscheinlichkeit für Streuung zu erhöhen. Diese Studie erklärt, wie Veränderungen im Fettstoffwechsel bei adipösen Patientinnen Tumoren versteifen, und zeigt, dass eine spezialisierte Ultraschalltechnik, die Shear-Wave-Elastographie, diese Steifigkeit extern ablesen kann und damit Einblicke in das Tumorverhalten liefert.
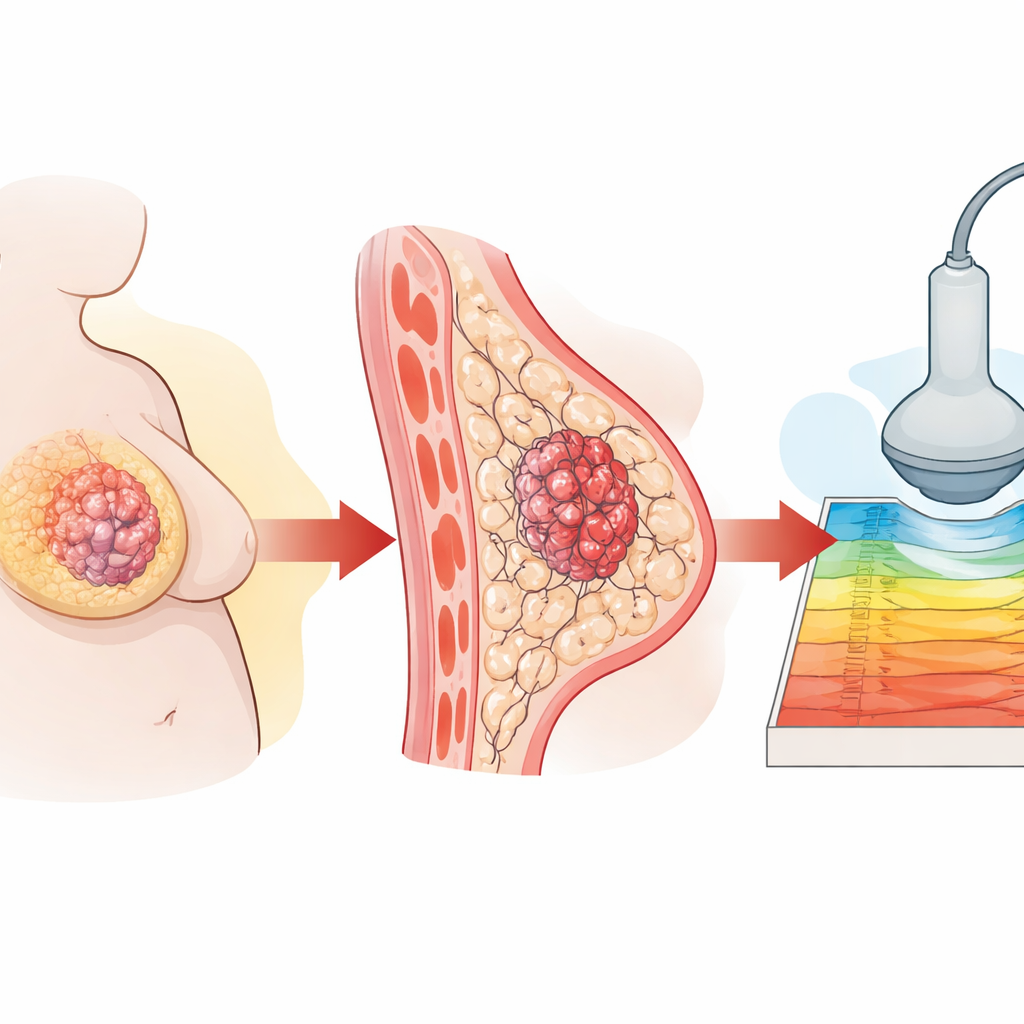
Körpergewicht und Tumorrisiko
Die Forschenden begannen mit der Nachverfolgung von 147 Frauen mit triple-negativem Mammakarzinom an einem großen Krebszentrum in Shanghai. Sie stellten fest, dass Frauen mit einem höheren Body‑Mass‑Index (BMI) schlechtere Langzeitergebnisse hatten, darunter mehr Rückfälle und Todesfälle. Bei der Auswertung von Ultraschallbildern zeigten Tumoren bei schwereren Patientinnen durchgehend höhere Steifigkeitswerte in der Shear‑Wave‑Elastographie, obwohl die konventionellen Grauwert‑Ultraschallaufnahmen ähnlich wirkten. Gewebeproben bestätigten, dass Tumoren aus adipösen Patientinnen mehr Kollagen und mehr aktiv teilende Zellen enthielten, beides Anzeichen für ein feindlicheres Tumorumfeld.
Von der Ernährung zu härteren Tumoren
Um Ursache und Wirkung zu untersuchen, verwendete das Team Mausmodelle und fütterte einige Tiere mit einer fettreichen, andere mit einer normalen Diät, bevor triple‑negative Brusttumoren implantiert wurden. Mäuse mit Fettreicher Ernährung nahmen mehr Gewicht zu, entwickelten größere Tumoren und zeigten vor allem einen über die Zeit ansteigenden Steifigkeitswert in der Shear‑Wave‑Elastographie. Die mikroskopische Untersuchung zeigte dichtere Kollagennetze, vermehrt aktivierte Stütz‑/Bindegewebszellen (Fibroblasten) und erhöhte Aktivität eines Enzyms, das Kollagen quervernetzt — alles Faktoren, die das Gewebe starrer machen. Gleichzeitig wiesen Tumorzellen aus adipösen Mäusen Hinweise auf einen hochgefahrenen Fettstoffwechsel auf und akkumulierten mehr Lipidtröpfchen im Inneren.
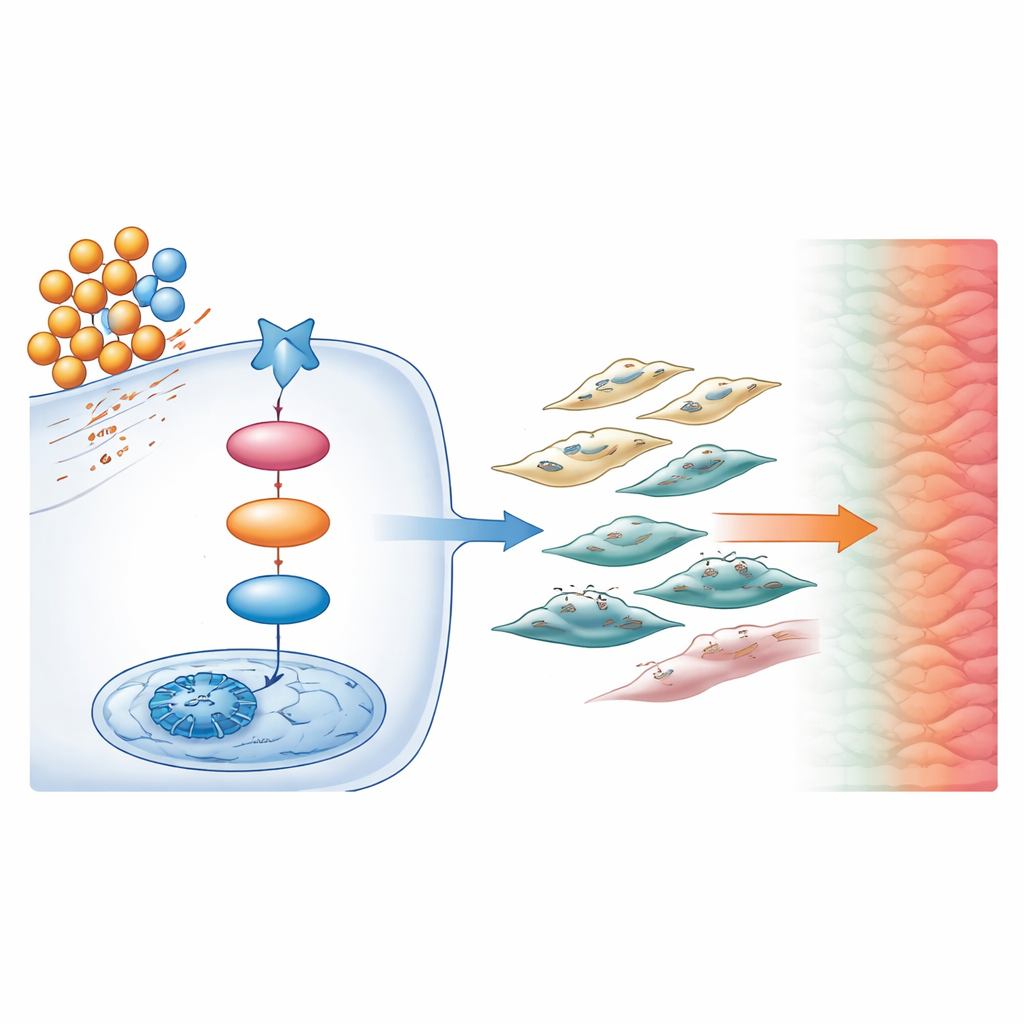
Eine verborgene chemische Kettenreaktion
Bei tiefergehenden Analysen nutzten die Wissenschaftler Lipidprofile und Genaktivitätsanalysen, um die molekulare Kettenreaktion zu kartieren, die diese Veränderungen antreibt. Sie fanden heraus, dass ein bestimmtes fettbasiertes Molekül, Diacylglycerol (DAG), in Tumoren von adipösen Mäusen erhöht war. DAG fungierte wie ein biochemischer Schalter und aktivierte ein Protein namens PKC in den Krebszellen. PKC steigerte wiederum die Aktivität eines zentralen Steuerproteins, CREB1, im Zellkern. Nach Aktivierung trieb CREB1 die Produktion von TGF‑β1 an, einem starken Signalstoff, der für Narbenbildung und die Förderung der Tumorstreuung bekannt ist. Zusammen bildete diese DAG → PKC → CREB1 → TGF‑β1‑Abfolge einen zentralen Signalweg, der überschüssiges Fett mit einem steiferen und invasiveren Tumor verband.
Ein teuflischer Dialog zwischen Zellen
TGF‑β1 wirkte nicht nur auf die Krebszellen selbst. Es aktivierte auch benachbarte Fibroblasten, die strukturellen Zellen, die das Gewebe um Tumoren herum aufbauen und umbauen. Unter dem Einfluss von Signalen aus DAG‑aktivierten Krebszellen schalteten Fibroblasten in einen hochaktiven Zustand, legten zusätzliches Kollagen ab und verschärften so das Tumorumfeld weiter. Diese aktivierten Fibroblasten sendeten wiederum Signale zurück an die Krebszellen, die deren Fettstoffwechsel, Wachstum und Invasivität erhöhten. In Mausmodellen erzeugte dieser Wechsel eine sich selbst verstärkende Schleife, die Tumoren in der Shear‑Wave‑Elastographie steifer, unter dem Mikroskop fibrotischer und anfälliger für die Bildung entfernter Metastasen machte.
Bilder in Behandlungshinweise verwandeln
Durch die Kombination von Patientendaten, Tierversuchen und detaillierten molekularen Studien zeigen die Autorinnen und Autoren, dass die in der Shear‑Wave‑Elastographie gemessene Steifigkeit mehr ist als eine strukturelle Auffälligkeit: Sie spiegelt die Aktivierung einer spezifischen, fettgetriebenen Signalkette wider, die das triple‑negative Mammakarzinom verschlechtert. Für Laien bedeutet das, dass eine nichtinvasive Ultraschallmessung der Tumorhärte offenbaren kann, wie stark dieser schädliche Signalweg eingeschaltet ist. In Zukunft könnten Patientinnen mit hohem BMI und sehr steifen Tumoren in der Elastographie als Hochrisiko eingestuft und für Therapien in Betracht gezogen werden, die PKC, CREB1, TGF‑β1 oder verwandte Schritte in der Schleife blockieren — wodurch eine einfache Bildgebung zu einem Leitfaden für präzisere, biologiegestützte Behandlungen wird.
Zitation: Wang, S., Zheng, D., Wang, Z. et al. The DAG/PKC/CREB1/TGF-β1 axis drives shear-wave elastography stiffness and malignant progression in triple-negative breast cancer via lipid metabolic reprogramming. Cell Death Dis 17, 327 (2026). https://doi.org/10.1038/s41419-026-08625-0
Schlüsselwörter: triple-negatives Mammakarzinom, Tumorsteifigkeit, Adipositas, Lipidstoffwechsel, Shear-Wave-Elastographie