Clear Sky Science · de
Metabolische Orchestrierung durch GGCT: Umleitung von Glutamin in die Glutathionbiosynthese bei gleichzeitiger Verstärkung der Glukose‑Anaplerose zur Tumorproliferation
Warum das für die Krebstherapie wichtig ist
Krebszellen wachsen schnell und verbrauchen dabei große Mengen an Brennstoff; zugleich müssen sie sich ständig vor toxischen Nebenprodukten ihres eigenen Stoffwechsels schützen. Diese Studie zeigt, wie ein wenig bekanntes Enzym, GGCT, Leber‑ und Prostatatumoren dabei hilft, zwei häufige Nährstoffe — Glutamin und Glukose — geschickt umzuleiten, sodass beides zugleich Wachstum antreibt und schädliche Moleküle, die sogenannten reaktiven Sauerstoffspezies, in Schach gehalten werden. Das Verständnis dieses metabolischen Balanceakts könnte neue Wege eröffnen, Tumoren zu verhungern oder ihre Abwehrkräfte zu überwältigen.
Wie Tumorzellen Brennstoff und Schutz jonglieren
Tumorzellen sind stark von Glutamin abhängig, einer Aminosäure mit doppelter Funktion: Sie kann zur Versorgung des zentralen energieproduzierenden Zyklus abgebaut werden und liefert außerdem Bausteine für Glutathion, ein starkes Antioxidans, das reaktive Sauerstoffspezies neutralisiert. Die Autorinnen und Autoren bestätigten zunächst, dass Glutaminspiegel in Lebertumoren höher sind als im umliegenden gesunden Gewebe und dass Krebszellen, die mit mehr Glutamin gezüchtet werden, sowohl in Kultur als auch in Mäusen schneller proliferieren. Bei Glutaminmangel verlangsamen sich die Zellen, wichtige Zellzyklusproteine sinken, und Tumoren in Tieren schrumpfen — teilweise, weil die antioxidativen Abwehrmechanismen geschwächt sind und reaktive Sauerstoffspezies akkumulieren.
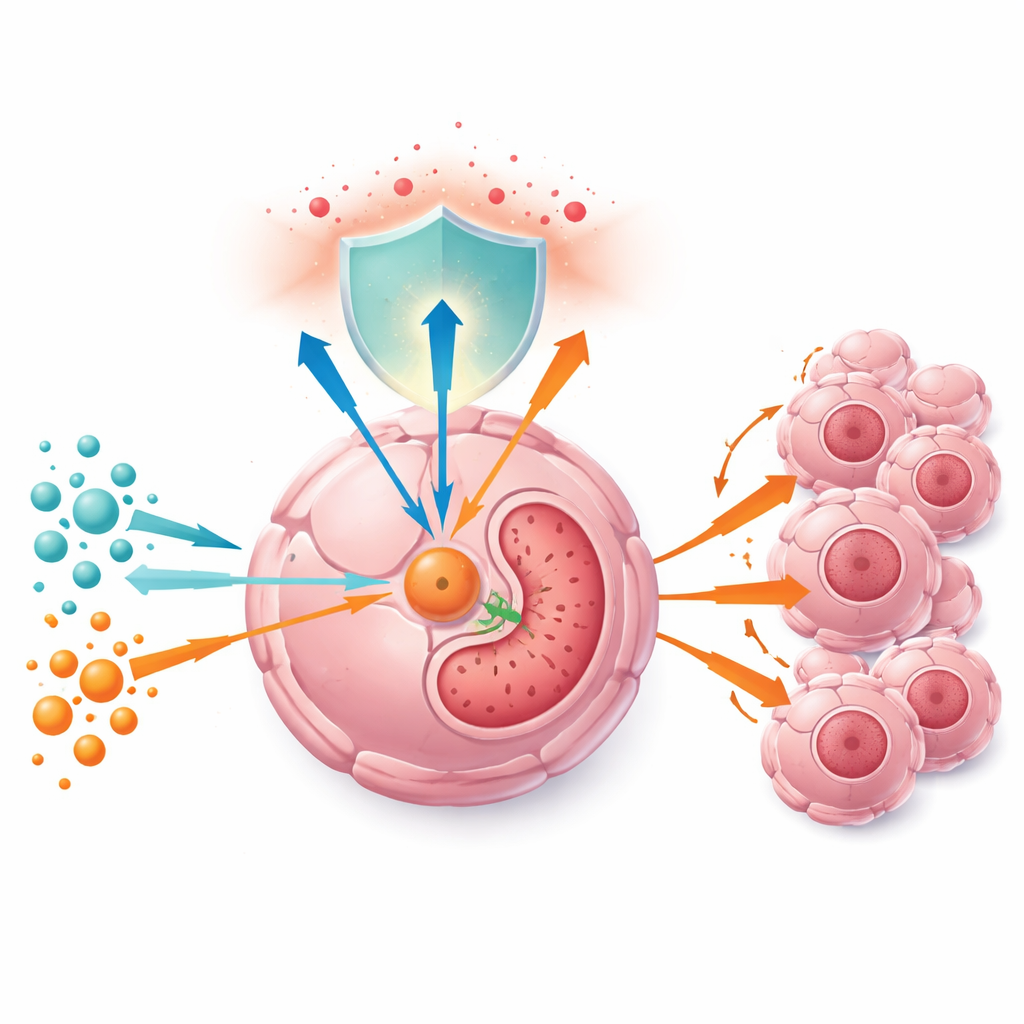
Ein Stoffwechselumschalter, der offen sichtbar ist
Beim Vergleich von Patientenproben und großen Krebsdatenbanken fanden die Forschenden, dass das Enzym GGCT in Leber‑ und Prostatatumoren konstant stärker exprimiert ist als in normalem Gewebe und dass höhere GGCT‑Spiegel schlechtere Prognosen vorhersagen. In Tumorproben wie in kultivierten Zellen steigen die GGCT‑Spiegel mit der Glutaminkonzentration, was darauf hindeutet, dass Tumoren die Verfügbarkeit von Glutamin über dieses Protein „ablesen“. Die Forschenden entwarfen eine Kontrollkette: Glutamin hält den wachstumsfördernden Faktor c‑Myc aktiv, der eine kleine regulatorische RNA namens miR‑29b‑3p unterdrückt; ist miR‑29b‑3p niedrig, wird GGCT aus seiner Hemmung entlassen und reichert sich an. Bei Glutaminmangel kehrt sich diese Kette um, miR‑29b‑3p steigt, GGCT‑Botschaften werden schneller abgebaut und das Enzymniveau fällt.
Glutamin umleiten und mehr Glukose aufnehmen
Um zu klären, was GGCT in der Zelle bewirkt, reduzierten oder erhöhten die Autorinnen und Autoren dessen Menge und maßen das Verhalten der Zellen sowie hunderte Metaboliten. Die Stilllegung von GGCT stoppte den Zellzyklus, verkleinerte Kolonien und verringerte Glutathion deutlich, während reaktive Sauerstoffspezies zunahmen; die Zugabe eines chemischen Antioxidans rettete das Wachstum teilweise. Unter dem Mikroskop wurden Mitochondrien auffällig verlängert und waren weniger effizient beim Sauerstoffverbrauch, während die Zellen versuchten zu kompensieren, indem sie die Glykolyse, den ersten Schritt des Zuckerabbaus, hochfuhren. Detaillierte metabolische Profile zeigten, dass Zwischenprodukte des zentralen Energiestoffwechselzyklus sanken, wenn GGCT fehlte, und zunahmen, wenn es überproduziert wurde.
Den Weg der Kohlenstoffatome verfolgen
Das Team verfolgte dann markierte Glutamin‑ und Glukoseatome, während sie durch den Tumorstoffwechsel flossen. Bei Überexpression von GGCT landete weniger markiertes Glutamin im Energiestoffwechselzyklus, und mehr wurde in neu gebildetes Glutathion gelenkt, was die antioxidativen Abwehrmechanismen stärkte. Gleichzeitig trug markierte Glukose stärker zum Zyklus bei und kompensierte das umgeleitete Glutamin. Eine mutierte Form von GGCT ohne normale Enzymaktivität konnte diese Verschiebungen oder die Proliferation nicht antreiben, was zeigt, dass die katalytische Funktion von GGCT entscheidend ist. Wichtig ist, dass das Zuführen von zusätzlichem Pyruvat oder das Verändern des Eintritts in den Energiestoffwechsel die zellulären Energiespiegel wiederherstellte, aber die reaktiven Sauerstoffspezies nicht senkte — was darauf hindeutet, dass GGCT vor allem das Redoxgleichgewicht über Glutathion steuert und nicht durch einfache Änderungen der Energieversorgung.
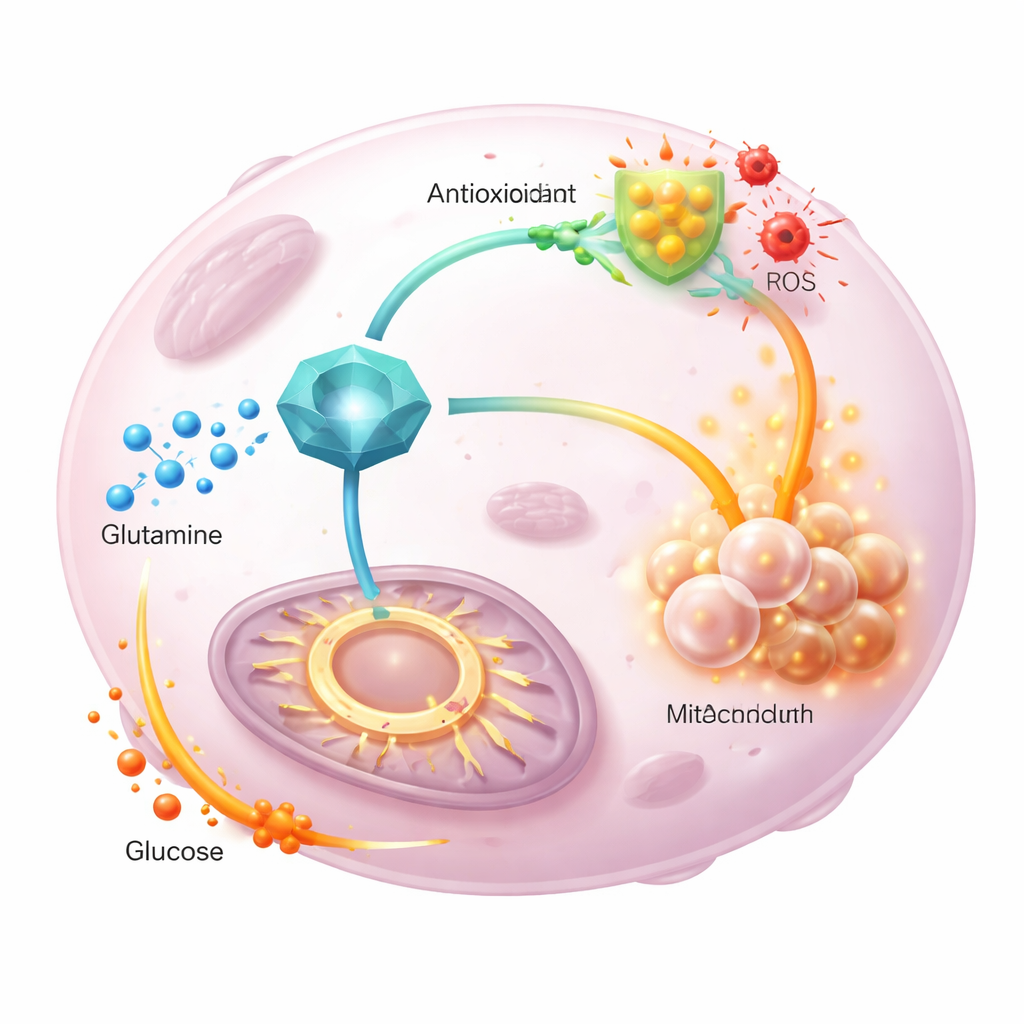
Was das für künftige Therapien bedeutet
In der Summe positionieren die Ergebnisse GGCT als zentralen Koordinator, der Tumoren erlaubt, die Aufgaben von Glutamin aufzuteilen: Mehr dieses Nährstoffs wird in die Produktion von Antioxidantien gelenkt, während Glukose in den Energiestoffwechsel gezogen wird, um die Zellteilung aufrechtzuerhalten. In Tiermodellen verlangsamte die Herunterregulierung von GGCT das Tumorwachstum, verringerte Glutathion und erhöhte oxidativen Stress; diese Effekte ließen sich teilweise mit einem Antioxidans rückgängig machen. Für eine allgemein verständliche Betrachtung lautet die Botschaft: Manche Krebsarten überleben, indem sie GGCT als metabolischen Umschalter nutzen; Wirkstoffe, die diesen Schalter deaktivieren, könnten gleichzeitig die Abwehr des Tumors gegen oxidative Schäden schwächen und seine flexible Nährstoffnutzung stören, wodurch Standardtherapien wirksamer werden.
Zitation: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Schlüsselwörter: Krebstoffwechsel, Glutamin, Glutathion, oxidativer Stress, GGCT‑Enzym