Clear Sky Science · de
Adipogene Transdifferenzierung reprogrammiert EMT-hohe PDAC-Zellen in einen post-mitotischen, adipozytenähnlichen Zustand und begrenzt Metastasen
Aggressive Krebszellen in harmlose Fettzellen verwandeln
Pankreaskrebs gehört zu den tödlichsten Krebsarten, was zum großen Teil daran liegt, dass er früh metastasiert und Standardtherapien widersteht. Diese Studie untersucht eine auffallend andere Idee: Anstatt zu versuchen, Tumorzellen zu vergiften oder auszuhungern, könnte man die gefährlichsten Pankreaskrebszellen dazu bringen, sich in fettähnliche Zellen zu verwandeln, die nicht mehr teilen oder im Körper wandern? Die Arbeit beschreibt, wie Forschende hoch aggressive Pankreaskrebszellen in einen stabilen, fettzellähnlichen Zustand drängten, der das Tumorwachstum verlangsamte und die Ausbreitung bei Mäusen verringerte, und deutet so auf einen neuen Ansatz zur Kontrolle dieser verheerenden Krankheit hin.
Warum Pankreaskrebs so schwer zu stoppen ist
Das duktale Adenokarzinom der Bauchspeicheldrüse, die Hauptform des Pankreaskrebses, hat eine sehr schlechte Prognose: Nur etwa einer von acht Patienten lebt fünf Jahre nach der Diagnose. Ein Teil des Problems ist, dass viele Tumorzellen in diesem Krebs einen gestaltwandelnden Zustand namens EMT einnehmen, der sie mobiler, invasiver und resistenter gegen Medikamente macht. Versuche, die zahlreichen Signale, die diesen Zustand antreiben, zu blockieren, brachten nur begrenzten Nutzen. Gleichzeitig zeigen die Bauchspeicheldrüse und ihre Tumoren eine überraschende Neigung, Fettzellen anzureichern, was die Frage aufwirft, ob sich diese verborgene Flexibilität in der Zellidentität nutzen lässt. Die Autoren nahmen an, dass, wenn EMT-reiche Pankreaskrebszellen bereits vorgespurt zur Veränderung sind, man sie vielleicht in eine ruhige, fettähnliche Identität umleiten kann statt in eine invasive.
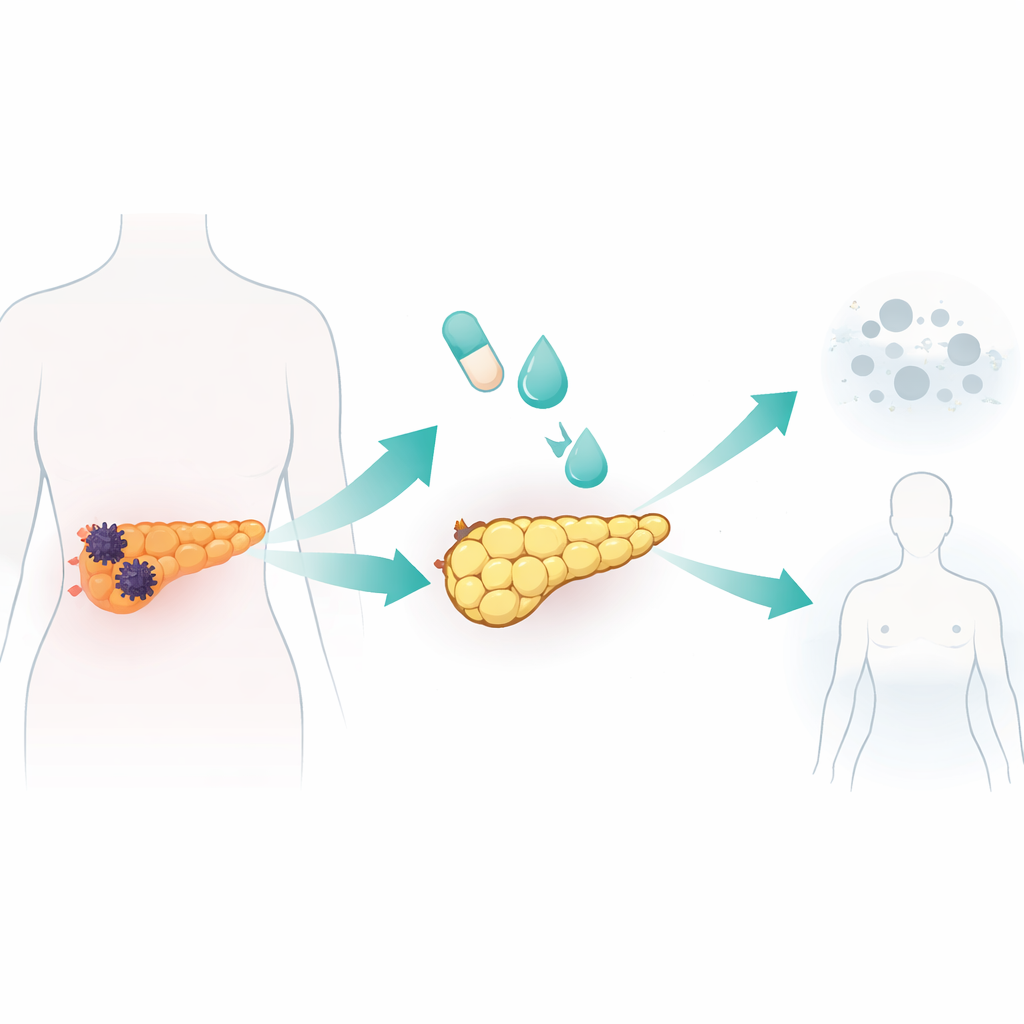
Krebszellen im Labor in fettähnliche Zellen umprogrammieren
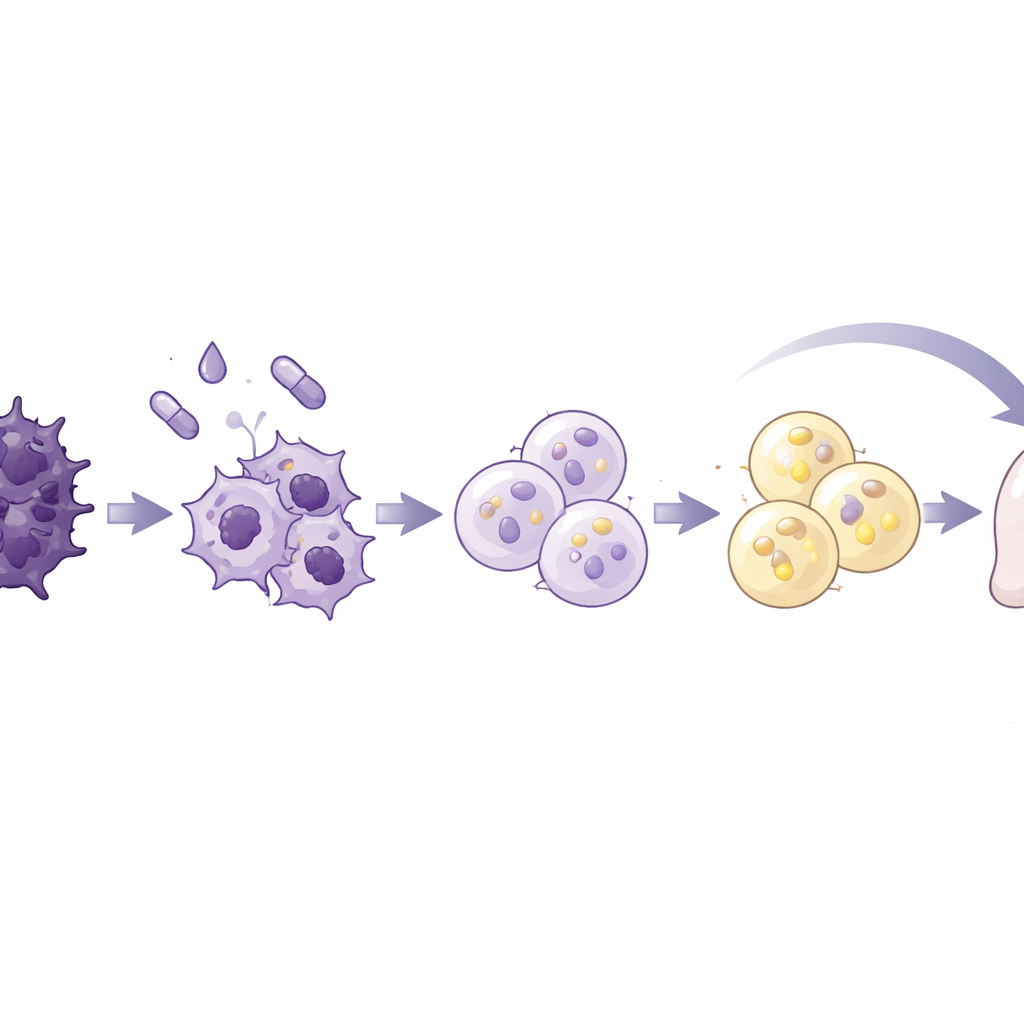
Das Team testete ein Standardcocktail zur Adipozyteninduktion, wie es in früheren Fettbiologie- und Brustkrebsstudien verwendet wurde, an sieben humanen Pankreaskrebszelllinien und einer normalen Pankreaszelllinie. Die Mischung kombinierte Insulin und ein Steroid mit Rosiglitazon, einem Wirkstoff, der einen zentralen Fettregulator aktiviert, sowie dem Signalprotein BMP2, um die Zellplastizität zu öffnen. Eine Krebszelllinie, AsPC-1 genannt, war besonders ansprechbar. Innerhalb von zehn Tagen wurden diese Zellen größer und runder und füllten sich mit Lipidtröpfchen — Kennzeichen von Fettzellen. Sie schalteten Gene und Proteine an, die typisch für reife Adipozyten sind, und zeigten robusten Fettstoffwechsel, einschließlich Sekretion von Adiponektin und gezieltem Abbau gespeicherter Lipide. Entscheidend ist, dass diese umgewandelten Zellen nicht mehr proliferierten, im frühen Zellzyklusstadium verharrten und deutlich weniger bewegten und invasiv waren als unbehandelte Krebszellen.
Programme der Krebszelle tief im Inneren abschalten
Um auf molekularer Ebene zu verstehen, was geschah, untersuchten die Forschenden die DNA-Verpackung und Genaktivität der umgewandelten Zellen. Sie fanden eine weitreichende Kondensation des Chromatins, des DNA–Protein-Komplexes, der den Zugang zu Genen steuert, zusammen mit einem globalen Rückgang der Genexpression — beide Merkmale nicht teilender Zellen. Gene, die EMT, Invasion und Metastasen unterstützen, einschließlich Matrix-abbauender Enzyme und zentraler EMT-Regulatoren, waren stark reprimiert, während fettbezogene Gene verstärkt wurden. Das gesamte Genexpressionsprofil verschob sich von einer mesenchymalen, hoch mobilen Identität zu einer, die reifen Fettzellen sehr ähnlich war. Signalwege, die mit Zellwachstum und der Reaktion auf einen wichtigen EMT-Treiber, TGF-beta, verknüpft sind, wurden gedämpft, während Pfade im Zusammenhang mit Lipidverarbeitung und Zelladhäsion verstärkt waren. Diese Veränderungen deuten darauf hin, dass die Zellen nicht nur verlangsamt, sondern grundlegend umprogrammiert wurden.
Den Ansatz in Mäusen testen
Die Wissenschaftler fragten dann, ob diese erzwungene, fettähnliche Umwandlung helfen kann, Tumoren in lebenden Tieren zu kontrollieren. Sie implantierten humane Pankreaskrebszellen in die Bauchspeicheldrüse oder die Milz von Mäusen, um Primärtumore und Lebermetastasen zu modellieren. Mäuse, die mit Rosiglitazon und BMP2 behandelt wurden, entwickelten kleinere Pankreastumore und zeigten reichlichere Lipidtröpfchen und Fettzellmarker innerhalb der Tumore sowie niedrigere Spiegel von EMT- und Invasionsgenen. Im Metastasemodell veränderte die Behandlung das frühe Tumorsamen nicht, verlangsamte aber im Laufe der Zeit die Ausbreitung der Lebertumorlast im Vergleich zu unbehandelten Tieren. Wichtig ist, dass das benachbarte normale Pankreasgewebe keine offensichtliche Fettzellkonversion zeigte und der fettähnliche Zustand in den Tumoren mindestens einen Monat nach Absetzen der Medikamente anhielt, was auf eine gewisse Dauerhaftigkeit und Spezifität hindeutet.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Diese Studie stützt ein provokantes Konzept: Für hoch plastische, EMT-reiche Pankreaskrebsarten könnte es möglich sein, „konvertieren statt töten“ — gefährliche, wandernde Tumorzellen in stabile, nicht teilende, fettähnliche Zellen umzuleiten, die weniger metastasierungsfähig sind. Obwohl dies vorläufige Arbeiten an Zellen und Mausmodellen sind und nicht alle Pankreaskrebsfälle gleichermaßen ansprechbar sind, eröffnet es einen neuen therapeutischen Weg, der durch Änderung der Zellidentität wirkt statt nur Wachstumssignale zu blockieren. In Zukunft könnten solche Transdifferenzierungsansätze mit gezielten Medikamenten oder Immuntherapien kombiniert werden, um Pankreaskrebs in einem ruhigeren, besser handhabbaren Zustand zu halten und das Risiko tödlicher Metastasen zu verringern.
Zitation: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Schlüsselwörter: Pankreaskrebs, Zellplastizität, Transdifferenzierung, Epitheliale-mesenchymale Transition, adipozytenähnliche Zellen