Clear Sky Science · de
CBX2-Phasenseparation trägt zur homologen Rekombinationsreparatur und Medikamentenresistenz beim Ovarialkarzinom bei
Warum diese Forschung wichtig ist
Eierstockkrebs gehört zu den tödlichsten Krebserkrankungen bei Frauen, vor allem weil viele Tumore auf Chemotherapie nicht mehr ansprechen. Diese Studie enthüllt einen verborgenen Überlebensmechanismus hochgradig seröser Ovarialkarzinome: Sie bilden winzige, flüssigkeitsähnliche Tropfen im Zellkern, die die DNA-Reparatur deutlich verstärken und Tumorzellen helfen, Schäden durch Standardmedikamente zu überstehen. Die Arbeit weist außerdem auf ein bereits verfügbares Medikament, Ibrutinib, als mögliche Möglichkeit hin, diese Schwachstelle bei Patientinnen auszunutzen, deren Tumore auf dieses tropfenbasierte Reparatursystem angewiesen sind.
Tumorzellen, die ihre DNA zu gut reparieren
Die meisten wirkungsvollen Krebsmedikamente wirken, indem sie die DNA so stark schädigen, dass Tumorzellen sich nicht mehr teilen können. Bei hochgradig serösem Ovarialkarzinom werden viele Tumore jedoch zu Experten im Ausbessern dieser Schäden, was zu einer Resistenz gegen Platinchemotherapie und PARP-Inhibitoren führt. Die Autorinnen und Autoren konzentrierten sich auf ein Protein namens CBX2, das chemische Markierungen an der DNA-Verpackung liest und in Ovarialtumoren höher exprimiert ist als in normalem Gewebe. In Patientendaten und Gewebeproben korrelierten höhere CBX2-Werte mit einer größeren Wahrscheinlichkeit für Platinresistenz und schnellerem Wiederauftreten, besonders in diesem aggressiven Subtyp.
Tropfen im Zellkern: eine reparaturfördernde „Werkbank“
CBX2 besitzt die ungewöhnliche Fähigkeit, dichte, tropfenförmige Cluster im Zellkern zu bilden — ein Prozess, der als Phasenseparation bekannt ist. Diese Tropfen verhalten sich wie winzige flüssige Werkbänke, die bestimmte Proteine konzentrieren können. Im Vergleich von Krebszellen mit normalem CBX2, ohne CBX2 oder mit einer Mutante, die keine Tropfen bilden kann, zeigten die Forschenden, dass CBX2-Tropfen zentral dafür sind, wie Tumorzellen gebrochene DNA reparieren. Entfernt man CBX2, brechen Chromosomen häufiger, DNA-Schadenssignale häufen sich, und beide Hauptwege zur Reparatur von Doppelstrangbrüchen werden geschwächt. Die Wiederherstellung von normalem CBX2 brachte die Reparaturkapazitäten zurück, eine tropfendefekte Variante jedoch nicht, obwohl diese noch an DNA binden konnte. 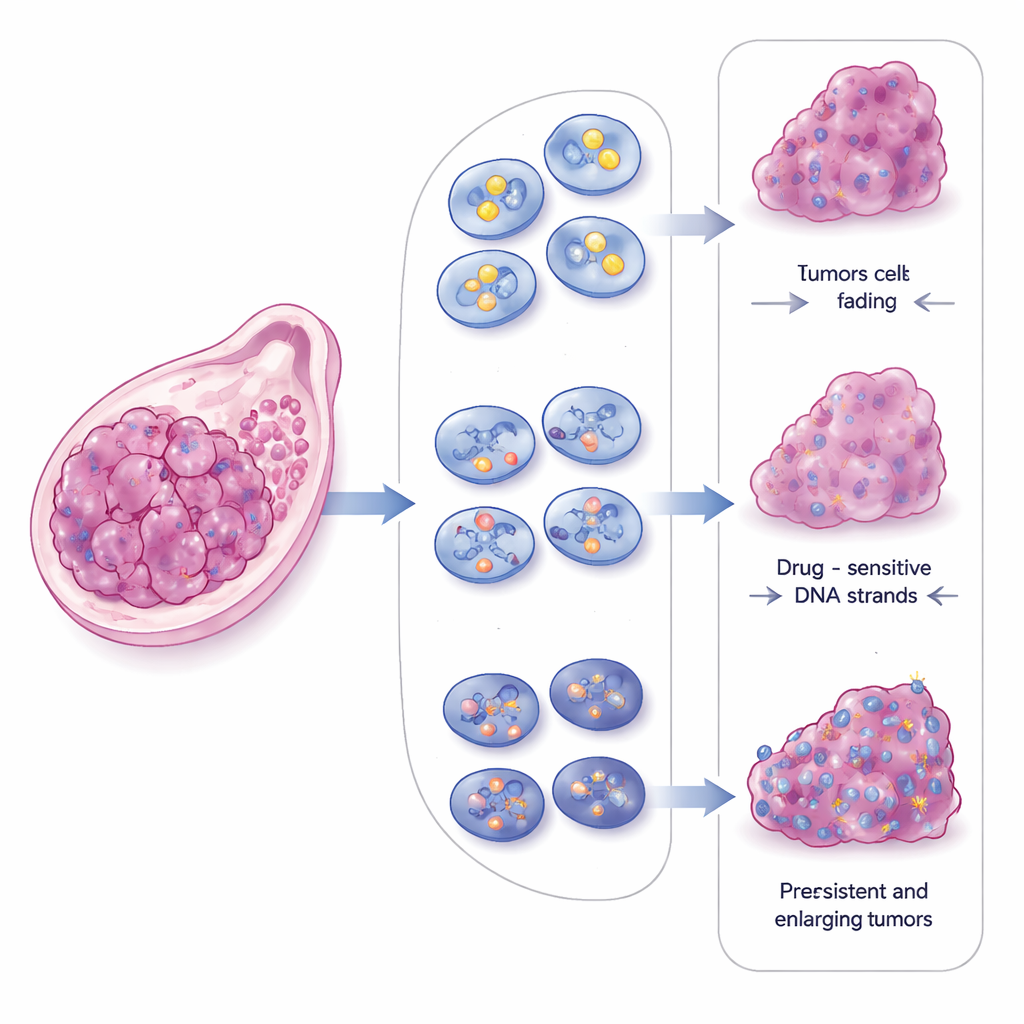
Wie CBX2-Tropfen die Reparaturmannschaft organisieren
Bei genauerer Untersuchung prüfte das Team, welche Reparaturproteine in Anwesenheit oder Abwesenheit von CBX2-Tropfen tatsächlich an die DNA gebunden sind. Sie fanden, dass CBX2-Tropfen Schlüsselakteure der Schadensantwort anlocken, darunter PARP1, 53BP1, BRCA1 und RAD51 — Proteine, die entscheiden, wie ein Bruch repariert wird, und die Reparatur ausführen. Live‑Zell‑Imaging zeigte zwei Ausprägungen von CBX2-Tropfen: eine mobile, flüssige Form, die dynamisch mit geschädigtem Chromatin vermischt, und eine dichte, festigkeitsähnliche Form, die das nicht tut. Nur die mobilen Tropfen überlappten mit DNA-Schadensfoci und den Hauptreparaturproteinen, was darauf hindeutet, dass diese flüssige Phase als funktionales Gerüst wirkt, das die Reparaturmaschinerie genau dorthin zusammenführt, wo sie gebraucht wird.
Eine Stärke mit einem bestehenden Medikament zur Schwäche machen
Da CBX2-Tropfen Tumorzellen besonders gut bei der DNA-Reparatur machen, fragten die Autorinnen und Autoren, ob diese erhöhte Reparaturfähigkeit gegen die Zellen selbst eingesetzt werden kann. Sie durchsuchten eine Wirkstoffbibliothek an Zellen mit bzw. ohne funktionelle CBX2-Tropfen und entdeckten, dass Ibrutinib — ein oral verabreichtes Medikament, das bereits für bestimmte Blutkrebserkrankungen zugelassen ist — besonders toxisch für Zellen war, die auf CBX2-Kondensate angewiesen sind. Ibrutinib verhinderte nicht die Bildung der Tropfen, schwächte jedoch selektiv den hochpräzisen Reparaturweg, von dem diese Zellen abhängig sind. In Tiermodellen schrumpften Tumore mit CBX2-Tropfen unter Ibrutinib-Behandlung, und dreidimensionale Organoide aus Patientenproben mit hohem CBX2-Gehalt waren gegenüber dem Medikament empfindlicher als solche mit niedrigem Gehalt. 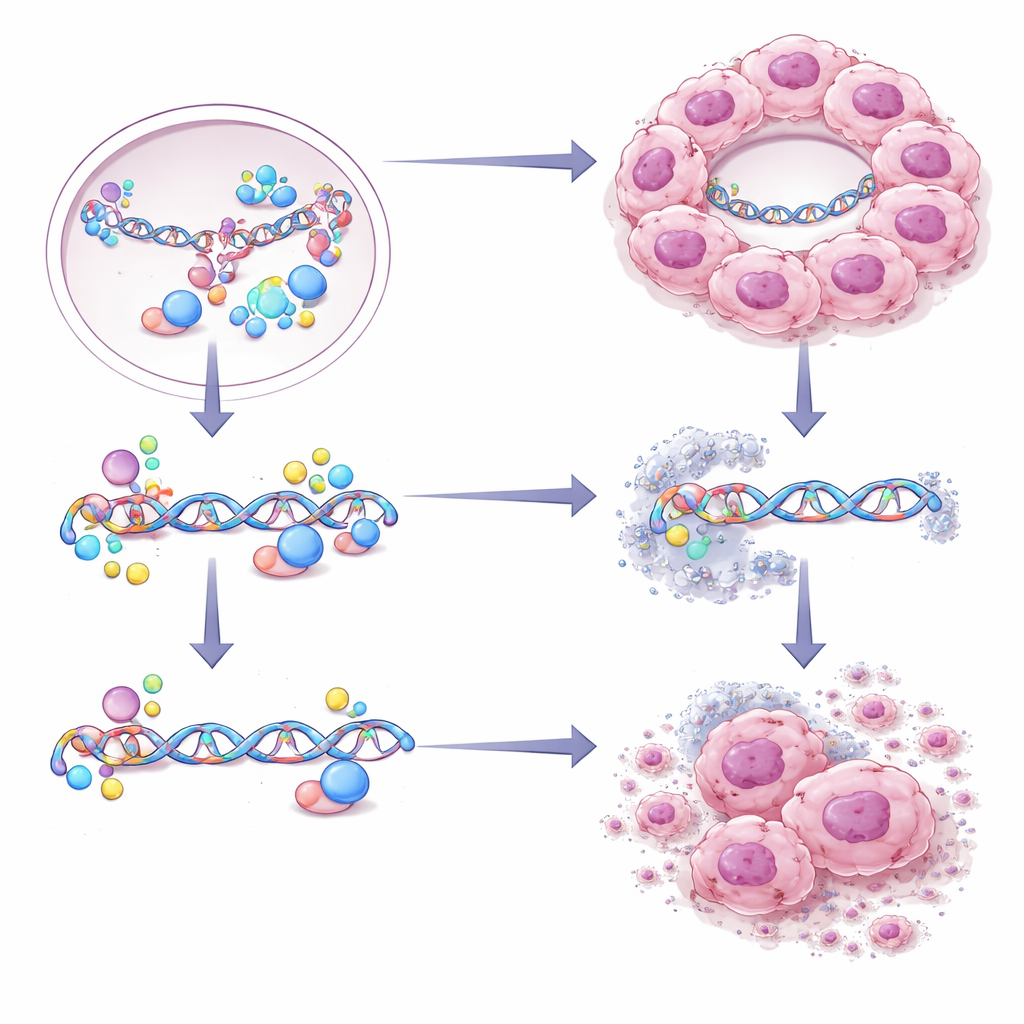
Was das für Patientinnen bedeuten könnte
Für Patientinnen legt die Studie zwei wichtige Ideen nahe. Erstens könnte das Vorkommen und Muster von CBX2-Tropfen im Tumorgewebe helfen vorherzusagen, wie gut jemand auf Platinchemotherapie und PARP-Inhibitoren anspricht: Patientinnen ohne CBX2 schneiden am besten ab, solche mit diffusem CBX2 liegen im Mittelfeld, und Patientinnen mit klar erkennbaren CBX2-Kondensaten haben die schlechteste Prognose. Zweitens könnte dasselbe Tropfenmuster Patientinnen kennzeichnen, die von Ibrutinib profitieren könnten — also eine Umwidmung eines Blutkrebsmittels für einen schwer zu behandelnden Ovarialkarzinom-Subtyp. Im Kern zeigt die Arbeit, dass die Strukturen, die die Tumor-DNA schützen, auch eine neue Achillesferse offenbaren können — und damit einen möglichen Weg zu personalisierterer und wirksamerer Therapie bieten.
Zitation: Sun, S., Huang, L., Ma, Y. et al. CBX2 phase-separation contributes to homologous recombination repair and drug resistance in ovarian cancer. Cell Death Dis 17, 366 (2026). https://doi.org/10.1038/s41419-026-08605-4
Schlüsselwörter: Eierstockkrebs, Medikamentenresistenz, DNA-Reparatur, Phasenseparation, Ibrutinib