Clear Sky Science · de
Hemmung der Vaccinia-related kinase 2 macht den Glutathionstoffwechsel bei Pankreaskrebs verwundbar
Warum das für Pankreaskrebs wichtig ist
Pankreaskrebs zählt zu den tödlichsten Krebsarten, teilweise weil Standardbehandlungen oft versagen. Diese Studie deckt eine verborgene Schwäche bestimmter Pankreastumoren auf: ihre Abhängigkeit von einem zellulären „Schild“ gegen toxische Nebenprodukte des Sauerstoffs. Indem untersucht wird, wann dieser Schild brüchig ist und wie ein Krebsgen namens VRK2 ihn stärkt, schlagen die Forscher neue Wege vor, Krebszellen selektiv zu vergiften und dabei gesundes Gewebe zu schonen.
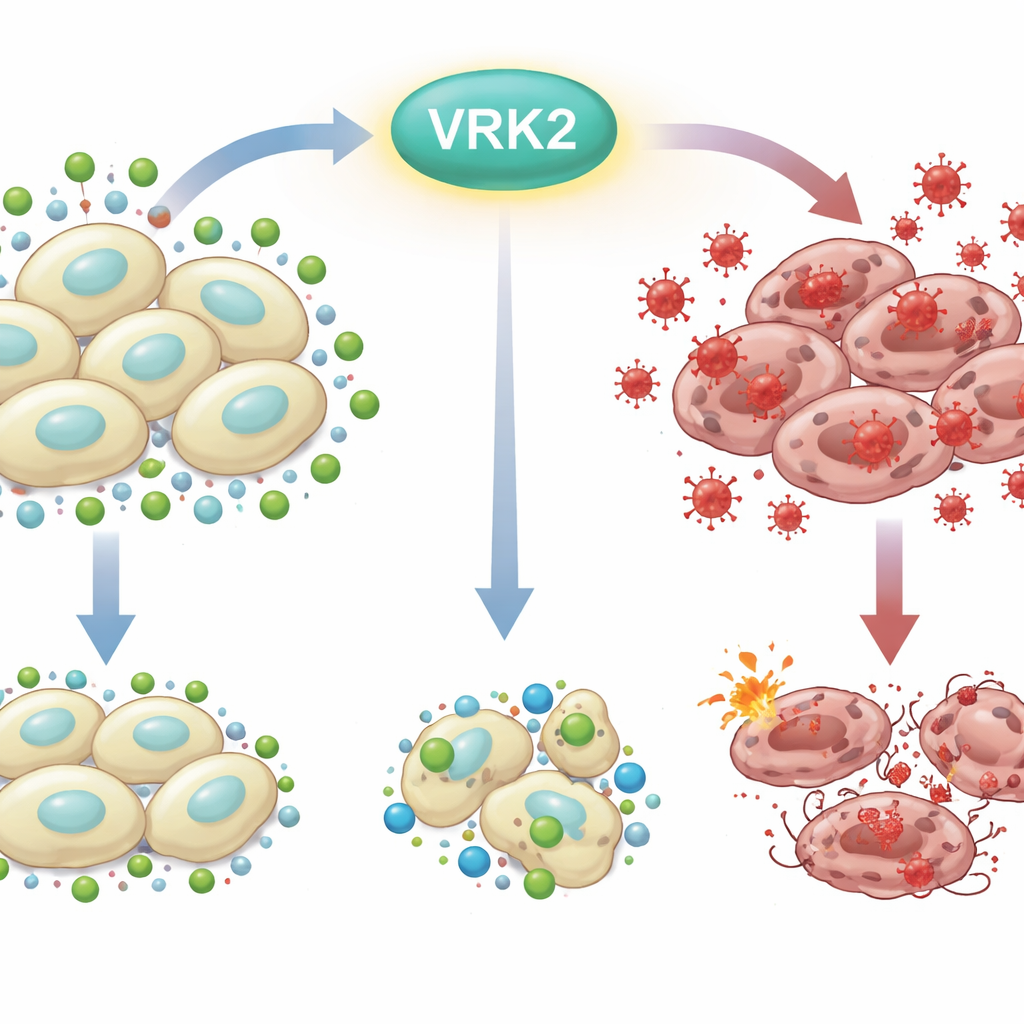
Das Rostproblem der Zelle
Jede Zelle kämpft ständig gegen ein „von innen heraus Rosten“, verursacht durch reaktive Sauerstoffspezies—hochreaktive Formen des Sauerstoffs, die DNA, Lipide und Proteine schädigen können. Um zu überleben, nutzen Zellen chemische Abwehrmechanismen; Glutathion dient dabei als einer der wichtigsten Schilde. Pankreaskrebszellen, die unter harten Bedingungen leben und schnell wachsen, sind stark auf Stoffwechseltricks angewiesen, um genug Glutathion bereitzuhalten. Wird dieses Gleichgewicht zwischen schädlichen Oxidantien und schützenden Antioxidantien gestört, kann das die Krebszellen über die Grenze zur Zellteilung und schließlich zum Zelltod treiben.
Eine verborgene Schwachstelle finden
Die Forscher begannen damit, VRK2 auszuschalten—ein krebsförderndes Gen, das zuvor mit schlechteren Prognosen bei Pankreaskrebs in Verbindung gebracht worden war—und testeten dann 281 stoffwechselgerichtete Verbindungen. Sie entdeckten, dass Zellen ohne VRK2 auffallend empfindlich auf Wirkstoffe reagierten, die die Glutathionproduktion blockieren. In diesen VRK2-defizienten Zellen sanken die Glutathionspiegel, während reaktive Sauerstoffarten anstiegen und die Zellen abtöteten. Die Zugabe zusätzlicher Antioxidantien oder glutathionähnlicher Moleküle rettete die Zellen, was bestätigte, dass die zentrale Verwundbarkeit genau in ihrer beeinträchtigten Fähigkeit lag, oxidativen Stress zu entgiften.
Wie VRK2 den Krebszellen zur Rüstung verhilft
Als Nächstes fragten die Forschenden, warum VRK2 den Glutathionstoffwechsel verändert. Sie konzentrierten sich auf ein Transporterprotein namens SLC7A11, das in der Außenmembran der Zelle sitzt und Cystin einführt, einen Baustein zur Glutathionherstellung. Überraschenderweise veränderte VRK2 nicht die Gesamtmenge an SLC7A11, die die Zelle produzierte; stattdessen steuerte es, ob dieser Transporter erfolgreich zur Zelloberfläche gelangte. In gesunden VRK2-aktiven Zellen wandert SLC7A11 vom endoplasmatischen Retikulum über den Golgi zur Membran. VRK2 fördert diesen Transport, indem es ein Fracht-Sortierprotein namens Sec24C chemisch modifiziert, das hilft, SLC7A11 in Vesikel zu verladen. Fehlt VRK2 oder wird es blockiert, bleibt SLC7A11 im Zellinneren stecken, weniger Transporter erreichen die Oberfläche und der Glutathionschild schwächt sich ab.
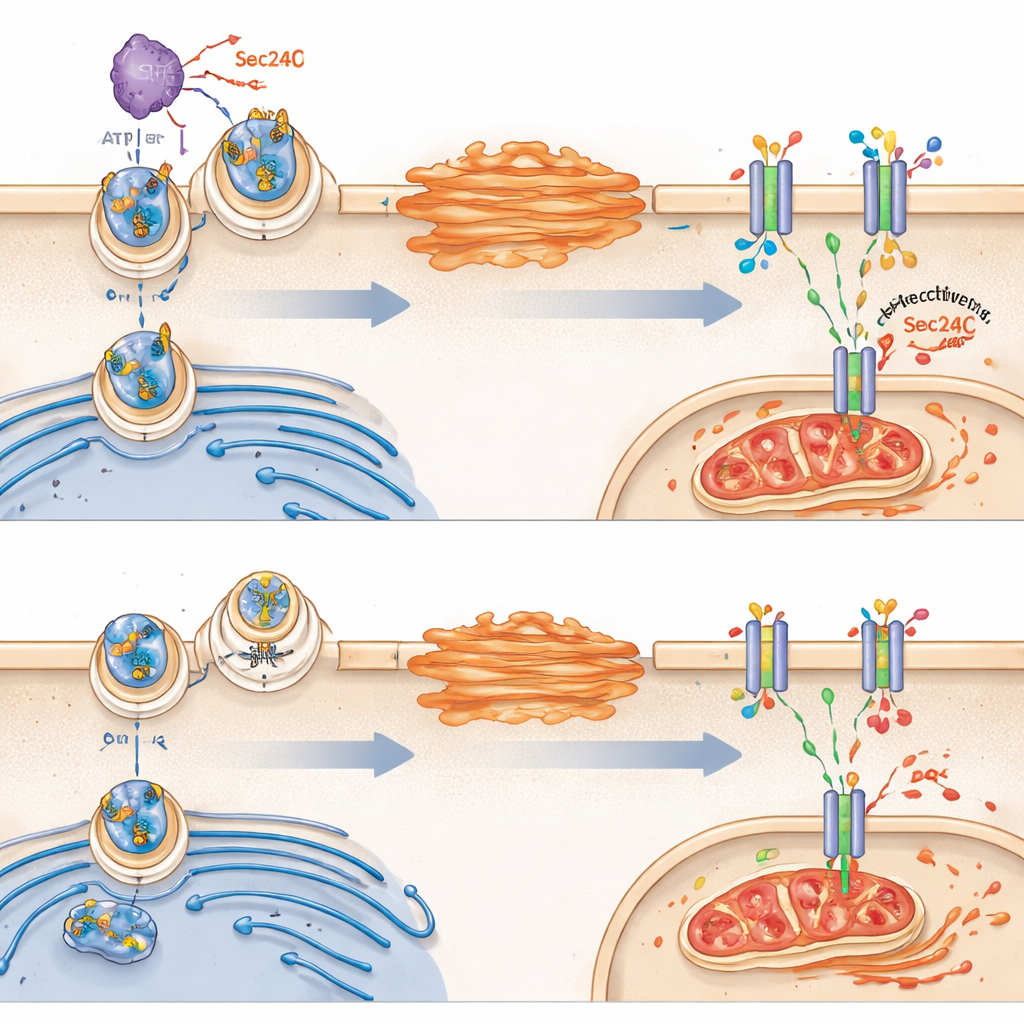
Vom gebrochenen Schild zur Ferroptose
Ohne ausreichend Membran-SLC7A11 haben VRK2-defiziente Zellen Schwierigkeiten, Cystin aufzunehmen und Glutathion aufrechtzuerhalten. Das macht sie besonders anfällig für eine Form des eisenabhängigen Zelltods namens Ferroptose, die durch unkontrollierte Oxidation von Membranlipiden und mitochondriale Schäden gekennzeichnet ist. Die Studie zeigte, dass Wirkstoffe, die die Glutathionsynthese blockieren, bei VRK2-defizienten Zellen Merkmale der Ferroptose auslösten, darunter deformierte Mitochondrien und Anreicherung von lipidoxidierten Produkten. Die Blockade der Ferroptose, nicht aber anderer Zelltodtypen, schützte diese Zellen—ein deutlicher Hinweis darauf, dass ihre Achillesferse die Unfähigkeit ist, oxidativen Schaden zu begrenzen.
Zur Anleitung personalisierter Behandlungsentscheidungen
Schließlich testeten die Forschenden das Konzept in Tiermodellen und in frisch aus Patienten gewonnenen Zellen. Tumoren mit niedrigem VRK2-Spiegel schrumpften unter Behandlung mit einem glutathionorientierten Wirkstoff, während Tumoren mit hohem VRK2-Expression größtenteils resistent blieben. Wurden VRK2-hohe Tumoren jedoch zusätzlich mit einem VRK2-blockierenden Wirkstoff behandelt, gewannen sie wieder Anfälligkeit gegenüber der Glutathionhemmung. Das legt nahe, dass VRK2-Spiegel Patienten in Gruppen einteilen können: solche, deren Tumoren von vornherein empfindlich gegenüber glutathionzielgerichteter Therapie sind, und solche, die von einer zweigleisigen Strategie profitieren könnten, bei der zunächst VRK2 deaktiviert und anschließend der Glutathionstoffwechsel angegriffen wird.
Was das für Patientinnen und Patienten bedeutet
Kurz gesagt zeigt diese Arbeit, dass einige Pankreaskrebsarten mithilfe von VRK2 ihren Antioxidantien-Schild stark halten. Nimmt man VRK2 weg, dünnt dieser Schild aus; entzieht man zusätzlich das Glutathion, kollabieren die Krebszellen unter oxidativem Stress. Die Messung von VRK2 in Tumoren könnte Ärzten daher helfen zu entscheiden, wer am ehesten von Medikamenten profitiert, die den Glutathionstoffwechsel stören, und wer möglicherweise zunächst eine VRK2‑gerichtete Behandlung benötigt. Zwar sind weitere Untersuchungen am Menschen nötig, doch die Studie skizziert einen klaren Weg zu stärker individualisierten, stoffwechselbasierten Therapien für eine Krebsart, die dringend bessere Optionen braucht.
Zitation: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Schlüsselwörter: Pankreaskrebs, Glutathionstoffwechsel, VRK2, Ferroptose, SLC7A11