Clear Sky Science · de
Unterdrückung von EGFR durch das neue Biguanid 4C verstärkte die Wirkung von PARP-Inhibitoren bei Eierstockkrebs durch Herunterregulierung von BRCA2 und Rad51
Warum diese Forschung wichtig ist
Für viele Menschen mit einer Diagnose von Eierstockkrebs wirken heutige zielgerichtete Medikamente nur bei einer kleinen Minderheit, deren Tumoren bestimmte genetische Defekte tragen. Diese Studie untersucht einen Ansatz, um die Vorteile einer wichtigen Medikamentenklasse, der PARP-Inhibitoren, auf die deutlich größere Gruppe von Patientinnen auszudehnen, deren Tumoren diese Mutationen nicht aufweisen. Durch die Kombination einer neuen experimentellen Verbindung mit bestehenden Wirkstoffen zeigen die Forscher eine Strategie, Krebszellen in eine tödliche Sackgasse zu treiben, während gesundes Gewebe geschont wird.
Ein Hindernis in der aktuellen Behandlung von Eierstockkrebs
Eierstockkrebs wird häufig spät entdeckt und gehört zu den tödlichsten Krebserkrankungen bei Frauen. PARP-Inhibitoren, wie Olaparib, können bemerkenswert wirksam sein, und zwar vor allem bei Patientinnen, deren Tumoren bereits Defekte in einem DNA-Reparaturweg aufweisen, der mit den Genen BRCA1 und BRCA2 verknüpft ist. Die meisten Tumoren verfügen jedoch weiterhin über intakte Reparaturmechanismen und können die durch diese Medikamente verursachten DNS-Schäden beheben, sodass Krebszellen überleben. Ein zentraler Bestandteil dieser Reparaturmannschaft bilden die Proteine BRCA2 und Rad51, die gebrochene DNA-Stränge mittels eines Prozesses namens homologe Rekombination wieder zusammenfügen. Wege zu finden, diesen Reparaturweg gezielt in Krebszellen zu schwächen, könnte PARP-Inhibitoren für wesentlich mehr Patientinnen nutzbar machen.
Die Rolle eines bekannten Wachstumsschalters
Das Team konzentrierte sich auf ein bekanntes, krebsassoziiertes Molekül, den epidermalen Wachstumsfaktor-Rezeptor (EGFR), der auf der Oberfläche vieler Tumorzellen sitzt und deren Wachstum antreibt. Sie fanden heraus, dass EGFR mehr tut als Wachstumssignale zu senden: In Eierstockkrebszellen mit normalen BRCA-Genen standen hohe EGFR-Werte in Verbindung mit schlechterem Überleben der Patientinnen und Resistenz gegenüber PARP-Inhibitoren. Wurde EGFR in Zellkulturen und in Mäusen reduziert oder ausgeschaltet, wurden Tumoren deutlich anfälliger für Olaparib. Die Forscher zeigten, dass EGFR BRCA2 und Rad51 nach DNA-Schäden in den Zellkern befördert, wo sie Brüche reparieren und die Wirkung der Behandlung abschwächen können. Es genügte nicht, nur die Enzymaktivität von EGFR zu blockieren; die Gesamtmenge des EGFR-Proteins musste gesenkt werden, um diesen Reparaturweg signifikant zu stören.
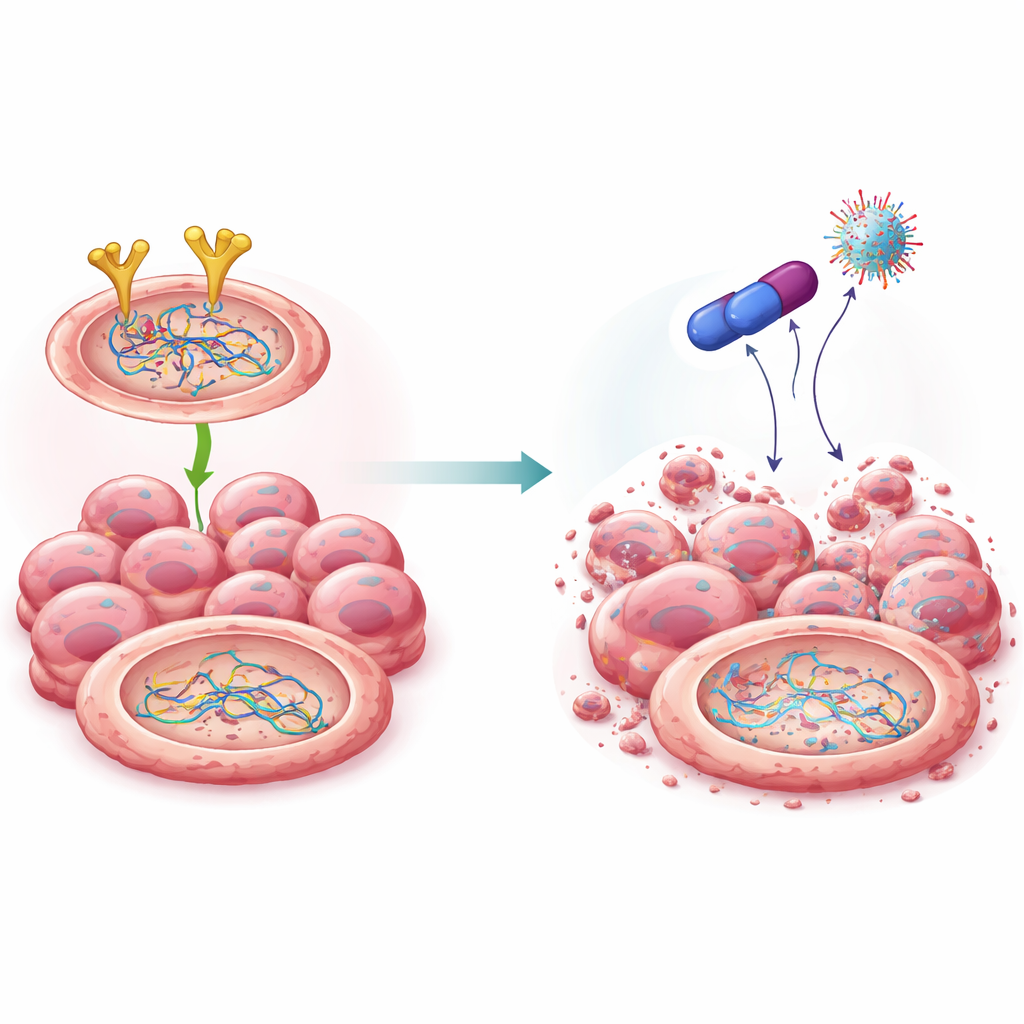
Eine neue Verbindung, die die Reparaturmannschaft entwaffnet
Aufbauend auf früheren Arbeiten mit einer Wirkstoffklasse, die als Biguanide bekannt ist, synthetisierten die Wissenschaftler mehrere chemische Verwandte und identifizierten ein besonders wirkungsvolles Molekül namens 4C. Diese Verbindung war stark toxisch für Eierstockkrebszellen, aber relativ schonend gegenüber normalen Zellen. Computermodelle und Labortests deuteten darauf hin, dass 4C direkt an EGFR bindet und es für den Abbau in der zellulären Proteinasche kennzeichnet. Im Gegensatz zu manchen bestehenden EGFR-Präparaten verringerte 4C die Gesamtmenge an EGFR, statt nur dessen Aktivität zu hemmen. Mit fallenden EGFR-Spiegeln nahm auch die Stabilität von BRCA2 und Rad51 ab: Sie wurden für den Abbau markiert, zersetzt und konnten die effiziente DNA-Reparatur nicht mehr unterstützen. Wichtig ist, dass dieses Zurückfahren auf Proteinebene erfolgte, ohne die zugrunde liegenden Gene zu verändern.
Eine Rettungsroute innerhalb der Zelle blockieren
Die Studie enthüllte eine detailliertere Ereigniskette, die DNS-Schäden mit dem Überleben von Tumoren verbindet. Nachdem PARP-Inhibitoren die DNA geschädigt haben, sendet ein weiterer Sensor, das Protein ATM, eine Nachricht vom Zellkern in das Zellplasma. Als Reaktion darauf arbeitet EGFR mit BRCA2 und Rad51 zusammen und hilft ihnen, in den Zellkern zu gelangen, wo sie die Schäden reparieren. Die Forscher entdeckten, dass ein drittes Protein, c-Cbl, normalerweise als eine Art Kennzeichner für den Abbau von BRCA2 und Rad51 dient. EGFR konkurriert mit c-Cbl um den Zugang zu diesen Reparaturproteinen und schützt sie so davor, für den Abbau markiert zu werden. Wenn 4C die EGFR-Spiegel senkt, kann c-Cbl leichter an BRCA2 und Rad51 binden, was zu deren Markierung, Abbau und Verlust führt. Mit weniger Reparaturproteinen im Zellkern häufen sich DNA-Läsionen an und Krebszellen werden deutlich empfindlicher gegenüber PARP-Inhibitoren.
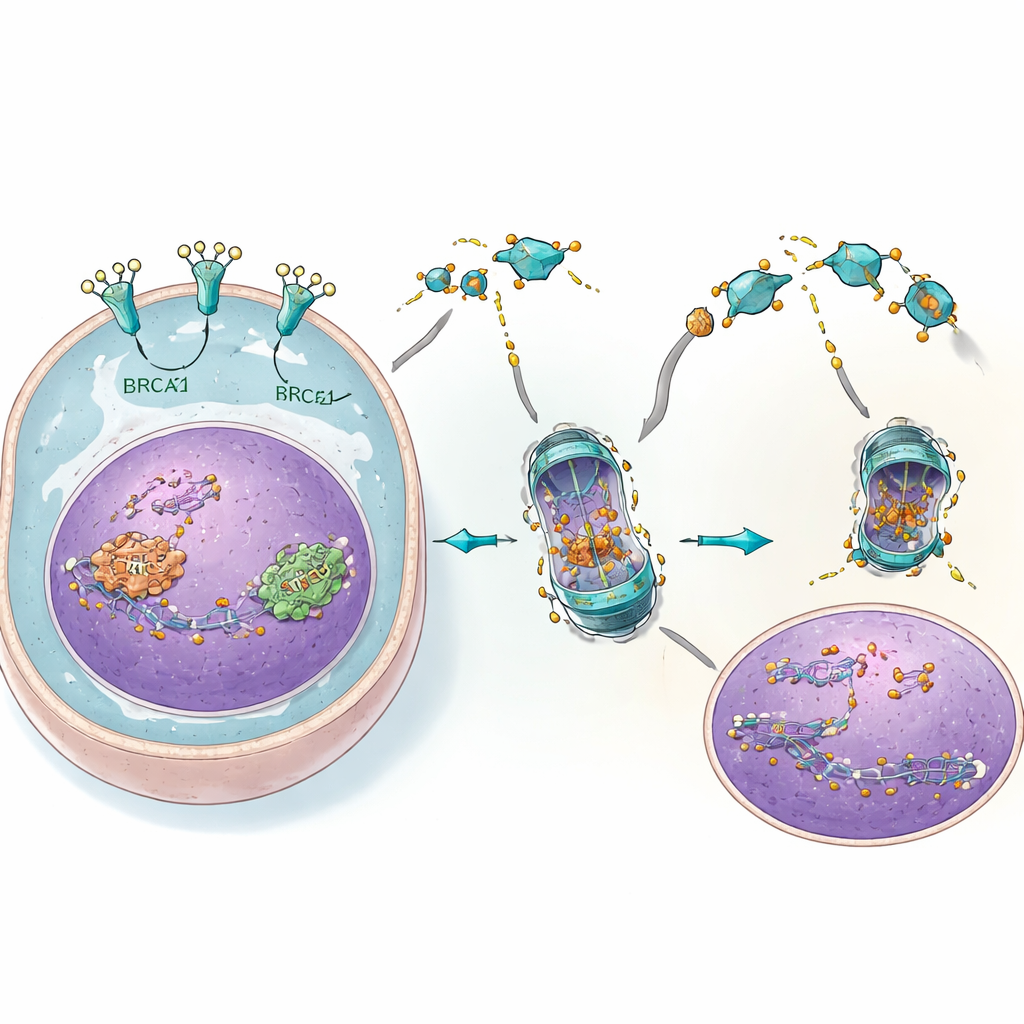
Von Zellen zu Tieren: eine potente Kombination
Sowohl in kultivierten Zellen als auch in Mausmodellen erzeugte die Kombination von 4C mit PARP-Inhibitoren einen kraftvollen Doppelschlag. Tumoren mit normalen BRCA-Genen, die entweder dem einen oder dem anderen Wirkstoff allein widerstanden, schrumpften dramatisch oder stellten ihr Wachstum ein, wenn sie beiden gleichzeitig ausgesetzt wurden. Marker für DNA-Schäden stiegen stark an, was zur Idee passt, dass die Reparatur überfordert wurde. Gleichzeitig zeigten normale Zellen und wichtige Organe wie Leber und Nieren nur wenig Anzeichen von Schaden, wahrscheinlich weil sie deutlich niedrigere EGFR-Spiegel haben und weniger auf diesen speziellen Reparaturweg angewiesen sind. Der Vorteil der Kombination erstreckte sich zudem auf die Verringerung der Ausbreitung von Eierstockkrebszellen im Körper.
Was das für Patientinnen bedeuten könnte
Diese Arbeit schlägt einen Weg vor, die Stärke einer Krebszelle in eine Schwäche zu verwandeln. Durch die gezielte Hemmung von EGFR mit der neuartigen Verbindung 4C entreißen die Forscher den Tumoren den Schutz, den BRCA2 und Rad51 bieten, und bringen Tumoren mit ansonsten intakter DNA-Reparatur dazu, sich in ihrem Ansprechen auf PARP-Inhibitoren wie BRCA-mutierte Krebserkrankungen zu verhalten. Diese erzwungene Verwundbarkeit, bekannt als „synthetische Letalität“, könnte die Einsatzmöglichkeiten vorhandener Medikamente für deutlich mehr Frauen mit Eierstockkrebs erweitern, bei beherrschbaren Nebenwirkungen. Obwohl 4C noch experimentell ist und umfangreiche Prüfungen in weiterführenden Modellen und klinischen Studien benötigt, liefert die Studie eine klare Blaupause dafür, wie das Zerlegen spezifischer Reparaturhelfer in Tumorzellen die Therapieergebnisse verbessern könnte.
Zitation: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Schlüsselwörter: Eierstockkrebs, PARP-Inhibitoren, EGFR, DNA-Reparatur, zielgerichtete Therapie