Clear Sky Science · de
Verlust von PRKACB fördert Metastasenbildung bei diffuser Magenkrebs durch Aktivierung der RhoA-Signalgebung
Warum diese Studie für Magenkrebs wichtig ist
Diffuser Magenkrebs ist eine besonders aggressive Form von Magenkrebs, die sich häufig weit in der Bauchhöhle ausbreitet, wodurch die Behandlung schwierig und die Prognose schlecht ist. Diese Studie untersucht, warum diese Tumoren so metastasenfreudig sind, und deckt ein molekulares Bremssystem auf, das normalerweise verhindert, dass Krebszellen abwandern — und zeigt, was passiert, wenn diese Bremse versagt. Das Verständnis dieses versteckten Kontrollschalters könnte neue Wege eröffnen, um vorherzusagen, welche Patienten das höchste Risiko tragen, und um Wirkstoffe zu entwickeln, die die gefährliche Ausbreitung verlangsamen oder stoppen.
Eine gefährliche Form von Magenkrebs
Nicht alle Magenkrebse verhalten sich gleich. Darmtypische Tumoren bilden eher strukturierte Massen, während diffuser Magenkrebs (DGC) aus verstreuten Zellen besteht, die sich leicht vom Primärtumor lösen. Patienten mit DGC haben ein höheres Sterberisiko als solche mit dem Darmentyp, zum Teil weil ihre Tumoren leichter neue Herde in der Bauchhöhle bilden. Frühere genetische Untersuchungen hatten DGC bereits mit wiederkehrenden Veränderungen im Gen RHOA in Verbindung gebracht, das die Zellbewegung und -form beeinflusst. Unklar war jedoch, wie diese Veränderungen mit den breiteren Signalnetzen zusammenhängen, die steuern, ob Krebszellen an ihrem Ort bleiben oder migrieren.
Suche nach einer fehlenden Bremse in Tumorproben
Die Forschenden konzentrierten sich auf ein Protein namens PRKACB, eine katalytische Untereinheit des bekannten Enzyms Proteinkinase A, das viele Zellfunktionen durch Phosphorylierung anderer Proteine feinreguliert. Eine frühere Proteomik-Studie hatte bereits angedeutet, dass PRKACB in aggressiven DGC ungewöhnlich gering ausgeprägt ist. Um das zu prüfen, analysierte das Team Tumorproben von 376 Patientinnen und Patienten und verglich diffusen und darmtypischen Krebs sowie das umliegende nicht-krebsartige Gewebe. Sie fanden, dass PRKACB in diffusen Tumoren markant reduziert war, insbesondere in fortgeschrittenen Stadien, während dies bei darmtypischen Tumoren nicht der Fall war. Patienten mit geringen PRKACB-Werten in ihren Tumoren hatten eine deutlich schlechtere Gesamtüberlebenszeit, selbst nach Korrektur für andere klinische Faktoren, was darauf hindeutet, dass PRKACB in diesem Kontext als Tumorsuppressor wirkt.
Wie niedriges PRKACB das Entweichen von Zellen fördert
Um zu verstehen, was PRKACB in Krebszellen bewirkt, verwendete das Team kultivierte Zelllinien, die diffusen Magenkrebs modellieren. Wenn sie PRKACB künstlich reduzierten, wurden die Zellen in Labortests beweglicher und invasiver, drückten sich leichter durch Barrieren und bildeten fingerartige Fortsätze (Pseudopodien), die beim Kriechen helfen. Diese Zellen wechselten zudem von einem eher geordneten, epithelialen Zustand zu einem lockereren, mesenchymal-ähnlichen Zustand, der mit Metastasenbildung assoziiert ist, und verloren das Adhäsionsmolekül E‑Cadherin, das normalerweise Zellen zusammenhält. Im Gegensatz dazu machten gesteigerte PRKACB-Spiegel die Zellen weniger migratorisch und weniger invasiv. Wichtig ist, dass sich durch diese Veränderungen nicht die Teilungsrate der Zellen änderte, was auf eine spezifische Rolle von PRKACB bei der Ausbreitung, nicht beim Wachstum, hinweist.
Im Fokus: der RhoA-Signalumschalter
Die Forschenden fragten dann, wie PRKACB diesen anti-metastatischen Effekt ausübt. Mit Methoden zur Analyse von Protein‑Protein‑Interaktionen und strukturellem Modellieren zeigten sie, dass PRKACB direkt an RhoA bindet, einen molekularen Schalter, der zwischen inaktiven und aktiven Formen wechselt und damit Zellform und -bewegung steuert. PRKACB fügt RhoA an einer spezifischen Position (Serin 188) eine Phosphatgruppe hinzu, wodurch RhoA heruntergeregelt und die nachgeschalteten ROCK‑ und FAK‑Signalwege gedämpft werden, die für Umbau des Zytoskeletts und Zellmotilität verantwortlich sind. Wird PRKACB herunterreguliert, ist RhoA weniger phosphoryliert, stärker aktiv und ROCK/FAK‑Signale nehmen zu, was zu aggressiverer Zellbewegung führt. In Mausmodellen, in die humanähnliche Tumoren in die Magenwand transplantiert wurden, führte eine Verringerung von PRKACB zu mehr und größeren Metastasen in der Bauchhöhle und zu einem früheren Auftreten sichtbarer Streuungen, wiederum ohne die Wachstumsrate bereits etablierter Metastasen zu verändern.
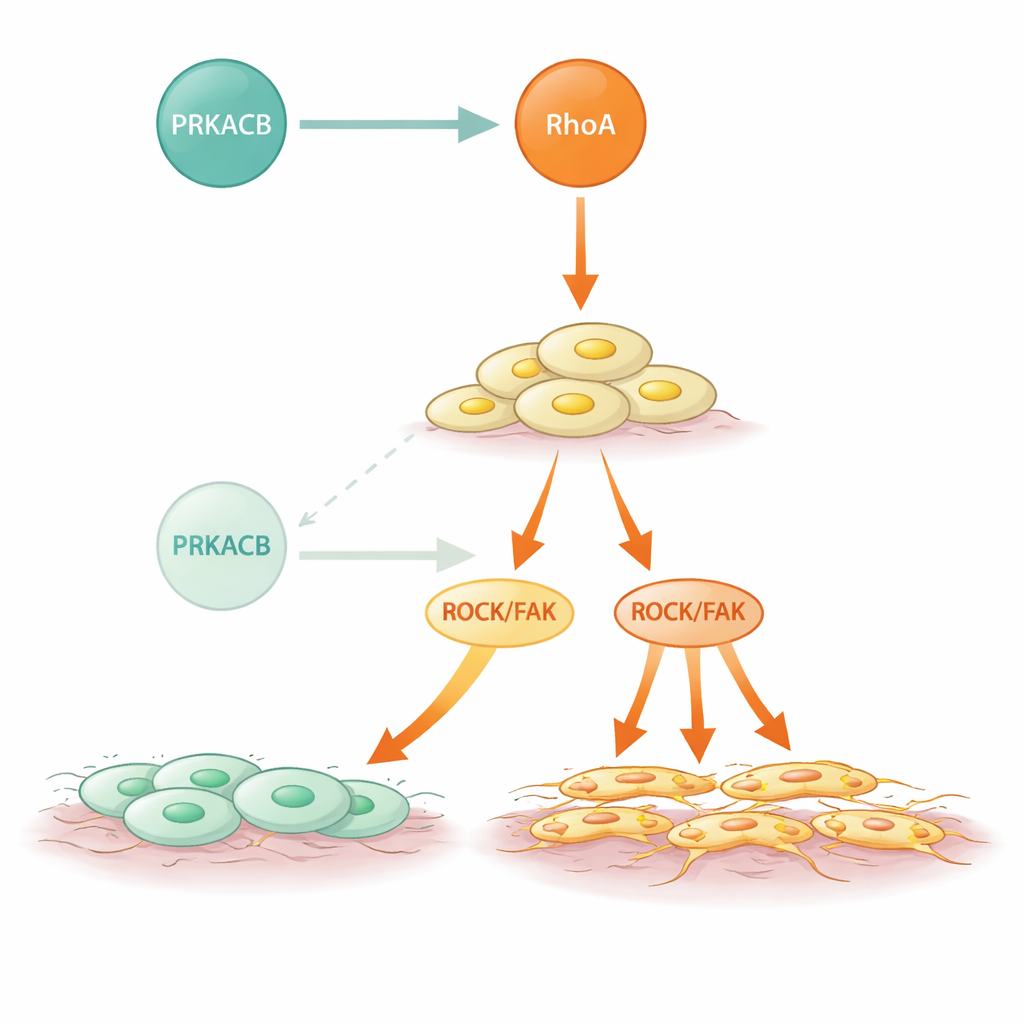
Mutierte Signalgebung und ein möglicher Eingriffspunkt
Diffuse Magenkrebse tragen oft RHOA‑Mutationen, und diese Studie zeigt, wie einige dieser Veränderungen das Problem verstärken. Mehrere häufige, mit DGC assoziierte RhoA‑Mutationen schwächten oder verhinderten dessen Bindung an PRKACB, beeinträchtigten jedoch nicht die Fähigkeit von RhoA, seine nachgeschalteten Partner zu aktivieren. Folglich entzogen sich diese mutierten Formen der einschränkenden Phosphorylierung durch PRKACB und zeigten eine erhöhte ROCK‑Aktivität und stärkeres invasives Verhalten. Auffällig war, dass die Behandlung von Zellen und Mäusen mit einem RhoA‑hemmenden Wirkstoff die durch niedrige PRKACB verursachte zusätzliche Metastasierung weitgehend umkehrte. Das deutet darauf hin, dass selbst in Tumoren, in denen die natürliche Bremse schwach oder fehlend ist, die direkte Hemmung des überaktiven RhoA‑Weges die Ausbreitung begrenzen könnte.
Was das für Patientinnen, Patienten und zukünftige Therapien bedeutet
Kurz gesagt identifiziert diese Arbeit PRKACB als zentralen Bestandteil eines inneren „Anti‑Migrations“-Kreises beim diffusen Magenkrebs. Fallen die PRKACB‑Spiegel, oder ist RhoA so mutiert, dass PRKACB nicht binden und es modifizieren kann, läuft die RhoA‑Signalgebung heißer und Krebszellen werden geschickter darin, sich zu lösen und die Bauchhöhle zu besiedeln. Die Messung von PRKACB‑ und RhoA‑Status in Tumoren könnte Ärzten helfen einzuschätzen, wie wahrscheinlich eine Metastasierung ist und wer am meisten von Wirkstoffen profitieren könnte, die den RhoA–ROCK–FAK‑Weg hemmen. Solche Therapien bedürfen zwar weiterer Entwicklung und klinischer Prüfung, doch die Studie beschreibt einen klaren molekularen Pfad von einer fehlenden Bremse zur tödlichen Ausbreitung — und zeigt neue Ansätze auf, diese Reise zu verlangsamen.
Zitation: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Schlüsselwörter: diffuser Magenkrebs, Metastasierung, PRKACB, RhoA-Signalgebung, ROCK‑FAK‑Signalweg