Clear Sky Science · de
Androgenrezeptor‑abhängige DRAM1‑Aktivierung treibt autophagische Resistenz gegen BRAF‑Inhibitoren bei BRAFV600‑mutantem Melanom voran
Warum einige Hautkrebse mächtige Medikamente überlisten
Zielgerichtete Medikamente haben die Behandlung vieler Patientinnen und Patienten mit fortgeschrittenem Melanom, einer aggressiven Form von Hautkrebs, grundlegend verändert. Doch diese Therapien hören oft nach einigen Monaten auf zu wirken, weil Tumoren sich anpassen und wieder zu wachsen beginnen. Diese Studie enthüllt einen verborgenen Überlebensmechanismus von Melanomzellen: Sie schalten einen Hormon‑Sensor an, der häufiger mit männlicher Biologie assoziiert ist, und nutzen das zelluläre Recycling‑System, um den Wirkungen der Behandlung zu entkommen. Das Verständnis dieser Ausweichroute könnte den Weg zu klügeren Medikamentenkombinationen öffnen, die das Krebswachstum länger unter Kontrolle halten.
Ein genauerer Blick auf medikamentenresistente Melanome
Etwa die Hälfte der Melanome trägt eine spezifische DNA‑Veränderung im Gen BRAF, die das Tumorwachstum beschleunigt. Medikamente, die BRAF blockieren, oft kombiniert mit MEK‑Inhibitoren, können diese Tumoren dramatisch verkleinern. Leider tritt die Erkrankung bei vielen Patientinnen und Patienten innerhalb von zwei Jahren wieder auf. Ärztinnen und Ärzte haben außerdem beobachtet, dass Männer tendenziell schlechter auf diese Medikamente ansprechen als Frauen, was Fragen zur Rolle geschlechtsbezogener Hormone und ihrer Rezeptoren bei der Resistenz aufwirft.
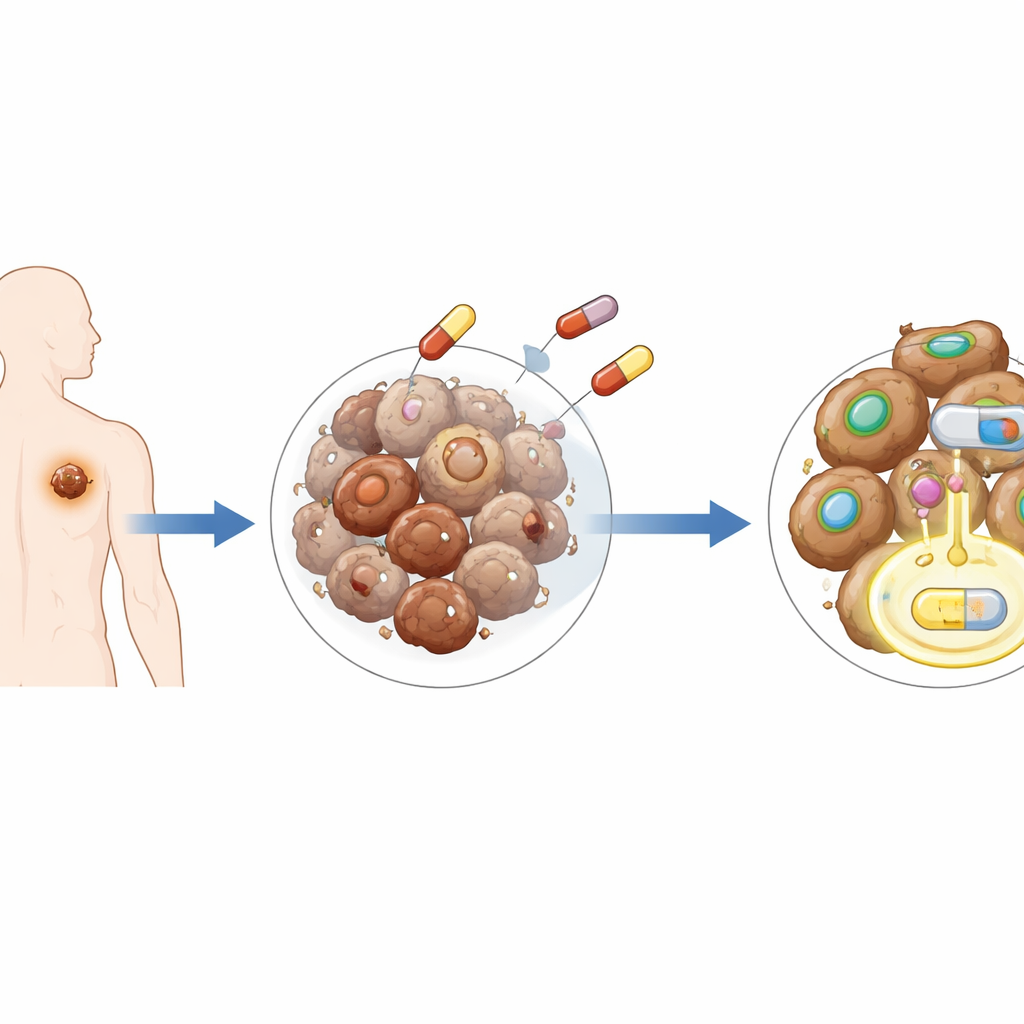
Ein männlicher Hormon‑Sensor rückt ins Rampenlicht
Die Forschenden konzentrierten sich auf den Androgenrezeptor, ein intrazelluläres Protein, das normalerweise auf männliche Sexualhormone wie Testosteron reagiert. Obwohl Melanom kein klassischer „hormongetriebener“ Krebs ist, zeigte frühere Arbeit, dass dieser Rezeptor Melanomzellen aggressiver machen kann. In dieser Studie setzten die Forschenden mehrere Melanomzelllinien BRAF‑ und MEK‑Inhibitoren aus und fanden heraus, dass die Medikamente selbst die Rezeptorproduktion in den Zellen erhöhten, unabhängig davon, ob der ursprüngliche Tumor von einem männlichen oder weiblichen Patienten stammte. Zellen, die so verändert wurden, dass sie zusätzliche Kopien dieses Rezeptors tragen, überlebten BRAF‑Blocker deutlich besser und bildeten mehr Kolonien, während Tumorproben von Patientinnen und Patienten nach der Behandlung höhere Rezeptorwerte zeigten als Proben derselben Personen vor der Therapie.
Aktivierung des zellulären Recycling‑ und Reinigungssystems
Das Team fragte dann, wie der Androgenrezeptor Melanomzellen hilft, die Behandlung zu überstehen. Im Fokus stand die Autophagie, der eingebaute Reinigungs‑ und Recyclingprozess der Zelle, der je nach Kontext entweder zum Zelltod beitragen oder Zellen helfen kann, Stress zu überstehen. Mit Mikroskopie, fluoreszenten Reportern und Proteinmarkern zeigten sie, dass eine Erhöhung des Androgenrezeptors in Melanomzellen die Bildung und den Umsatz der kleinen Bläschen und Verdauungskompartimente, die die Autophagie durchführen, stark steigerte. Die Blockade dieses Recyclingwegs mit einem chemischen Inhibitor machte rezeptorreiche Zellen deutlich empfindlicher gegenüber BRAF‑Blockern, während die Aktivierung der Autophagie Zellen, in denen der Rezeptor ausgeschaltet worden war, teilweise rettete. Zusammen zeigen diese Experimente, dass der Rezeptor die Medikamentenresistenz fördert, indem er eine schützende Form der zellulären Selbstreinigung hochfährt.
Ein wichtiger Schalter namens DRAM1 verbindet Hormone mit Recycling
Um herauszufinden, welche Gene den Androgenrezeptor mit der Recycling‑Maschinerie verbinden, durchsuchten die Forschenden mehrere große Expressionsdatensätze. Ein Gen, DRAM1, stach hervor: Es wurde stark durch den Rezeptor induziert und war in Zellen und Tumoren, die BRAF‑Inhibitoren ausgesetzt waren, beständig erhöht. DRAM1 kodiert für ein Protein, das in den Membranen von Recycling‑ und Verdauungskompartimenten innerhalb der Zelle eingebettet ist. Wenn das Team Melanomzellen dazu brachte, mehr DRAM1 zu produzieren, stieg die Autophagie; wenn sie die DRAM1‑Spiegel senkten, nahmen sowohl Autophagie als auch Medikamentenresistenz ab. Sie zeigten außerdem, dass der Androgenrezeptor direkt an spezifische Kontrollsequenzen im DRAM1‑Gen bindet und es einschaltet, wodurch eine klare Kette von der Medikamentenexposition über die Rezeptorsteigerung zur DRAM1‑Aktivierung und verstärktem Recycling etabliert wird.
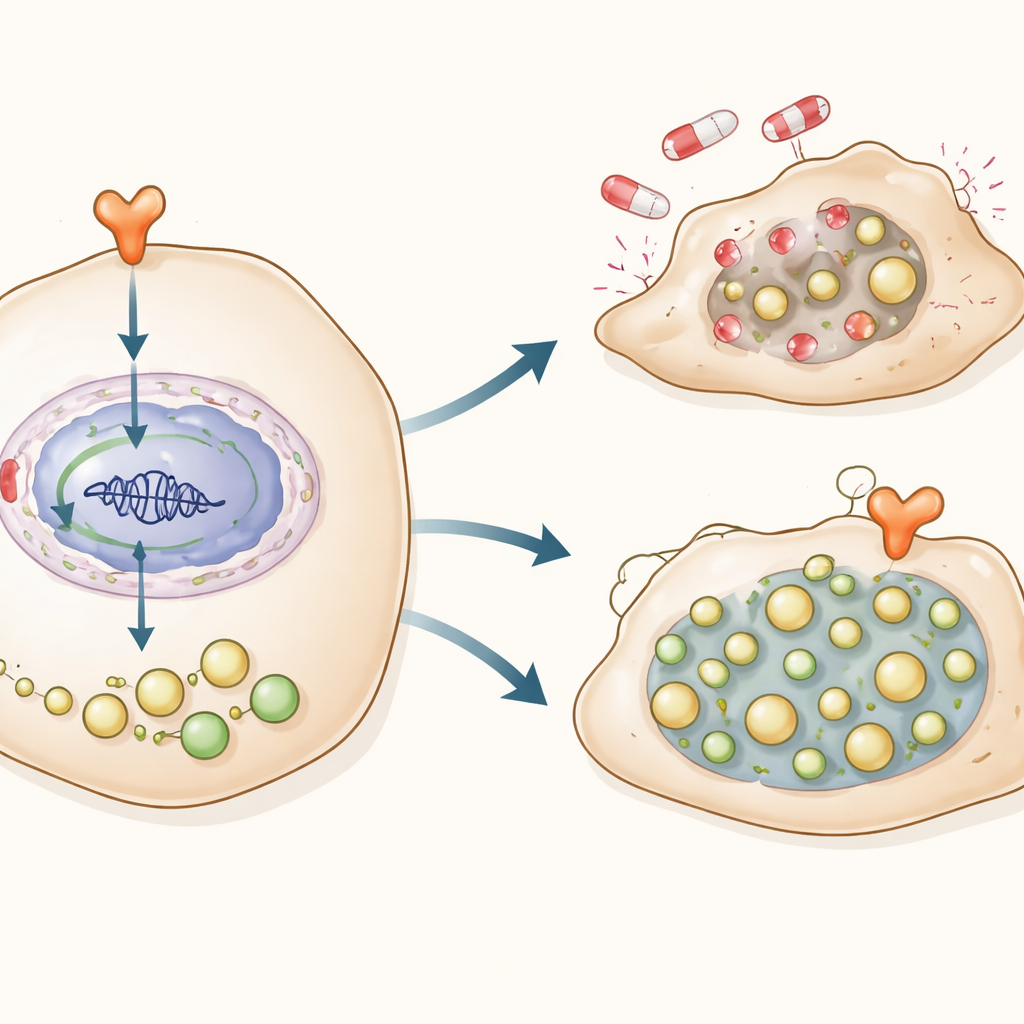
Zwei Schläge kombinieren, um die Flucht des Krebses zu blockieren
Weil diese Hormon‑Recycling‑Achse zentral für die Resistenz zu sein schien, prüften die Wissenschaftlerinnen und Wissenschaftler, ob die gleichzeitige Blockade beider Arme besonders effektiv wäre. In Zellkulturen behandelten sie BRAF‑resistente Melanomzellen mit einem modernen Degrader‑Wirkstoff (ARV110), der den Androgenrezeptor entfernt, zusammen mit einem Autophagie‑Inhibitor. Die Kombination reduzierte das Überleben resistenter Zellen deutlich stärker als eines der beiden Medikamente allein. In Mäusen mit resistenten menschlichen Melanomtumoren verkleinerte dieselbe Doppelbehandlung die Tumoren stärker und verlangsamte ihr Wachstum länger, ohne offensichtliche Schäden an wichtigen Organen oder Gewichtsverlust. Tumoren aus behandelten Mäusen zeigten reduzierte Spiegel des Rezeptors, von DRAM1 und von Recycling‑Markern, was bestätigte, dass der Weg erfolgreich abgeschaltet worden war.
Was das für Menschen mit Melanom bedeutet
Diese Ergebnisse zeigen, dass BRAF‑gerichtete Therapien unbeabsichtigt einen männlichen Hormon‑Sensor in Melanomzellen aktivieren können, der dann über DRAM1 ein Recyclingprogramm einschaltet, das den Tumoren beim Überleben hilft. Für Laien ist das vergleichbar damit, dem Krebs ein starkes Medikament zu geben, während der Tumor heimlich ein besseres Abfallverarbeitungs‑ und Reparatursystem aufbaut, das ihm erlaubt, den Angriff zu überdauern. Indem man gleichzeitig den Hormon‑Sensor und die Recycling‑Maschinerie abschneidet, konnten die Forschenden resistente Tumoren in präklinischen Modellen wieder verwundbar machen. Zwar sind weitere Studien nötig, um Sicherheit und Nutzen beim Menschen zu bestätigen, doch deutet diese Arbeit darauf hin, dass sorgfältig gestaltete Kombinationen, die Hormonsignalgebung und zelluläres Recycling gezielt angreifen, eines Tages die Wirksamkeit und Dauer aktueller Melanomtherapien verlängern könnten.
Zitation: Zhi, D., Wu, B., Yang, J. et al. Androgen receptor-dependent DRAM1 activation drives autophagic resistance to BRAF inhibitors in BRAFV600-mutant melanoma. Cell Death Dis 17, 265 (2026). https://doi.org/10.1038/s41419-026-08547-x
Schlüsselwörter: Melanom, Arzneimittelresistenz, Androgenrezeptor, Autophagie, BRAF‑Inhibitoren