Clear Sky Science · de
Achse aus langem nicht-kodierendem RNA ADEI/miR-93-3p/STAT3 fördert das Fortschreiten und die Immunflucht bei Epstein-Barr-Virus-positivem diffus großzelligem B-Zell-Lymphom durch Regulierung des PD-1/PD-L1-Checkpoints
Warum das für unsere Immunabwehr wichtig ist
Einige mit dem weitverbreiteten Epstein-Barr-Virus (EBV) verbundene Lymphome sind ungewöhnlich schwer zu behandeln und entziehen sich oft der Immunabwehr des Körpers. Diese Studie deckt ein verborgenes Nachrichtensystem in diesen Tumoren auf: winzige Bläschen, Exosomen genannt, die ein langes RNA-Molekül transportieren, das Tumoren beim Wachsen hilft und sie vor Immunzellen verbirgt. Das Verständnis dieses verdeckten Austauschs könnte neue Wege eröffnen, diese hartnäckigen Blutkrebsarten zu diagnostizieren und zu behandeln.
Ein Virus, das das Gleichgewicht verschiebt
Das diffusen großzellige B-Zell-Lymphom (DLBCL) ist das häufigste aggressive Lymphom. Tragen Tumorzellen EBV, sprechen Patienten tendenziell schlechter auf die Standard-Chemoimmuntherapie an. Die Forschenden verglichen zunächst im Labor EBV-positive und EBV-negative Lymphomzellen. Sie stellten fest, dass EBV-Infektion die Lymphomzellen schneller teilen ließ, mehr Kolonien bildeten und größere Tumoren in Mäusen erzeugten. EBV-positive Zellen zeigten außerdem mehr eines Oberflächenmoleküls namens PD-L1, das mit PD-1 auf Immunzellen interagiert, um deren Angriff abzuschalten. Wenn das Team Lymphomzellen mit zytotoxischen CD8-T-Zellen mischte, verringerten EBV-positive Tumoren sowohl Anzahl als auch Wirksamkeit dieser T-Zellen — ein Effekt, der mit Antikörpern gegen den PD-1/PD-L1-Bremse umkehrbar war.
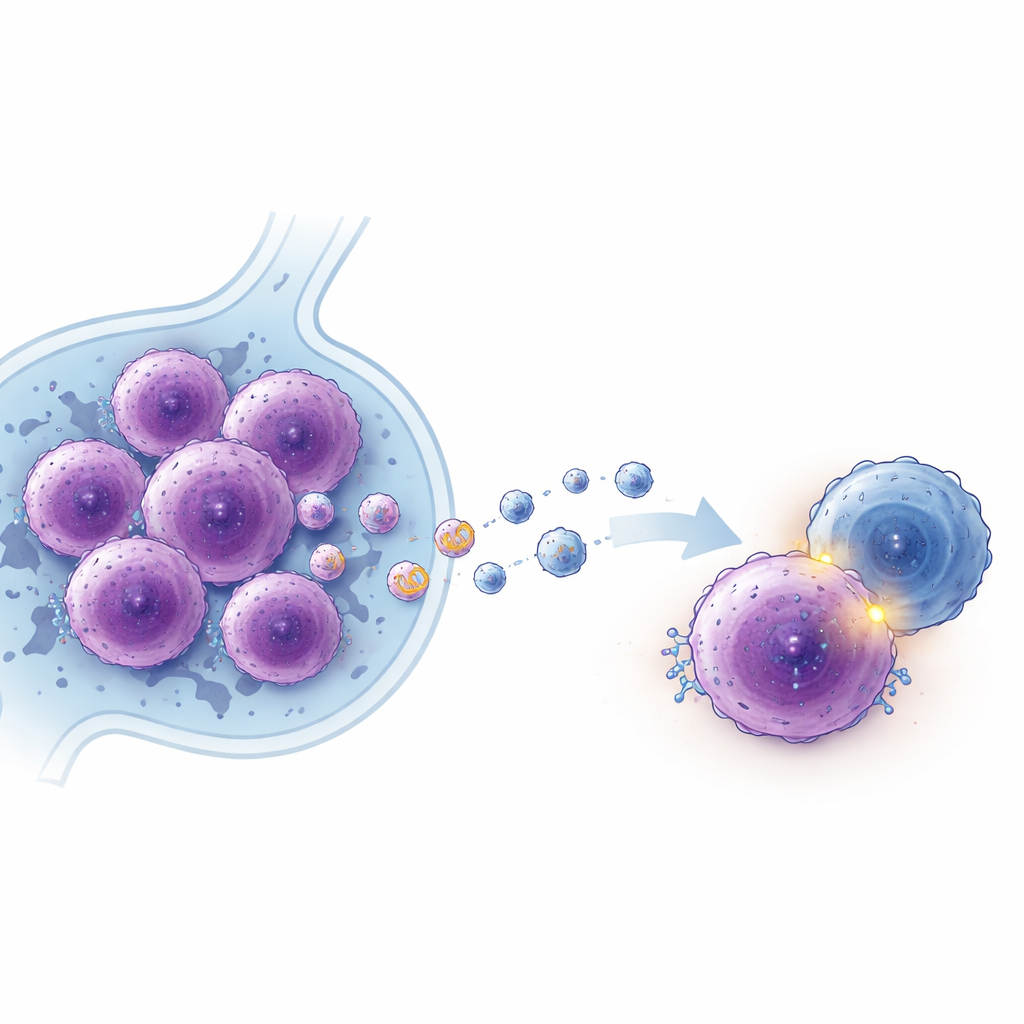
Eine lange RNA, die Tumoren Wachstum und Verstecken ermöglicht
Um zu verstehen, wie EBV das Tumorverhalten umprogrammiert, untersuchte das Team lange nicht-kodierende RNAs — RNA-Abschnitte, die keine Proteine herstellen, aber viele Zellprozesse regulieren können. Beim Durchsehen des RNA-Gehalts von Exosomen, die von EBV-positiven und EBV-negativen DLBCL-Zellen freigesetzt wurden, entdeckten sie eine zuvor uncharakterisierte RNA, die sie lncADEI nannten und die in EBV-positiven Zellen und deren Exosomen stark erhöht war. Wenn sie Lymphomzellen dazu brachten, mehr lncADEI zu produzieren, teilten sich die Zellen schneller, bildeten mehr Kolonien und widerstanden dem programmierten Zelltod. Die Reduktion von lncADEI hatte den gegenteiligen Effekt: verlangsamtes Wachstum und erhöhte Zellsterblichkeit sowohl in Zellkulturen als auch in Maus-Tumormodellen.
Wie lncADEI die Immunflucht umprogrammiert
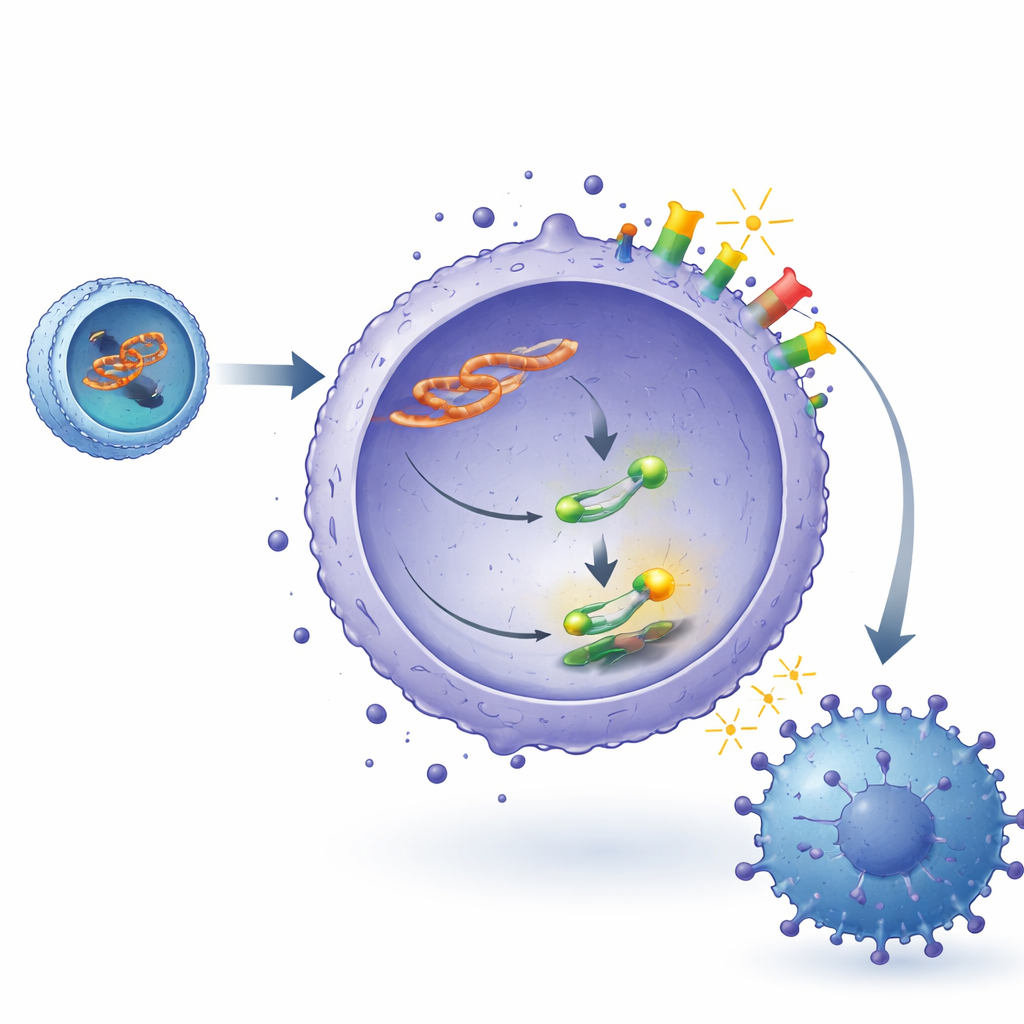
Die Forschenden verfolgten dann, wie lncADEI mit dem PD-1/PD-L1-Immuncheckpoint verbunden ist. Innerhalb der Lymphomzellen liegt lncADEI vorwiegend im Zytoplasma, wo es wie ein Schwamm für eine kleine regulatorische RNA namens miR-93-3p wirkt. Unter normalen Bedingungen hilft miR-93-3p, ein zentrales Signalmolekül, STAT3, in Schach zu halten, indem es dessen Botschaft bindet und die Produktion einschränkt. Wenn lncADEI miR-93-3p aufsaugt, wird mehr STAT3 hergestellt und aktiviert. STAT3 bindet wiederum direkt an die Kontrollregion des PD-L1-Gens in Lymphomzellen und steigert die PD-L1-Produktion. Diese Kette — lncADEI, das miR-93-3p blockiert, STAT3 freisetzt und PD-L1 antreibt — führt zu höherer PD-L1-Expression auf Tumorzellen, stärkeren Abschaltsignalen gegenüber CD8-T-Zellen und verringerter T-Zell-Aktivität.
Exosom-„Post“, die schädliche Instruktionen verbreitet
EBV-positive Lymphomzellen behalten lncADEI nicht für sich. Sie sezernieren deutlich mehr Exosomen als EBV-negative Zellen, und diese Exosomen sind mit lncADEI beladen. Wurden EBV-negative Lymphomzellen Exosomen von EBV-positiven Zellen ausgesetzt, nahmen sie diese auf, ihre internen lncADEI-Spiegel stiegen, und sie begannen, sich aggressiver zu verhalten — sie teilten sich schneller und bildeten mehr Kolonien. In gemischten Kulturen, die T-Zellen einschlossen, reduzierten lncADEI-angereicherte Exosomen die Zahl und die Abtötungskraft von CD8-T-Zellen und erhöhten PD-1 auf diesen Immunzellen, was die Immunantwort weiter schwächte. Das deutet darauf hin, dass EBV-positive Tumoren benachbarte Tumorzellen „umprogrammieren“ und ihr Umfeld durch lncADEI-reiche Exosomen umgestalten können.
Hinweise aus Patientenblutproben
Um die Laborbefunde mit der realen Krankheit zu verknüpfen, maßen die Forschenden lncADEI in Blutexosomen von 47 DLBCL-Patienten. Diejenigen mit EBV-positiven Tumoren hatten signifikant höhere Spiegel an exosomalem lncADEI als EBV-negative Patienten. Hohe lncADEI-Werte im Blut waren außerdem mit einem fortgeschritteneren Krankheitsstadium, einem aggressiveren Tumorsubtyp, höheren Standardrisikowerten und erhöhten Markern für Gewebeschädigung assoziiert. Diese Muster legen nahe, dass exosomales lncADEI im Blut als minimalinvasiver Indikator für EBV-getriebenes Lymphom und dessen Schwere dienen könnte.
Was das für die künftige Versorgung bedeutet
Kurz gesagt zeigt diese Arbeit einen dreistufigen Trick, den EBV-verbundene Lymphome anwenden: Sie überproduzieren eine lange RNA (lncADEI), verpacken sie in reisende Bläschen und nutzen sie sowohl innerhalb des Tumors als auch in benachbarten Zellen, um eine bekannte Immunbremse, PD-L1, hochzufahren. Das Ergebnis ist schnelleres Tumorwachstum und gedämpfte T-Zell-Angriffe. Da jeder Schritt dieser Kette — lncADEI selbst, seine Interaktion mit miR-93-3p und STAT3 sowie die Freisetzung lncADEI-reicher Exosomen — einen möglichen Interventions- oder Messpunkt bietet, weist die Studie auf neue Strategien hin, um die Immuntherapie zu verbessern und EBV-assoziierte Lymphome mit einem einfachen Bluttest zu überwachen.
Zitation: Zheng, W., Lai, G., Liao, Z. et al. Long noncoding RNA ADEI/miR-93-3p/STAT3 axis promotes Epstein–Barr virus-positive diffuse large B-cell lymphoma progression and immune evasion through regulating the PD-1/PD-L1 checkpoint. Cell Death Dis 17, 280 (2026). https://doi.org/10.1038/s41419-026-08532-4
Schlüsselwörter: Epstein-Barr-Virus-Lymphom, Immuncheckpoint, lange nicht-kodierende RNA, Exosomen, STAT3-Signalweg