Clear Sky Science · de
Leptin‑LEPR-Signale im Knochenmark stellen die mitochondriale oxidative Stoffwechselwelt um und verleihen Chemoresistenz bei akuter myeloischer Leukämie
Warum Fett im Knochenmark für die Leukämiebehandlung wichtig ist
Viele Menschen wissen, dass Körperfett Krankheiten wie Diabetes oder Herzkrankheiten beeinflussen kann; nur wenige ahnen jedoch, dass Fett, das in unseren Knochen verborgen liegt, ebenfalls beeinflussen kann, wie Blutkrebserkrankungen auf Therapien reagieren. Diese Studie untersucht, wie ein von Fettzellen produziertes Hormon, das Leptin, akute myeloische Leukämiezellen vor Standardchemotherapien schützt. Das Verständnis dieses verborgenen Schutzmechanismus könnte auf neue Wege hinweisen, bestehende Medikamente für Patientinnen und Patienten wirksamer zu machen.
Ein Hormon, das die Chancen gegen Chemotherapie verschiebt
Die Forschenden begannen mit Untersuchungen von Knochenmarkproben von Erwachsenen mit neu diagnostizierter AML. Sie bestimmten die Leptinspiegel im Mark und prüften, wie gut Patientinnen und Patienten die Leukämiezellen nach einer Behandlung mit dem häufig eingesetzten Chemotherapeutikum Cytarabin eliminieren konnten. Patienten mit höheren Leptinspiegeln im Knochenmark und höheren Mengen seines Rezeptors auf Leukämiezellen sprachen seltener auf die Behandlung an und hatten eine kürzere Überlebenszeit. Selbst nach Berücksichtigung anderer Risikofaktoren blieb Leptin ein starker Indikator für eine schlechte Chemotherapieantwort. Das deutete darauf hin, dass das von Fett stammende Hormon mehr war als nur ein Spiegel der Krankheitslast; es stand in aktivem Zusammenhang mit Resistenz.
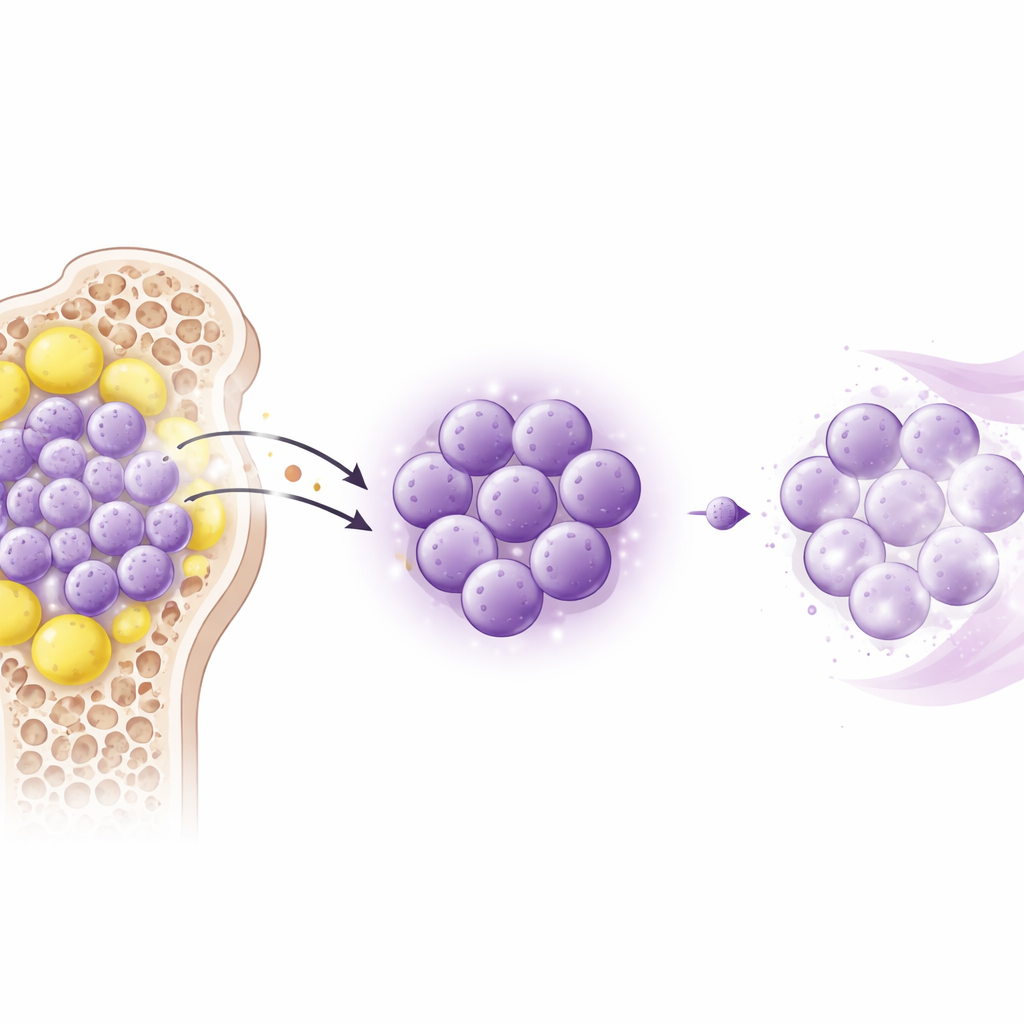
Tiermodelle zeigen einen verborgenen Schutz
Um zu prüfen, ob Leptin tatsächlich Arzneimittelresistenz verursacht, nutzte das Team zwei Mausmodelle der AML, die die menschliche Erkrankung gut nachbilden. Die Mäuse erhielten Cytarabin allein, Cytarabin plus zusätzliches Leptin oder Cytarabin zusammen mit einem kleinen Peptid, das den Leptinrezeptor blockiert. Die Zugabe von Leptin verkürzte das Überleben, vergrößerte Milz und Leber und erlaubte den Leukämiezellen, diese Organe trotz Chemotherapie zu fluten. Im Gegensatz dazu verlangsamte das Blockieren des Rezeptors allein nicht das Leukämiewachstum, verstärkte aber deutlich die Wirkung von Cytarabin, verkleinerte die befallenen Organe und reduzierte die Leukämielast. Diese Befunde zeigen, dass Leptins Hauptwirkung nicht darin besteht, das Krebswachstum direkt zu beschleunigen, sondern Leukämiezellen schwerer tödlich zu machen, wenn Chemotherapie angewendet wird.
Aufladung der Energiezentralen der Zelle
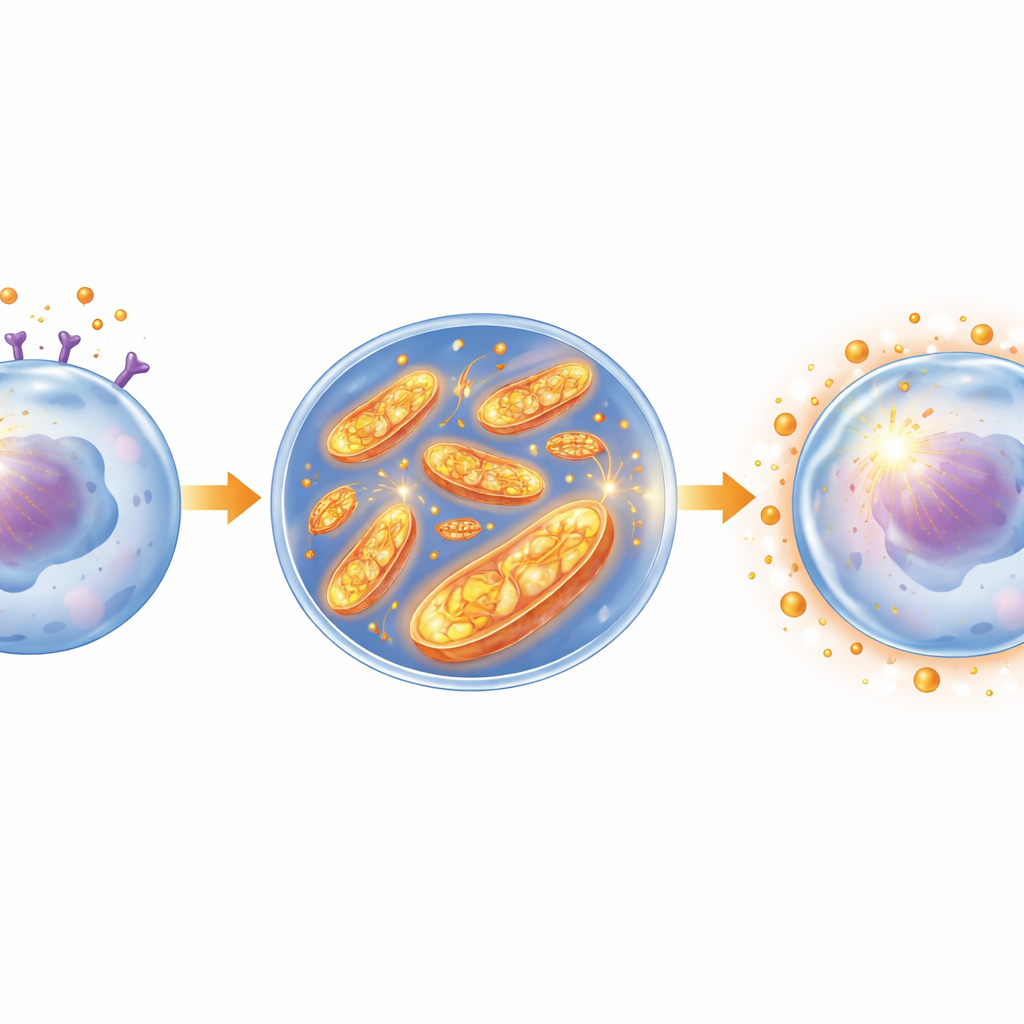
Vertiefende Untersuchungen zeigten, wie Leptin den Stoffwechsel von Leukämiezellen verändert. Man fand heraus, dass Leptin eine Signalkette im Inneren der Zelle aktiviert, bekannt als JAK2/STAT3, die ihrerseits die Mitochondrien – die winzigen Kraftwerke zur Energieproduktion – hochfährt. Sowohl in Maus-Leukämiezellen als auch in humanen AML-Zelllinien erhöhte Leptin die Aktivität einer wichtigen mitochondrialen Komponente, dem Komplex I, und steigerte den gesamten oxidativen Stoffwechsel. Dieser Umbau erzeugte mehr reaktive Sauerstoffspezies innerhalb der Mitochondrien. Paradoxerweise schädigten diese reaktiven Moleküle die Zellen nicht direkt, sondern lösten eine Anpassungsantwort aus: Die Leukämiezellen bauten ihre antioxidativen Abwehrmechanismen wie Glutathion und entgiftende Enzyme hoch und schufen so einen wirksamen inneren Schutzschild.
Wenn Stress zur Rüstung wird
Das Team zeigte, dass dieser Schutzschild zentral für die Chemoresistenz ist. Mit Leptin behandelte Leukämiezellen wiesen eine höhere gesamte antioxidative Kapazität auf und waren weniger anfällig für Cytarabin und ein weiteres Medikament, Daunorubicin. Die Entfernung des Leptinrezeptors mittels Geneditierung schwächte dieses antioxidative Netzwerk, senkte die Spiegel schützender Moleküle und machte die Zellen deutlich empfindlicher gegenüber der Behandlung, selbst ohne zusätzliches Leptin. Weitere Experimente bestätigten, dass ein scharfer Ausbruch mitochondrialen Stresses ebenfalls ein ähnliches Schutzprogramm auslösen kann, während das Beseitigen dieser reaktiven Moleküle den Schild zerstörte und die Medikamentenempfindlichkeit wiederherstellte. Wichtig ist, dass das Blockieren der JAK2/STAT3-Signalkaskade oder des Leptinrezeptors selbst die Aktivierung von Komplex I verhinderte, mitochondriale Stresssignale reduzierte, die antioxidative Barriere zum Einsturz brachte und die Chemotherapie wieder wirksam machte.
Eine Schwäche als neuer Behandlungsansatz
Für Patientinnen und Patienten lautet die Botschaft der Studie, dass Leukämiezellen ein von benachbarten Fettzellen gebildetes Hormon ausnutzen können, um eine Chemotherapie zu überstehen. Leptin aus dem Knochenmarkfett bindet an seinen Rezeptor auf Leukämiezellen, stellt deren Mitochondrien auf Hochleistungsbetrieb um und nutzt den dabei entstehenden Niedrig-Level-Stress, um ein antioxidatives Sicherheitsnetz zu aktivieren. Dieses Netz schützt die Zellen vor den härteren Schäden, die Krebsmedikamente verursachen. Durch das Blockieren des Leptinrezeptors oder seiner nachgeschalteten Signalwege könnten Ärztinnen und Ärzte eines Tages diesen Schutz entziehen und bestehenden Chemotherapien wieder ihre volle Wirkung verleihen, ohne zwangsläufig die Dosis zu erhöhen. Auf diese Weise könnte ein besseres Verständnis der Kommunikation zwischen Knochenmarkfett und Leukämiezellen direkt in langlebigere Remissionen für Menschen mit AML übersetzt werden.
Zitation: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
Schlüsselwörter: akute myeloische Leukämie, Leptin, Chemoresistenz, Mitochondrien, oxidativer Stress