Clear Sky Science · de
ISGylierung verhindert die autophagische Degradation von STING und fördert die antitumorale Immunität bei Lungenkrebs
Warum es für Lungenkrebs wichtig ist, einen zellulären Alarm zu schützen
Unser Immunsystem besitzt winzige Alarmschalter, die den Körper warnen können, wenn etwas nicht stimmt — etwa bei einer Virusinfektion oder einem wachsenden Tumor. Einer dieser Alarme, STING genannt, hilft dabei, ruhende Tumoren in Ziele zu verwandeln, die das Immunsystem angreifen kann. In vielen Lungenkrebserkrankungen nimmt die Menge an STING in Tumorzellen jedoch im Laufe der Zeit ab, was die Wirksamkeit neuer Krebsmedikamente, die diesen Alarm aktivieren sollen, abschwächen kann. Diese Studie zeigt, warum STING verschwindet, und beschreibt einen Weg, es stabil zu halten, wodurch sich ein Ansatz ergibt, die Immuntherapie bei Patientinnen und Patienten zu verbessern, deren Tumoren derzeit schlecht ansprechen.
Wie Zellen interne Gefahrensignale erkennen
Wenn DNA-Fragmente an Orten innerhalb einer Zelle auftreten, an denen sie nicht hingehören, deutet das häufig auf eine Virusinfektion oder auf geschädigte Krebszellen hin. Die Zelle nutzt ein Erkennungssystem, den cGAS–STING-Signalweg, um diese fehlplatzierten DNA-Fragmente zu erkennen. Nach Aktivierung löst STING eine Signalkaskade aus, die zur Produktion von Typ‑I‑Interferonen führt — potente immunologische Botenstoffe. Diese Botenstoffe mobilisieren verschiedene Abwehrzellen, darunter natürliche Killerzellen und zytotoxische T‑Zellen, um infizierte oder maligne Zellen anzugreifen. In vielen Tumoren, besonders in fortgeschrittenen Lungenkrebsarten, sind die STING‑Spiegel jedoch ungewöhnlich niedrig, was dieses interne Alarmsystem schwächt und den Krebszellen hilft, sich zu verbergen.
Ein schützender Markierer, der STING bewahrt
Proteine in Zellen werden ständig markiert, transportiert und abgebaut. Die Autorinnen und Autoren konzentrierten sich auf eine spezielle Form einer molekularen Markierung namens ISGylierung, bei der ein kleines Protein, ISG15, an andere Proteine angehängt wird. Sie fanden heraus, dass das Anhängen von ISG15 an STING an vier bestimmten Positionen wie ein Schutzschild wirkt. Dieser Schutz verhindert, dass STING vom zellulären Recycling‑Apparat verschlungen wird — einem selbstreinigenden Prozess namens Autophagie, der normalerweise dabei hilft, gebrauchte oder überschüssige Komponenten zu entsorgen. In Lungenkrebszellen wird STING schneller entfernt, wenn es diese ISG15‑Markierungen nicht erhält; das Alarmsignal verblasst und die nachgeschaltete Immunantwort — einschließlich der Interferonproduktion — nimmt deutlich ab. 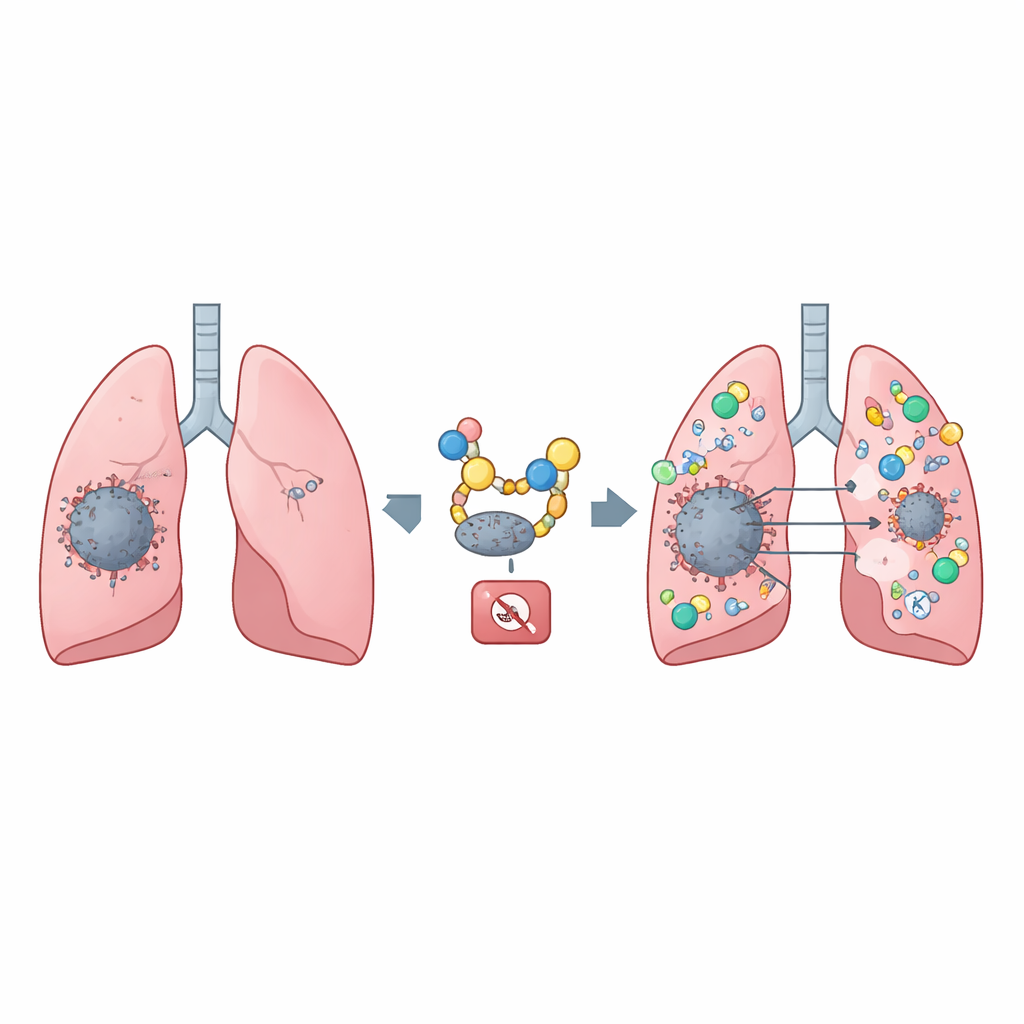
Den zellulären Schredder blockieren
Das Team untersuchte anschließend, welche Moleküle diesen Schutzmarker entfernen. Sie identifizierten ein Enzym, USP18, das ISG15 von STING abtrennt und es somit der autophagischen Zerstörung ausliefert. In Zellexperimenten und Mausmodellen für Lungenkrebs führten höhere USP18‑Spiegel zu weniger STING, reduzierter Infiltration von Immunzellen in Tumoren und schnellerem Tumorwachstum. Analysen menschlicher Lungenkrebsproben zeigten ein ähnliches Bild: USP18 war in Tumoren häufig erhöht, während STING vermindert war, und Patientinnen und Patienten mit höheren USP18‑Werten hatten tendenziell eine schlechtere Überlebensprognose. Diese Muster deuten darauf hin, dass USP18 wie ein zellulärer Schredder‑Schalter wirkt und den STING‑Alarm zur Unzeit dämpft.
Eine Wirkstoffkombination, die den Immunangriff verstärkt
Da Enzyme wie USP18 durch kleine Moleküle blockiert werden können, screente die Gruppe tausende Verbindungen und identifizierte Tanshinon IIA‑sulfonat (TST) als direkten USP18‑Inhibitor. Im Labor verhinderte TST, dass USP18 ISG15 von STING abspaltet, verlängerte die Lebensdauer von STING in Zellen und verstärkte seine Signalübertragung. In Mäusen mit Lungenmetastasen verlangsamte TST das Tumorwachstum. Als die Forschenden TST mit einem separaten Wirkstoff kombinierten, der STING direkt aktiviert — dem diABZi — war der Effekt beeindruckend: Die Tumoren schrumpften stärker, und Immunzellen — insbesondere natürliche Killerzellen und zytotoxische T‑Zellen — strömten vermehrt in den Tumor. Diese Kombination erzeugte einen stärkeren und länger anhaltenden Immunangriff als jede Behandlung für sich allein. 
Was das für die zukünftige Behandlung von Lungenkrebs bedeutet
Kurz gesagt: Diese Arbeit zeigt, dass Lungentumoren einen wichtigen internen Alarm, STING, oft nicht nur durch verringerte Produktion, sondern auch durch beschleunigten Abbau zum Schweigen bringen. Der natürliche Schutzmarker ISG15 bewahrt STING davor, ins zelluläre Recycling eingesogen zu werden, während USP18 diesen Marker entfernt und so den Verlust von STING fördert. Indem die Studie ein Medikament identifiziert, das USP18 blockiert und STING bewahrt, und dieses mit einem STING‑aktivierenden Wirkstoff kombiniert, skizziert sie eine Strategie, ruhige, STING‑arme Tumoren in für das Immunsystem gut sichtbare Ziele zu verwandeln. Für Patientinnen und Patienten, deren Tumoren derzeit nicht auf STING‑basierte Therapien ansprechen, könnte die Stabilisierung von STING den Unterschied zwischen einer schwachen Reaktion und einem starken, dauerhaften antitumoralen Angriff ausmachen.
Zitation: Cao, D., Huang, B., Fu, X. et al. ISGylation prevents autophagic degradation of STING and promotes antitumor immunity in lung cancer. Cell Death Dis 17, 271 (2026). https://doi.org/10.1038/s41419-026-08527-1
Schlüsselwörter: STING-Signalweg, ISGylierung, Immuntherapie bei Lungenkrebs, USP18-Inhibition, Autophagie