Clear Sky Science · de
Kern-Myosin 1 verbindet genomische Architektur mit Umbau des Fettgewebes, metabolischer Entzündung und Fettleibigkeit bei Mäusen
Warum das Zellskelett für Körperfett wichtig ist
Fettleibigkeit wird oft dem, was wir essen, und unserer Bewegung zugeschrieben. Doch tief in unseren Zellen kann auch die Art, wie DNA verpackt und abgelesen wird, das Gleichgewicht verschieben. Diese Studie zeigt, dass ein winziges Motorprotein, das nukleäre Myosin 1 (NM1), das bei der Organisation der DNA im Zellkern hilft, eine überraschende Rolle dabei spielt, wie Fettzellen entstehen, Energie speichern und Entzündungen auslösen. An Mäusen ohne dieses Protein fanden die Forschenden einen direkten Zusammenhang zwischen der physischen Architektur unserer Gene und der Entwicklung ungesunden viszeralen Fetts sowie metabolischer Probleme.
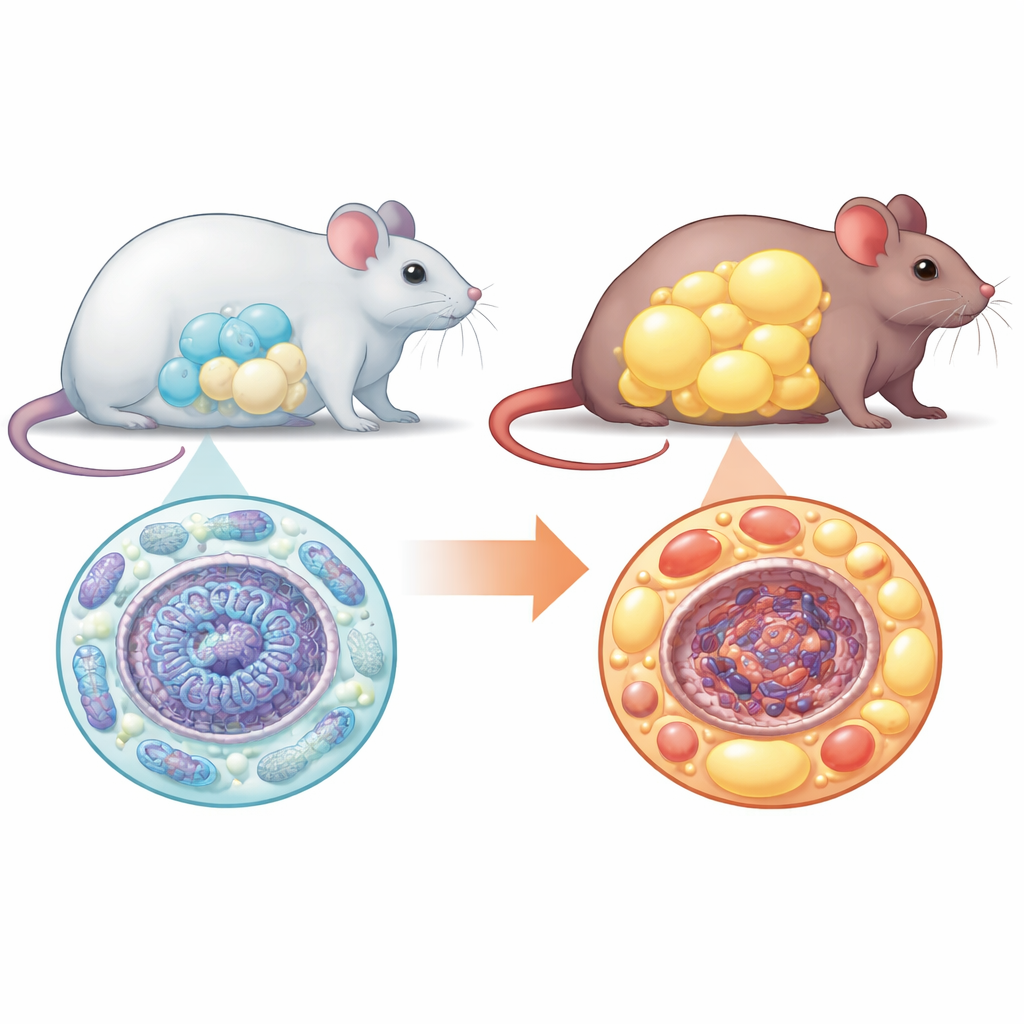
Von Stammzellen zu Fettzellen
Fettzellen entwickeln sich aus vielseitigen Vorläufern, den mesenchymalen Stammzellen. Normalerweise teilen sich diese Vorläufer, stellen ihren Energiehaushalt um und reifen zu vielen kleinen, gut funktionierenden Fettzellen heran, die überschüssige Kalorien sicher speichern. Das Team stellte fest, dass dieser geordnete Prozess ohne NM1 zusammenbricht. Wenn sie Stammzellen von normalen und NM1-defizienten Mäusen im Labor kultivierten und zur Adipogenese anregten, schlossen deutlich weniger Zellen die Umwandlung ohne NM1 ab. Die Zellen, die ausreiften, waren auffällig größer als normal, prall mit Fett gefüllt und zeigten auf Gen- und Proteinebene nicht die üblichen Kennzeichen gesunder Fettzellen. Dieses Muster – weniger Zellen, aber jede einzelne vergrößert – ist ein Kennzeichen ungesunden Fettgewebes.
Wie die Genverpackung das Verhalten von Fettzellen prägt
NM1 wirkt im Zellkern, wo es hilft, DNA-Abschnitte zugänglich zu halten, sodass wichtige Gene eingeschaltet werden können. Um zu verstehen, wie sein Verlust das Zellverhalten ändert, überlagerten die Forschenden Karten offener DNA-Regionen mit Messungen der Genaktivität in Zellen mit und ohne NM1. Sie beobachteten, dass viele Gene, die für Fettzellbildung, den Umgang mit Fetttröpfchen und die Erhaltung der Mitochondrien nötig sind, sowohl an Zugänglichkeit als auch an Aktivität verloren, wenn NM1 fehlte. Gleichzeitig wurden andere Gene, die mit Wachstums- und Signalwegen verbunden sind, offener und aktiver. Das weist NM1 als einen wichtigen Verkehrslotsen aus: Es trägt dazu bei, eine ausgewogene Landschaft offener und geschlossener DNA-Regionen zu erhalten, damit die richtigen Gen-Netzwerke gesunde Fettzellentwicklung und Stoffwechsel antreiben.
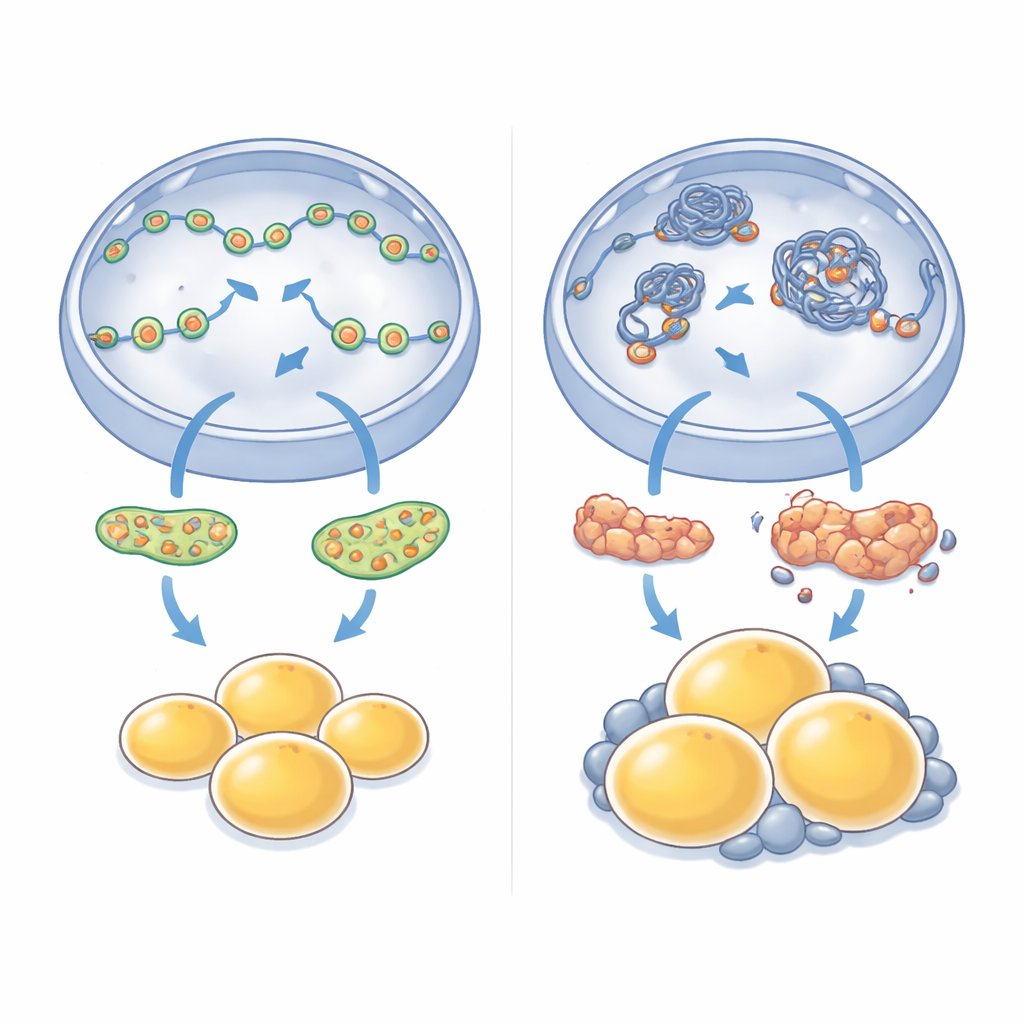
Wenn lokale Veränderungen zu einer Gewichtszunahme des ganzen Körpers werden
Die Folgen des Verlusts dieses einzelnen nukleären Motors blieben nicht auf Zellen in der Schale beschränkt. Mäuse ohne NM1 wurden mit der Zeit schwerer als ihre normalen Wurfgeschwister, obwohl sie nicht mehr Nahrung aufnahmen. Scans und Gewebeanalysen zeigten eine deutliche Fettansammlung, besonders um innere Organe im Bauchraum, und die einzelnen Fettzellen in diesen Bereichen waren auffällig vergrößert. Als die Forschenden maßen, welche Gene in diesem viszeralen Fett hoch- oder runterreguliert waren, fanden sie weitreichende Veränderungen: Signalwege, die Energieverbrauch, Insulinsignalisierung und Gewebeumbau steuern, waren umprogrammiert. Gene, die mit Fettzellwachstum und -expansion verbunden sind, waren oft verstärkt, während mehrere zentrale Steuerfaktoren gesunder Fettzellbildung abgeschwächt waren – ein Spiegelbild der Defekte, die in kultivierten Stammzellen beobachtet wurden.
Entzündetes Fett und gestörte Energie-Motoren
Abgesehen von der reinen Größe zeigte das Fettgewebe der NM1-defizienten Mäuse Anzeichen von Entzündung und metabolischem Stress. Eine detaillierte Pfadanalyse hob eine starke Aktivierung von Immun-Signalen hervor, angetrieben von Molekülen wie Interferon-Gamma und Tumornekrosefaktor, die für die Förderung von Insulinresistenz und Stoffwechselkrankheiten bekannt sind. Gleichzeitig waren Regulatoren, die ein ruhiges, energieeffizientes Fettgewebe unterstützen, unterdrückt. Die Studie verband den Verlust von NM1 zudem mit gestörten Mitochondrien – den Energieaggregaten der Zelle. Gene, die normalerweise die Qualitätssicherung der Mitochondrien und den Wechsel zwischen effizienter Energieproduktion und schnellem, glykolytischem Energiestoffwechsel überwachen, waren fehlreguliert. Das deutet darauf hin, dass Fettzellen ohne NM1 eine weniger effiziente und stressanfälligere Energie-Strategie annehmen.
Gemeinsame Signale zwischen Mäusen und Menschen
Um zu prüfen, ob dieser nukleäre Motorweg auch beim Menschen relevant sein könnte, untersuchten die Autorinnen und Autoren große genetische Datensätze aus menschlichem viszeralen Fett. Sie konzentrierten sich auf einen menschlichen Verwandten von NM1, MYO1C, und analysierten Netzwerke von Varianten, die die Aktivität benachbarter Gene beeinflussen. Sie fanden viele der gleichen Themen wie bei Mäusen – zytoskelettale Kontrolle, Immun-Signalisierung und metabolische Regulation – in menschlichen Gen-Netzwerken rund um MYO1C. Mehrere Gene, die im NM1-defizienten Mausfett verändert waren, waren auch in diesen menschlichen Netzwerken verankert und wurden mit Umbauprozessen und Stoffwechsel des Fettgewebes in Verbindung gebracht. Diese artsübergreifende Übereinstimmung deutet darauf hin, dass ähnliche nukleäre Mechanismen das Adipositasrisiko beim Menschen beeinflussen könnten.
Was das für Adipositas und metabolische Gesundheit bedeutet
Insgesamt zeigt die Arbeit, dass NM1 weit mehr als ein nukleärer Helfer ist; es ist ein zentraler Knotenpunkt, der DNA-Organisation mit der Art und Weise verbindet, wie Fettzellen wachsen, Energie speichern und mit dem Immunsystem kommunizieren. Fehlt NM1, werden Gen-Schalter in Fettvorläufern falsch gesetzt, Mitochondrien funktionieren schlecht, Fettzellen vergrößern sich statt sich zu vermehren, und viszerales Fett entzündet sich – eine Kombination, die dem ungesunden Fettbild bei Adipositas und Insulinresistenz ähnelt. Für die allgemeine Leserschaft lautet die Botschaft: Die physische Anordnung der DNA und ihrer Helfer im Zellkern kann Gewebe eher in Richtung gesunde oder schädliche Fettvergrößerung prädisponieren. Proteine wie NM1 und sein menschliches Gegenstück MYO1C könnten eines Tages Ziele für Therapien werden, die Fettgewebe von innen heraus umgestalten und so eine präzisere Bekämpfung adipositasbezogener Erkrankungen ermöglichen.
Zitation: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Schlüsselwörter: Adipogenese, Chromatin, Mitochondrien, viszerales Fett, metabolische Entzündung