Clear Sky Science · de
M2-Makrophagen fördern lymphatische Metastasen durch Regulation der nukleären Translokation von PKM2 beim triple-negativen Mammakarzinom
Warum diese Forschung wichtig ist
Für Menschen mit der Diagnose eines triple-negativen Mammakarzinoms gehört die Sorge, dass der Krebs in benachbarte Lymphknoten streut, zu den größten Ängsten — ein entscheidender Schritt zur Ausbreitung im Körper. Diese Studie untersucht, wie bestimmte Immunzellen, die uns eigentlich schützen sollten, stattdessen diesem Brustkrebs helfen, in das Lymphsystem einzudringen, und identifiziert einen molekularen "Schalter", der pharmakologisch angegangen werden könnte, um diese Ausbreitung zu verlangsamen oder zu stoppen.
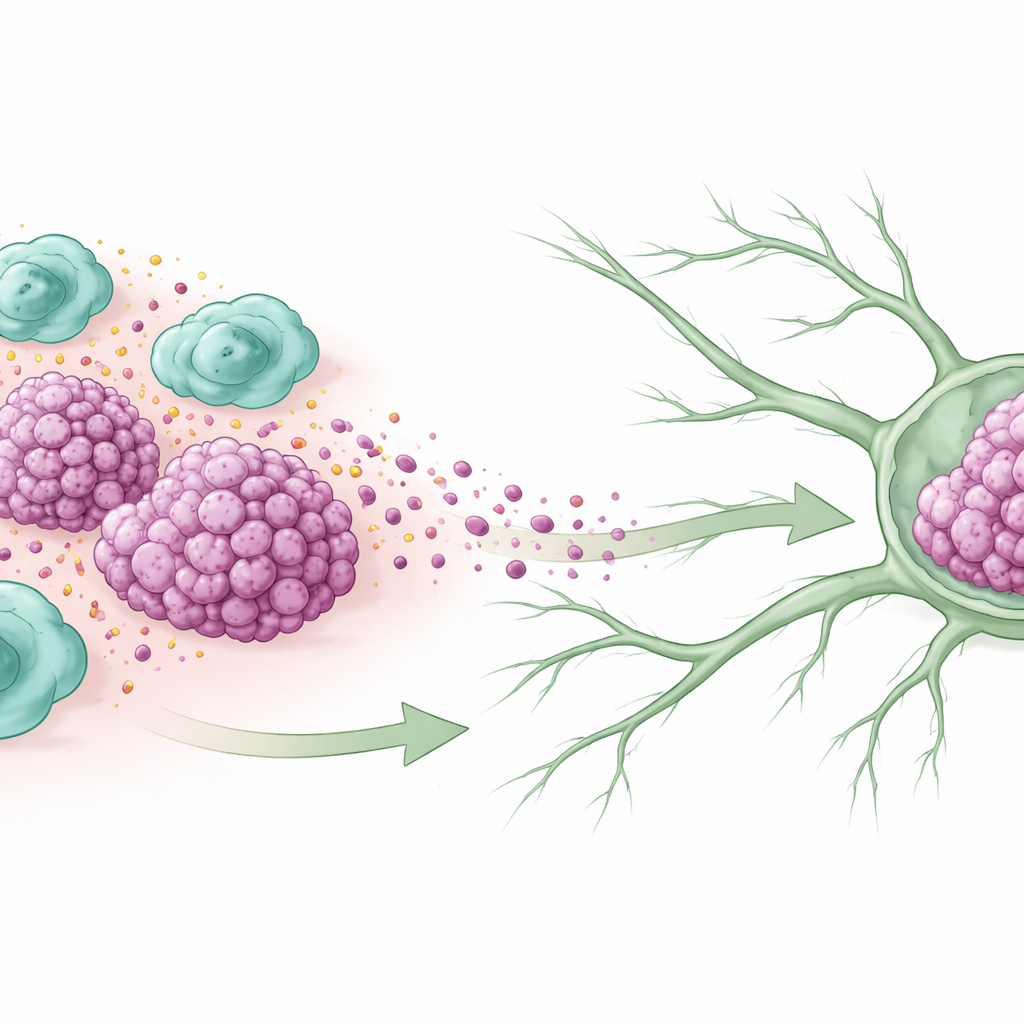
Immunhelfer, die zu Komplizen werden
In vielen Tumoren versammeln sich Immunzellen, die Makrophagen genannt werden, in großer Zahl. Einige von ihnen nehmen einen nährenden, wundheilungsähnlichen Zustand an, bekannt als M2-Phänotyp, der im Krebs häufig dazu führt, dass die Zellen dem Tumor eher helfen als ihn zu bekämpfen. Die Forschenden untersuchten Gewebeproben von Frauen mit triple-negativem Brustkrebs und fanden heraus, dass Tumoren, die bereits in Lymphknoten gestreut hatten, deutlich mehr dieser M2-Makrophagen enthielten. Patientinnen, deren Tumoren reich an diesen Zellen waren, wiesen tendenziell größere Tumoren, aggressivere Merkmale und eine kürzere Überlebenszeit auf, was darauf hindeutet, dass diese „friendly fire“ Immunzellen eng mit der Tumorprogression verknüpft sind.
Neue lymphatische „Autobahnen“ für Krebszellen aufbauen
Krebszellen erreichen Lymphknoten normalerweise nicht zufällig; sie reisen oft entlang neu gebildeter lymphatischer Gefäße, winziger Kanäle, die Gewebsflüssigkeit ableiten. In dieser Studie wiesen Tumoren mit hoher M2-Makrophagen-Dichte auch mehr dieser Lymphgefäße auf. In Zellkultur setzten Brustkrebszellen, die in Gegenwart von M2-Makrophagen gewachsen waren, Signale frei, die menschliche Lymphgefäßzellen dazu brachten, röhrenartige Netzwerke zu bilden und schneller zu wandern — ein Modell für das Wachstum neuer Lymphkanäle. In Mäusen produzierten Krebszellen, die vorher M2-Makrophagen ausgesetzt gewesen waren, mehr Lymphgefäße im Tumor und häufiger Metastasen in nahegelegene Lymphknoten, was bestätigt, dass diese Immunzellen aktiv Fluchtwege bauen.
Die verborgene Signalkette innerhalb der Krebszellen
Das Team fragte dann, welche chemischen Botschaften M2-Makrophagen senden, um Tumoren zur lymphatischen Ausbreitung zu treiben. Sie identifizierten ein bekanntes Molekül, TGF-β, das von M2-Makrophagen vermehrt freigesetzt wird. Dieses Signal veranlasste Brustkrebszellen, die Produktion von zwei Wachstumsfaktoren, VEGFC und VEGFD, hochzufahren — starke Treiber des Lymphgefäßwachstums. Entscheidend zeigten die Forschenden, dass ein Stoffwechselenzym in Krebszellen, PKM2, als zentraler Schalter in diesem Prozess dient. Unter TGF-β-Stimulation verstärkt PKM2 nicht nur die zelluläre Zuckerverbrennung, sondern wird auch chemisch modifiziert und wandert in den Zellkern, wo es die Gene für VEGFC und VEGFD mit aktiviert. Fehlt PKM2 oder ist seine Kerntranslokation blockiert, produzieren die Krebszellen deutlich weniger dieser lymphangiogenen Signale und sind weniger in der Lage, die Bildung von Lymphgefäßen zu stimulieren.
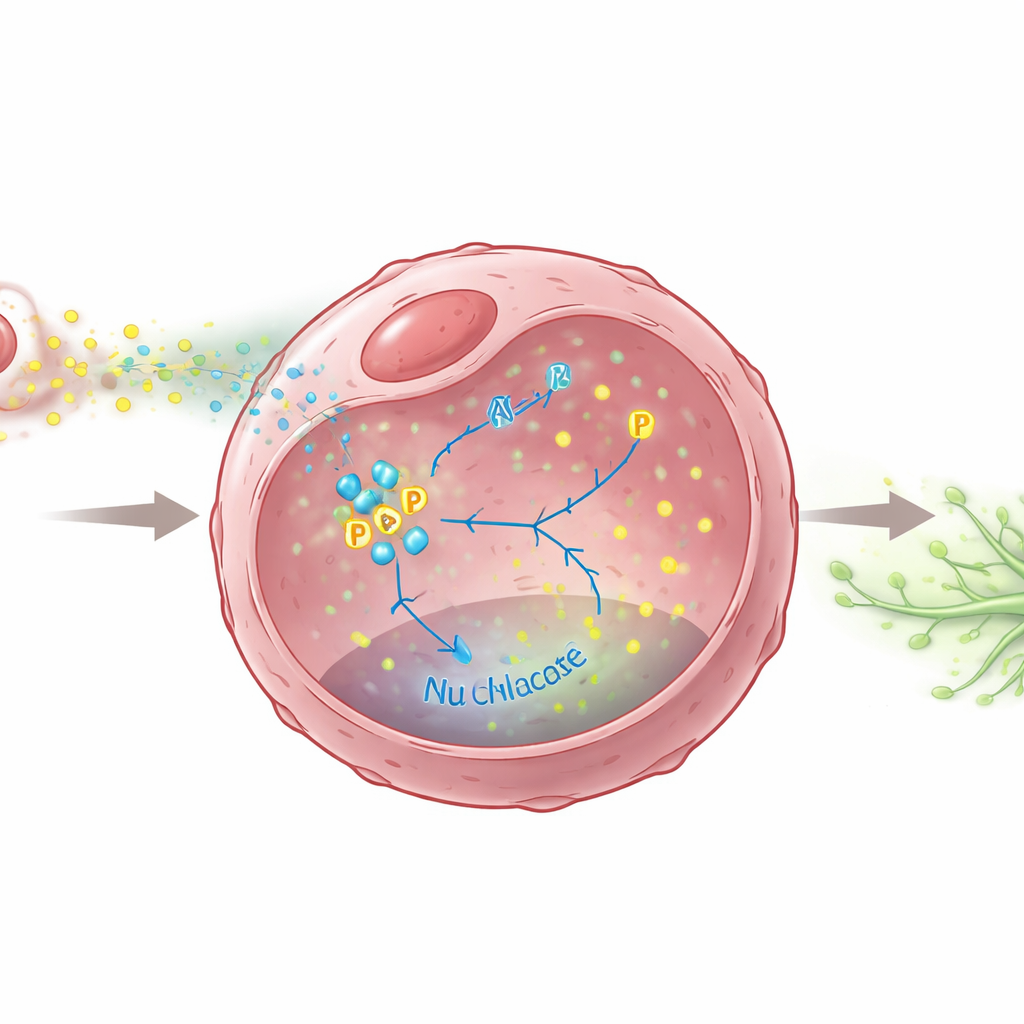
Testen einer möglichen Bremse gegen die Ausbreitung
Da PKM2 an dieser entscheidenden Schnittstelle zwischen verändertem Stoffwechsel und pro-metastatischer Signalgebung sitzt, prüften die Forschenden, ob seine Hemmung die lymphatische Ausbreitung verlangsamen kann. Sie verwendeten Shikonin, eine Verbindung, die die Aktivierung von PKM2 und dessen Eintritt in den Zellkern stört. In Zellversuchen reduzierte Shikonin die Mengen von VEGFC und VEGFD deutlich und schwächte die Fähigkeit der von Krebszellen freigesetzten Faktoren, Lymphgefäßwachstum und -bewegung zu induzieren. In Mausmodellen verminderte eine Behandlung mit Shikonin Anzahl und Größe der Lymphknotenmetastasen und verringerte die Dichte lymphatischer Gefäße im Tumor, ohne offensichtliche toxische Effekte bei den Tieren. Diese Befunde deuten darauf hin, dass die Blockade von PKM2 Krebszellen einerseits metabolische Vorteile entziehen und andererseits ihre Fähigkeit, das Lymphnetz zu ihren Gunsten umzubauen, abschwächen kann.
Was das für Patientinnen und Patienten bedeutet
Insgesamt schlägt die Studie eine klare Abfolge vor: M2-Makrophagen in triple-negativen Brusttumoren sekretieren TGF-β, das PKM2 in Krebszellen in eine doppelte Rolle versetzt — es fördert einen erhöhten Zuckerstoffwechsel und wirkt im Zellkern als Aktivator von VEGFC und VEGFD. Diese Faktoren stimulieren dann das Wachstum von Lymphgefäßen, die Krebszellen nutzen, um Lymphknoten und weiter entfernte Stellen zu erreichen. Indem PKM2 als kritischer Knotenpunkt in dieser Kette identifiziert wird, eröffnet die Arbeit neue Möglichkeiten, die lymphatische Ausbreitung vorherzusagen und potenziell zu behandeln — insbesondere bei Patientinnen und Patienten, deren Tumoren hohe Werte an M2-Makrophagen, PKM2 oder VEGFC/D zeigen. Obwohl weitere Studien am Menschen erforderlich sind, könnte das Anvisieren dieses Signalwegs helfen, das Lymphsystem von einer Krebsautobahn wieder in eine Barriere zu verwandeln.
Zitation: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
Schlüsselwörter: triple-negatives Mammakarzinom, Lymphknotenmetastasen, Tumor-assoziierte Makrophagen, PKM2, Lymphangiogenese