Clear Sky Science · de
Trimethylierung von Histon 3 Lysin 36 durch SETD2 formt eine epigenetische Landschaft in intestinalen Stammzellen, um den Lipidstoffwechsel zu orchestrieren und Zellseneszenz abzuschwächen
Warum Darmstammzellen im Alter wichtig sind
Tief in der Auskleidung unseres Darms arbeiten winzige Stammzellen unermüdlich, um das Gewebe zu erneuern, das uns bei der Verdauung und der Nährstoffaufnahme hilft. Mit zunehmendem Alter ermüden diese Stammzellen, wodurch der Darm anfälliger für Krankheiten wird und langsamer heilt. Diese Studie untersucht, wie feine chemische Markierungen an den DNA-verpackenden Proteinen dazu beitragen, intestinale Stammzellen jugendlich zu halten, wie ihr Verlust das intrazelluläre Fettverbrennen stört und wie gezielt eingesetzte Medikamente eines Tages den Abbau verlangsamen könnten.
Altern in einer anspruchsvollen Umgebung
Die Innenfläche des Darms ist eines der sich am schnellsten erneuernden Gewebe des Körpers. Stammzellen, die an der Basis kleiner Täler, so genannter Krypten, liegen, teilen sich, um alle paar Tage Milliarden von Zellen zu ersetzen. Diese ständige Arbeit erfordert eine verlässliche Energiezufuhr, viel davon aus dem Abbau von Fetten. Gleichzeitig werden diese Stammzellen durch einen „epigenetischen“ Code gesteuert — chemische Markierungen an Histonproteinen, die mitbestimmen, welche Gene aktiv oder stillgelegt sind. Die Autorinnen und Autoren konzentrierten sich auf eine solche Markierung, bekannt als H3K36-Trimethylierung, die von einem Enzym namens SETD2 erzeugt wird, und fragten, ob Veränderungen dieser Markierung erklären könnten, warum intestinale Stammzellen mit dem Alter an Leistungsfähigkeit verlieren.
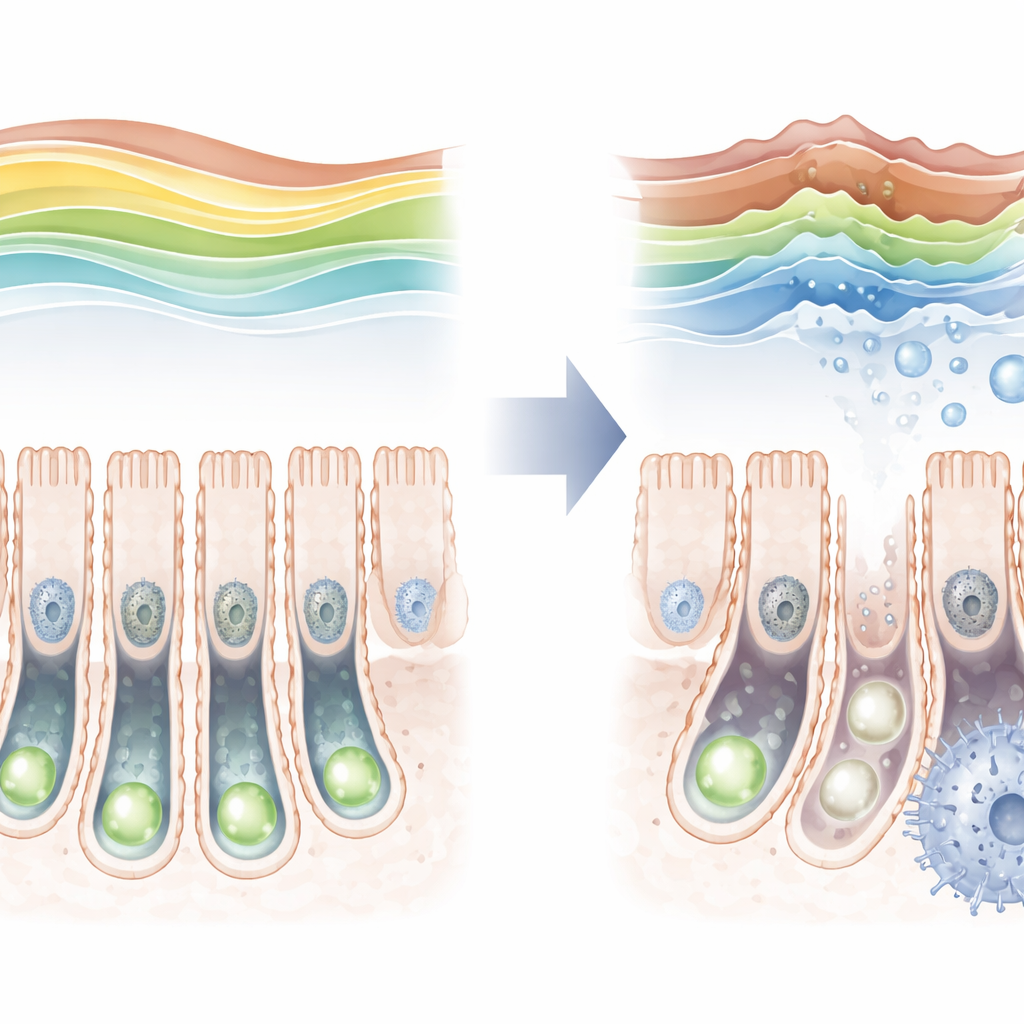
Eine Schutzmarkierung, die mit dem Alter schwindet
Anhand von Mäuseuntersuchungen über die Lebensspanne stellten die Forschenden fest, dass die H3K36-Trimethylmarkierung nicht statisch ist. Sie ist kurz nach der Geburt vergleichsweise niedrig, steigt bis zum jungen Erwachsenenalter an und fällt im hohen Alter wieder ab. Mit dem Rückgang dieser Markierung in älteren Tieren nahmen gleichzeitig Marker des zellulären Alterns in den Stammzellen zu, was auf einen Zusammenhang hindeutet. Um dies direkter zu prüfen, erzeugte das Team Mäuse, bei denen SETD2 nur in intestinalen Stammzellen entfernt werden konnte. Nach Löschung des Enzyms verschwand die Schutzmarkierung nahezu vollständig, die Stammzellen teilten sich seltener und sie hatten Schwierigkeiten, das vollständige Spektrum spezialisierter Darmzelltypen hervorzubringen.
Wie epigenetische Veränderungen das Fettverbrennen entgleisen lassen
Der Verlust dieser einzelnen Histonmarkierung löste eine Kaskade von Veränderungen innerhalb der Stammzellen aus. Messungen der Genaktivität zeigten, dass viele Gene, die am Zellzyklus und der DNA-Replikation beteiligt sind, herunterreguliert wurden, während Gene, die mit Stress und Altern verknüpft sind, hochfuhren. Auffallend war das stärkste Signal in Richtung gestörter Lipidverarbeitung: Gene, die normalerweis die Fettsäureoxidation — das kontrollierte Verbrennen von Fetten zur Energiegewinnung — unterstützen, wurden gedämpft, und Fette begannen sich in den Krypten anzusammeln. Metabolitprofile bestätigten die Akkumulation langkettiger Fettsäuren, ein Hinweis darauf, dass die üblichen Fettverarbeitungswege ins Stocken gerieten. Gleichzeitig verschob sich die physische Packung der DNA im Zellkern, wobei viele Regionen entweder zugänglicher oder stärker verschlossen wurden und so neu bestimmten, welche Gene die Zelle leicht nutzen kann.
Chromatin‑Remodeler und der Marsch in Richtung Seneszenz
Um zu verstehen, wie diese Veränderungen in der DNA‑Packung entstehen, kartierten die Autorinnen und Autoren sowohl offene Chromatinregionen als auch eine Reihe anderer Histonmarken im Genom. Beim Verlust der H3K36‑Trimethylierung gewannen große DNA‑Abschnitte „aktive“ Markierungen und wurden zugänglicher, insbesondere in der Nähe von Genen, die mit Stoffwechsel und Altern verknüpft sind. Ein Schlüsselakteur in diesem Übergang war der SWI/SNF‑Chromatin‑Remodeling‑Komplex, angetrieben von einer Kernuntereinheit namens SMARCA4. In Stammzellen ohne SETD2 stiegen die SMARCA4‑Spiegel an, und der Komplex schien dabei zu helfen, Regionen zu öffnen, die Seneszenzprogramme antreiben. Als die Forschenden die SMARCA4‑Aktivität genetisch oder mit einem gezielten Inhibitor reduzierten, erlangten die Stammzellen teilweise ihre Fähigkeit zurück, gesunde Mini‑Därme in einer Kultur zu bilden, und Altersmarker sanken — was darauf hindeutet, dass übermäßiges Remodeling diese Zellen in einen ermüdeten, seneszenten Zustand treibt.
Wiedererwecken von Energiestoffwechselwegen zur Rettung der Stammzellen
Da gestörtes Fettverbrennen als zentrales Problem auftauchte, testete das Team, ob die Ankurbelung dieses Weges das Altern der Stammzellen ausgleichen könnte. Sie verwendeten ein Medikament, das PPARα aktiviert, einen Masterregulator der Fettsäureoxidation. In Organoiden, die aus SETD2‑defizienten Stammzellen gezüchtet wurden, steigerten diese Maßnahmen das Wachstum, stellten die ausgeprägten Knospenstrukturen wieder her, die für vitale Stammzellen charakteristisch sind, und verringerten die Fettansammlungen. In lebenden Mäusen füllte dieselbe Intervention den Stammzellbestand teilweise wieder auf, senkte Seneszenzmarker und normalisierte die Lipidakkumulation in den intestinalen Krypten. Diese Befunde stellen die Fettsäureoxidation als eine entscheidende Verbindung zwischen epigenetischer Kontrolle und Stammzellgesundheit dar.
Was das für gesundes Altern bedeutet
Insgesamt zeigt die Arbeit, dass eine spezifische Histonmarkierung, die von SETD2 gesetzt wird, hilft, eine ausgewogene epigenetische Landschaft in intestinalen Stammzellen zu erhalten. Wenn diese Markierung schwindet, wird das Chromatin abnormal umgebaut, Fettverbrennungswege versagen, Lipide lagern sich an und Zellen rutschen in die Seneszenz, wodurch das Reparatursystem des Darms geschwächt wird. Durch das Drosseln der überaktiven Remodeling‑Maschinerie oder die Wiederherstellung des Fettstoffwechsels mit gezielten Medikamenten könnte es möglich sein, die Funktion von Stammzellen und die Darmgesundheit im Alter zu bewahren. Obwohl diese Ergebnisse aus Mäusen stammen, spiegeln sie Muster wider, die auch bei menschlichen Darmerkrankungen zu sehen sind, und legen die Aussicht nahe, dass fein abgestimmte metabolische Therapien eines Tages helfen könnten, altersbedingtem Abbau in unseren eigenen intestinalen Stammzellen entgegenzuwirken.
Zitation: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Schlüsselwörter: intestinale Stammzellen, Epigenetik, Fettsäureoxidation, zelluläre Seneszenz, SETD2