Clear Sky Science · de
Ein an Lamp2a gebundenes RNA-Molekül, das von ADSCs sezerniert wird, verhindert ENO1‑Lactylierung‑Glykolyse‑Rückkopplung und maligne Zellverhalten bei triple-negativem Mammakarzinom
Warum das für Patienten wichtig ist
Das triple-negative Mammakarzinom gehört zu den aggressivsten Formen von Brustkrebs und fehlt die Hormon‑ oder Wachstumsfaktor‑Zielstrukturen, die andere Subtypen behandelbarer machen. Diese Studie zeigt, wie diese Tumoren ihren Energiestoffwechsel umstellen, um in sauerstoffarmen Umgebungen zu überleben, und beschreibt einen erfinderischen Weg, diese Umstellung anzugreifen. Für Leserinnen und Leser bietet sie einen Einblick, wie das Verständnis des Krebsstoffwechsels zu neuen, hochspezifischen Therapien führen kann, die sich deutlich von traditioneller Chemotherapie unterscheiden.
Wie diese Tumoren sich mit Energie versorgen
Viele Krebserkrankungen verlassen sich stark auf einen schnellen, aber ineffizienten Energiemechanismus namens Glykolyse, bei dem Zucker in das Nebenprodukt Laktat umgewandelt wird. Anhand von Patientinnenproben, öffentlichen Gen‑Datenbanken und mehreren Brustkrebszelllinien zeigen die Forschenden, dass triple‑negative Tumoren noch stärker auf Glykolyse setzen als andere Brustkrebsformen. Ein Schlüsselenzym dieses Wegs, ENO1, liegt in diesen Tumoren besonders hoch vor und ist mit schlechterem Überleben verbunden. Wurden ENO1‑Spiegel in im Labor gezüchteten triple‑negativen Zellen reduziert, verschoben sich die Zellen von der Glykolyse hin zu normalerer Energiegewinnung in den Mitochondrien, sie wuchsen langsamer und waren weniger invasiv bzw. bildeten weniger Kolonien.
Eine gefährliche Rückkopplung in Krebszellen
Bei genauerer Untersuchung entdeckte das Team, dass Laktat selbst ENO1 stärkt und die Krebszellen in einen Teufelskreis einsperrt. Laktat kann Proteine chemisch modifizieren in einem Prozess, der als Lactylierung bezeichnet wird. In triple‑negativen Zellen erhöhte zusätzliches Laktat die Lactylierung von ENO1, was wiederum die Aktivität und Stabilität des Enzyms steigerte, die Glykolyse weiter beschleunigte und noch mehr Laktat produzierte. Unter sauerstoffarmen Bedingungen — typisch für solide Tumoren — wurde dieser Kreislauf stärker, wodurch Krebszellen dem Zelltod widerstanden und weiter proliferierten. Die Hemmung der ENO1‑Aktivität mit einem kleinmolekularen Inhibitor oder die Verringerung der Laktatproduktion schwächte diesen Kreislauf, dämpfte die Glykolyse und verlangsamte das Tumorwachstum in Mäusemodellen.
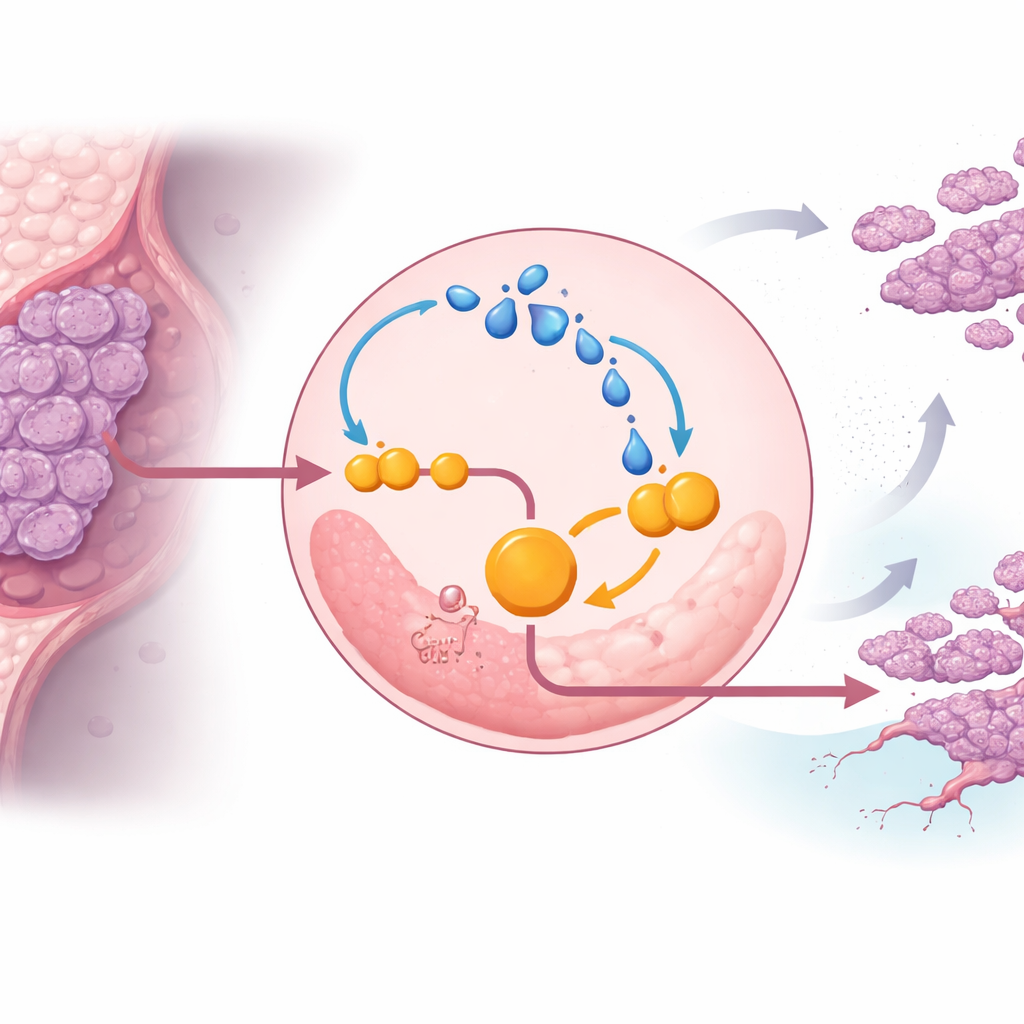
Der molekulare Schalter, der ENO1 schützt
Die Studie identifizierte einen spezifischen Kontrollpunkt an ENO1, der diesen Kreislauf ermöglicht. Ein Protein namens EP300 fügt an mehreren Lysinstellen von ENO1 laktatbasierte Markierungen hinzu, wobei eine Stelle, bezeichnet als K262, sich als entscheidend erwies. War diese Stelle so verändert, dass sie nicht mehr lactyliert werden konnte, wurde ENO1 schnell zu den Recyclingzentren der Zelle, den Lysosomen, transportiert und abgebaut. Ohne dieses schützende Mark verloren triple‑negative Zellen einen Großteil ihres glykolytischen Antriebs und ihrer Fähigkeit, Tumore und Metastasen in Tiermodellen zu bilden. Damit zeichnet sich die Lactylierung von ENO1 an K262 als molekularer Schalter ab, der das Enzym vor dem Abbau schützt und den veränderten Stoffwechsel des Tumors aufrechterhält.
Ein neuer Weg, ENO1 zur Zerstörung zu markieren
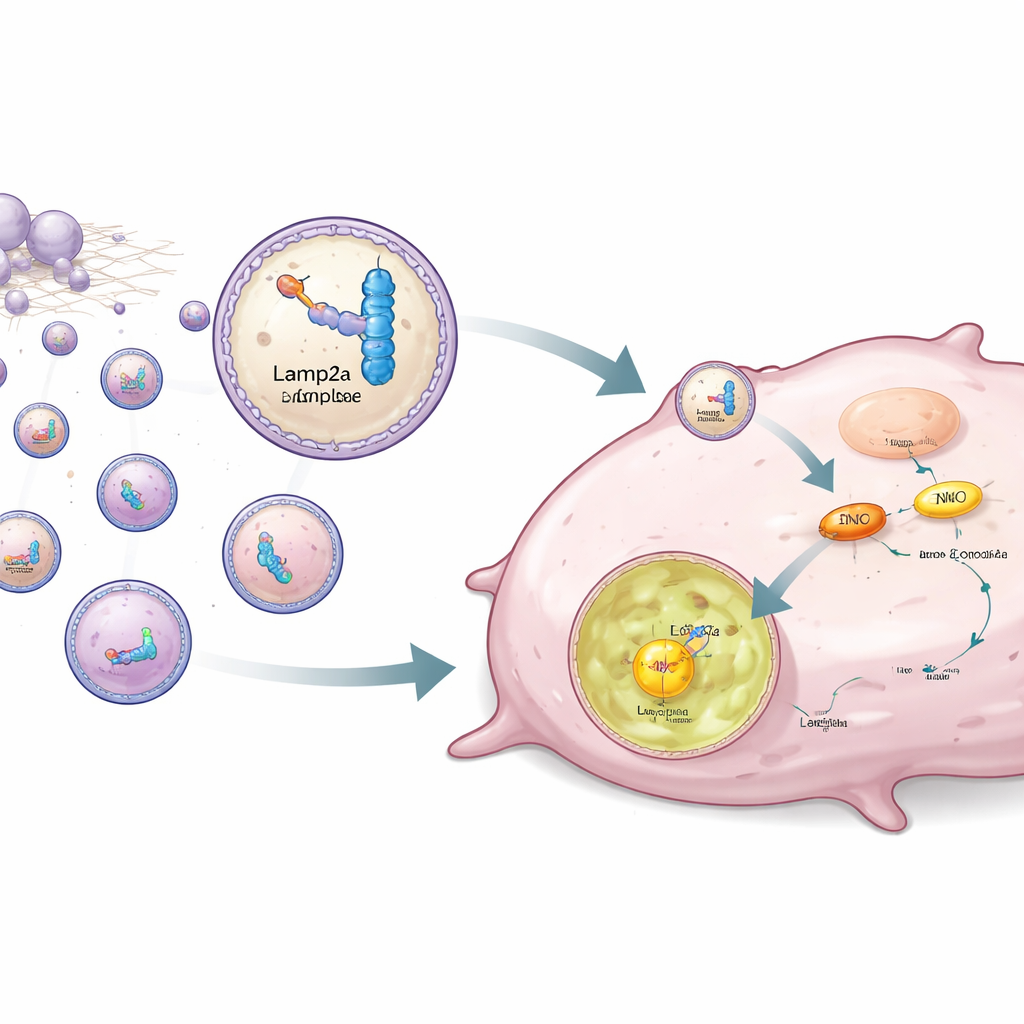
Anstatt ENO1 nur zu blockieren, entwarfen die Autorinnen und Autoren eine Strategie, es selektiv aus Krebszellen zu entfernen. ENO1 wirkt zudem als RNA‑bindendes Protein und erkennt bestimmte kurze RNA‑Sequenzen. Das Team entwickelte synthetische RNA‑Segmente, die stark an ENO1 binden, und koppelte sie an Lamp2a, ein Lysosomen‑Membranprotein, das an zielgerichtetem Proteinabbau beteiligt ist. Menschliche, aus Fettgewebe gewonnene Stammzellen wurden genetisch so verändert, dass sie dieses RNA–Lamp2a‑Paar produzieren und in kleine Vesikel, sogenannte Exosomen, verpacken. Wenn diese ingenieurmäßig veränderten Exosomen zu triple‑negativen Zellen gegeben wurden, heftete sich der RNA‑Teil an ENO1, während der Lamp2a‑Teil den gesamten Komplex in die Lysosomen lenkte, wo ENO1 abgebaut wurde, selbst wenn es die stabilisierende Lactylierung trug.
Testen des zielgerichteten Abbaus in Tiermodellen
Um diese Idee an eine praktischere Therapie heranzuführen, kultivierten die Forschenden die modifizierten Stammzellen auf einem biologisch abbaubaren Gerüst und implantierten diesen Verbund unter die Haut von Mäusen in der Nähe von triple‑negativen Tumoren. Von dieser Stelle aus setzten die Stammzellen kontinuierlich Exosomen frei, die die ENO1‑zielgerichteten Komplexe transportierten. Tumore in diesen Mäusen zeigten deutlich reduzierte ENO1‑Proteinwerte, verringerte Glykolyse, weniger teilende Zellen und stärkere Anzeichen von Zelltod im Vergleich zu Kontrolltieren. Die Tumore wuchsen langsamer und ihr malignes Verhalten war deutlich abgeschwächt, was zeigt, dass die Umlenkung von ENO1 in Lysosomen den Tumor effektiv der bevorzugten Brennstoffquelle berauben kann.
Was das für künftige Behandlungen bedeuten könnte
Für ein nicht spezialisiertes Publikum ist die Kernbotschaft, dass diese Arbeit sowohl eine Schwäche als auch einen potenziellen neuen Behandlungsansatz für das triple‑negative Mammakarzinom offenlegt. Die Schwäche ist die Abhängigkeit des Tumors von einem sich selbst verstärkenden Energiesystem, das um ENO1 und Laktat herum aufgebaut ist, besonders in sauerstoffarmen Regionen. Der Behandlungsansatz besteht in einem System für gezielten Proteinabbau, das maßgeschneiderte RNA und stammzellabgeleitete Exosomen nutzt, um ENO1 in die Entsorgungsmaschinerie der Zelle zu treiben. Auch wenn dieser Ansatz noch weit von der klinischen Anwendung entfernt ist, zeigt er, wie tiefgehendes Verständnis der metabolischen Tricks von Krebs präzise Therapien inspirieren kann, die darauf abzielen, bösartige Zellen zu entwaffnen statt sie einfach nur zu vergiften.
Zitation: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Schlüsselwörter: triple-negatives Mammakarzinom, Krebsstoffwechsel, Laktat‑Signalisierung, gezielte Proteinabbau, ENO1‑Enzym