Clear Sky Science · de
Die Phosphatase Shp1 reguliert die CXCR2-Proteinstabilität und IL8-vermittelte Invasivität bei Brustkrebs
Warum diese Forschung für Brustkrebs wichtig ist
Brustkrebs bleibt eine der häufigsten Todesursachen durch Krebs bei Frauen, vor allem weil einige Tumoren invasiv werden und in entfernte Organe streuen. Diese Studie beleuchtet, wie ein in Tumoren verbreitetes Entzündungssignal, genannt IL8, mit Brustkrebszellen kommuniziert und wie eine molekulare „Bremse“ namens Shp1 mitentscheidet, ob diese Zellen sesshaft bleiben oder aggressiver werden. Das Verständnis dieses molekularen Tauziehens könnte neue Wege eröffnen, die Ausbreitung schwer behandelbarer Brustkrebserkrankungen, insbesondere des triple-negativen Typs, zu verlangsamen oder zu verhindern.
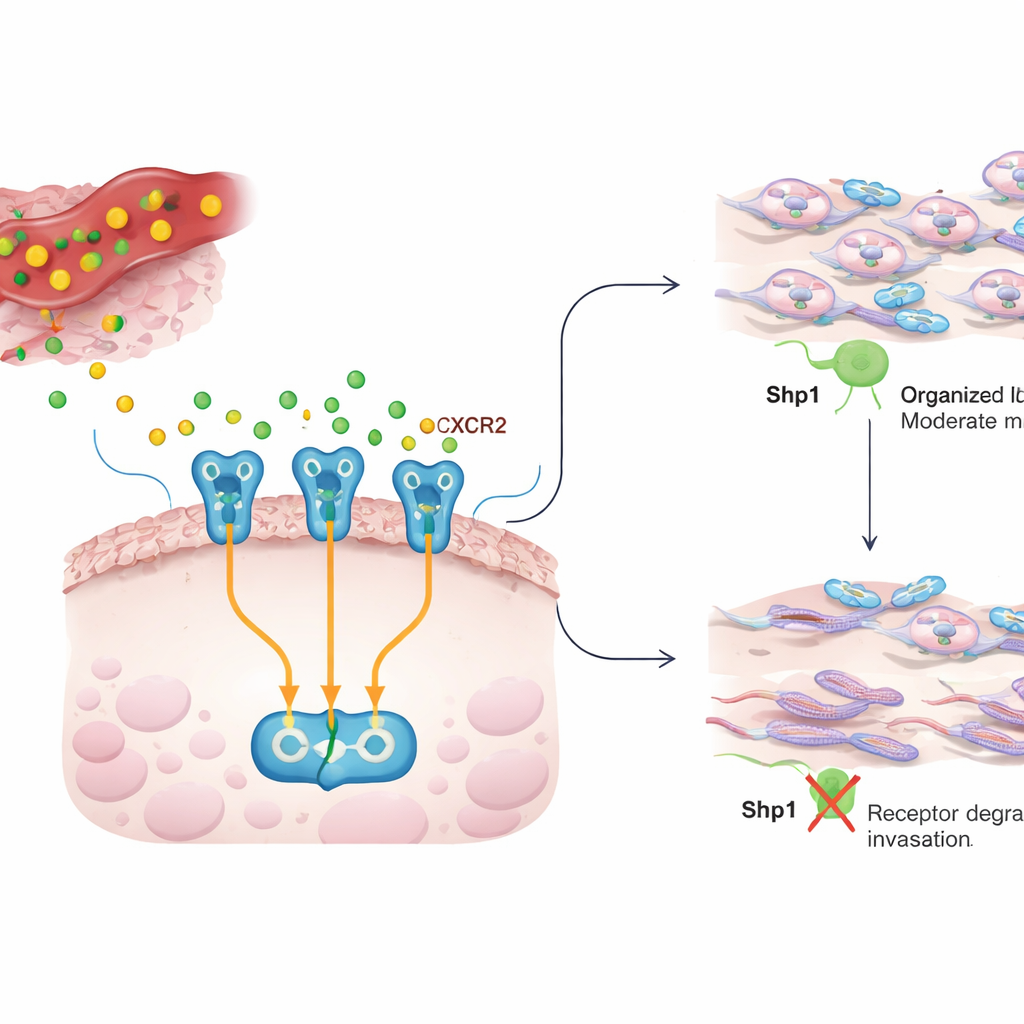
Ein Dialog zwischen Entzündung und Krebszellen
Im Tumor sind Krebszellen von Immun- und Stützzellen umgeben, die chemische Botenstoffe, sogenannte Zytokine, freisetzen. IL8 ist einer dieser Botenstoffe und kommt in vielen Krebserkrankungen in hohen Konzentrationen vor, wo es Wachstum, Gefäßbildung und die Beweglichkeit und Invasivität von Krebszellen fördert. IL8 signalisiert über einen Rezeptor an der Zelloberfläche, CXCR2. Bindet IL8 an CXCR2, schaltet das mehrere interne Signalwege ein, die das Zellskelett umorganisieren und den Zellen helfen, sich durch Gewebe zu bewegen und zu streuen. Die vorliegende Arbeit fragt, wie dieses IL8–CXCR2-Gespräch reguliert wird und ob Shp1, ein Enzym, das meist als wachstumshemmende Bremse betrachtet wird, auch dieses invasive Verhalten beeinflusst.
Die verborgene Rolle von Shp1 in der Zellbewegung
Die Forschenden entfernten oder blockierten zunächst Shp1 chemisch in einer häufig verwendeten luminalen Brustkrebszelllinie (MCF7) und maßen, wie gut die Zellen wandern und durch ein Gel, das Gewebe nachahmt, invasieren können. Ohne Shp1 schlossen die Krebszellen Wunden schneller und drückten sich zwei- bis dreimal effizienter durch das Gel, was zeigt, dass Shp1 normalerweise die Bewegung bremst. Anhand von Patientendaten fanden sie außerdem, dass Frauen mit Tumoren, die weniger Shp1 exprimierten, eine schlechtere Überlebensrate und eine kürzere Zeit bis zum Rückfall hatten. Zusammengenommen deuten diese Ergebnisse darauf hin, dass Shp1 das aggressive Verhalten von Brustkrebszellen begrenzt und der Verlust dieser Bremse mit ungünstigeren Verläufen verbunden ist.
Wie IL8 Shp1 umschaltet und einen Schlüsselrezeptor umprogrammiert
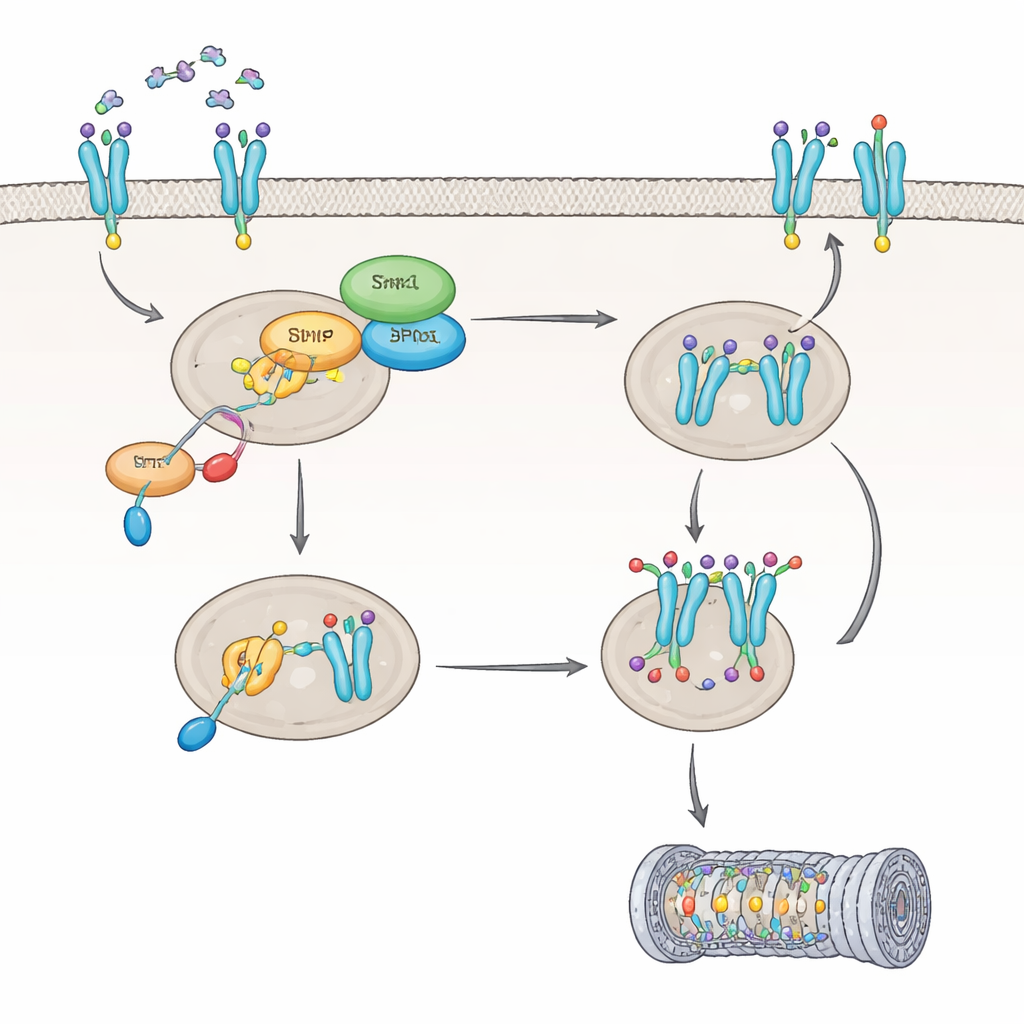
Im nächsten Schritt untersuchte das Team, wie IL8 Shp1 selbst beeinflusst. Sie entdeckten, dass IL8 ein Protein namens PKC aktiviert, das Shp1 an einer spezifischen Stelle markiert und dessen enzymatische Aktivität um etwa 60 Prozent reduziert. Wird Shp1 auf diese Weise gedämpft, wird ein anderes Enzym, PP2A, weniger aktiv, und der CXCR2-Rezeptor verbleibt in einem stark modifizierten Zustand, der sein Schicksal in der Zelle verändert. Statt abgebaut und wieder an die Zelloberfläche recycelt zu werden, wird CXCR2 hauptsächlich für die Zerstörung durch die proteasomale Abbaumaschinerie markiert. Eine bestimmte Modifikation an CXCR2, am Aminosäurerest Ser347, erwies sich als entscheidend für das Anheften dieser Abbausignale. In Zellen ohne Shp1 war CXCR2 stärker markiert und wurde schneller abgebaut, sodass weniger Rezeptoren an der Zelloberfläche verblieben und die Reaktion auf IL8 im Zeitverlauf abgeschwächt war.
Verschiedene Brustkrebsarten, verschiedene Verschaltungen
Brustkrebs ist keine einheitliche Krankheit; Tumoren werden anhand ihrer Rezeptormuster in luminale, HER2-positive und triple-negative Subtypen eingeteilt. Die Forschenden prüften den IL8–CXCR2–Shp1-Kreislauf in mehreren Zelllinien, die jede dieser Subtypen repräsentieren. In luminalen und triple-negativen Zellen aktivierte IL8 die Shp1–PP2A–CXCR2-Kaskade, und die Blockade von Shp1 erhöhte sowohl die Grundinvasivität als auch den Verlust des typischen pro-invasiven Effekts von IL8. Im Gegensatz dazu reagierten HER2-positive Zellen weiterhin auf IL8, aber die Blockade von Shp1 veränderte ihr Verhalten kaum, was darauf hindeutet, dass in diesen Tumoren Shp1 an andere Signalwege, etwa HER2, gebunden und weniger verfügbar ist, um CXCR2 zu regulieren. Groß angelegte Genexpressionsanalysen stützten dieses Bild: Triple-negative Linien zeigten tendenziell niedrigere Shp1-Werte, veränderte GPCR-bezogene Signalgebung und höhere IL8-Spiegel, konsistent mit einem aggressiveren, entzündungsgetriebenen Profil.
Was das für zukünftige Therapien bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft, dass das Enzym Shp1 als Verkehrsleiter für den IL8-Rezeptor CXCR2 fungiert und bestimmt, ob der Rezeptor wiederverwendet oder zerstört wird und damit, wie stark Brustkrebszellen auf entzündliche Signale reagieren. Bei luminalem und triple-negativem Brustkrebs scheint dieser Kontrollpunkt besonders wichtig: Sind Shp1-Spiegel niedrig oder ist seine Aktivität blockiert, werden die Zellen invasiver und die Patientenergebnisse verschlechtern sich. Da Shp1 durch bestimmte bereits existierende Medikamente verstärkt oder moduliert werden kann, könnte das Anvisieren der Shp1–CXCR2-Achse, möglicherweise in Kombination mit IL8- oder CXCR2-Blockern, eine neue Strategie sein, um Invasion und Metastasierung aggressiver Brustkrebs‑Subtypen zu begrenzen.
Zitation: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Schlüsselwörter: Brustkrebsinvasion, IL8-Signalgebung, CXCR2-Rezeptor, Shp1-Phosphatase, triple-negativer Brustkrebs