Clear Sky Science · de
CRMP2 hemmt die Metastasenbildung, indem es die ILF3‑abhängige Stabilisierung der CXCL10‑mRNA bei Brustkrebs beeinträchtigt
Warum das Stoppen der Krebsausbreitung wichtig ist
Die meisten Todesfälle durch Brustkrebs treten nicht wegen des ursprünglichen Tumors auf, sondern weil Krebszellen zu lebenswichtigen Organen wie der Lunge wandern und dort neue Herde bilden. Diese Studie enthüllt ein im Inneren von Brustkrebszellen vorhandenes Schutzprotein, das diese Ausbreitung verlangsamen oder sogar blockieren kann, indem es die „Willkommensmatte“ verändert, die entfernte Organe für wandernde Krebszellen auslegen. Das Verständnis dieses verborgenen Sicherheitsschalters könnte den Weg für neue Behandlungen öffnen, die verhindern, dass sich Krebs an anderen Stellen im Körper festsetzt.
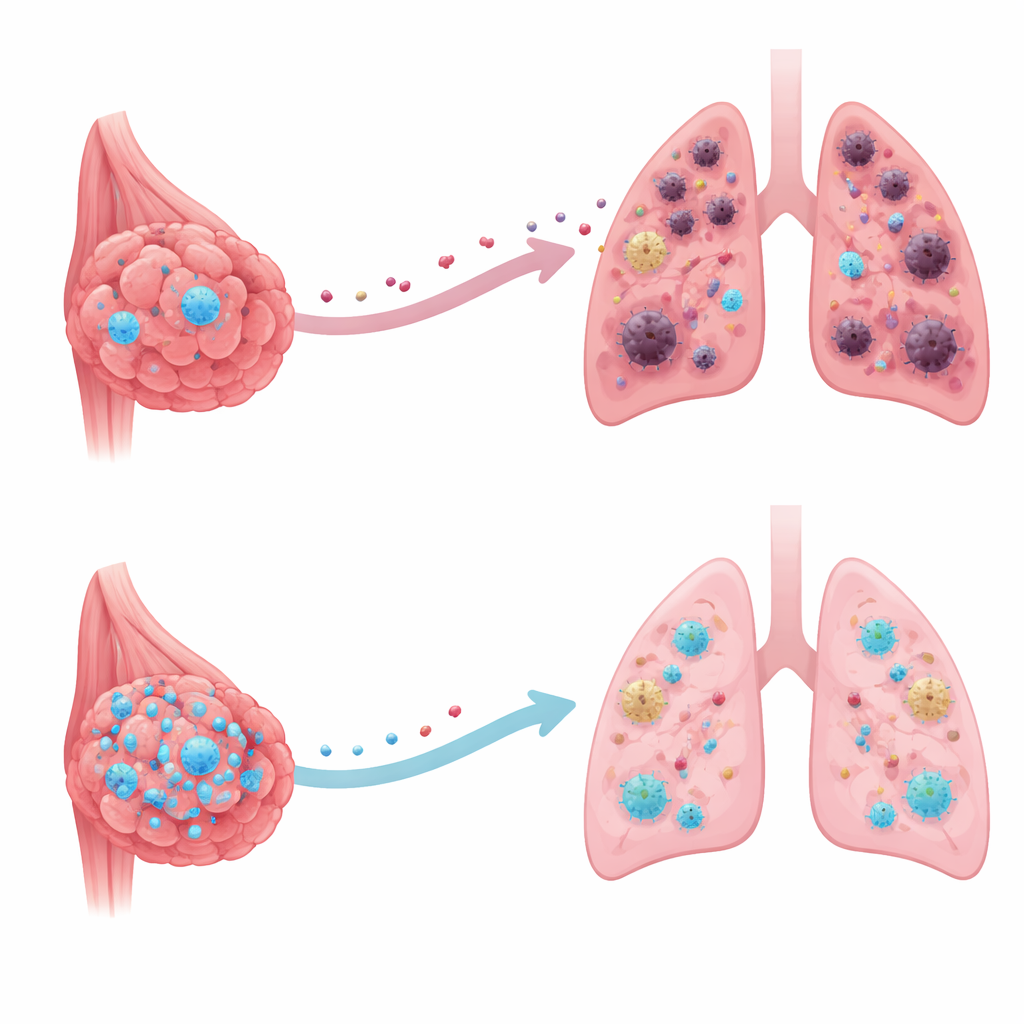
Ein stiller Verteidiger in Krebszellen
Die Forschenden konzentrierten sich auf ein Protein namens CRMP2, das vor allem dafür bekannt ist, Nervenzellen beim Wachstum und der Aufrechterhaltung ihres inneren Gerüsts zu unterstützen. Bei der Auswertung großer öffentlicher Krebsdatenbanken und Patiententumorproben stellten sie fest, dass die CRMP2‑Werte in Brusttumoren ungewöhnlich niedrig waren, besonders in bereits metastasierten Fällen. Patientinnen, deren Tumoren noch höhere Mengen an CRMP2 aufwiesen, lebten tendenziell länger und entwickelten seltener Fernmetastasen. Dieses Muster deutet darauf hin, dass CRMP2 eher wie eine Bremse als wie ein Beschleuniger beim Brustkrebs wirkt und als interner Verteidiger statt als Krankheits‑Treiber fungiert.
Wie die Lunge für eine Invasion vorbereitet wird
Krebszellen treffen in einem entfernten Organ selten unvorbereitet ein. Lange bevor sie dort ankommen, setzt der Primärtumor Moleküle frei, die dieses Organ so umgestalten, dass daraus das entsteht, was Wissenschaftler eine „prä‑metastatische Nische“ nennen – ein Mikromilieu, das das Überleben von Krebszellen begünstigt. Mithilfe eines gut etablierten Mausmodells, das menschlichen Brustkrebs eng nachbildet, zeigte das Team, dass bei Tumorzellen, die so verändert wurden, dass sie zusätzliches CRMP2 produzieren, der Primärtumor genauso schnell wuchs, die Lunge jedoch deutlich weniger gastfreundlich war. Entzündungs‑ und Gewebeumbau‑Marker in der Lunge nahmen ab, und weniger der Immunzellen, die normalerweise anti‑tumorale Abwehrkräfte unterdrücken, wurden angezogen. Infolgedessen bildeten sich nach Entfernung des Primärtumors deutlich weniger metastatische Knoten in der Lunge.
Eine Signalkette, die Ärger anrichtet
Bei tiefergehenden Untersuchungen fragten die Forschenden, welche vom Tumor abgegebenen Signale für die Vorbereitung der Lunge verantwortlich sind. Sie konzentrierten sich auf CXCL10, ein kleines Botenprotein (Chemokin), das bestimmte Immunzellen anlockt und ruhende Krebszellen wecken kann. In menschlichen und murinen Brustkrebszellen im Labor reduzierte eine Erhöhung von CRMP2 die Menge an produziertem und freigesetztem CXCL10 deutlich. In Mäusen zeigten Lungen, die Tumormaterial mit hohem CRMP2‑Gehalt ausgesetzt waren, deutlich geringere CXCL10‑Spiegel und weniger eingehende Immunzellen, die normalerweise die schützende T‑Zell‑Aktivität dämpfen. Als die Forschenden CXCL10 mit einem Antikörper blockierten, nahm die Lungenkolonisation durch Krebszellen ab; als sie zusätzliches CXCL10 hinzugaben, verschwand der schützende Effekt von CRMP2. Damit steht CXCL10 klar stromabwärts von CRMP2 als Schlüsselfaktor für die Entstehung einer metastasenfreundlichen Nische.
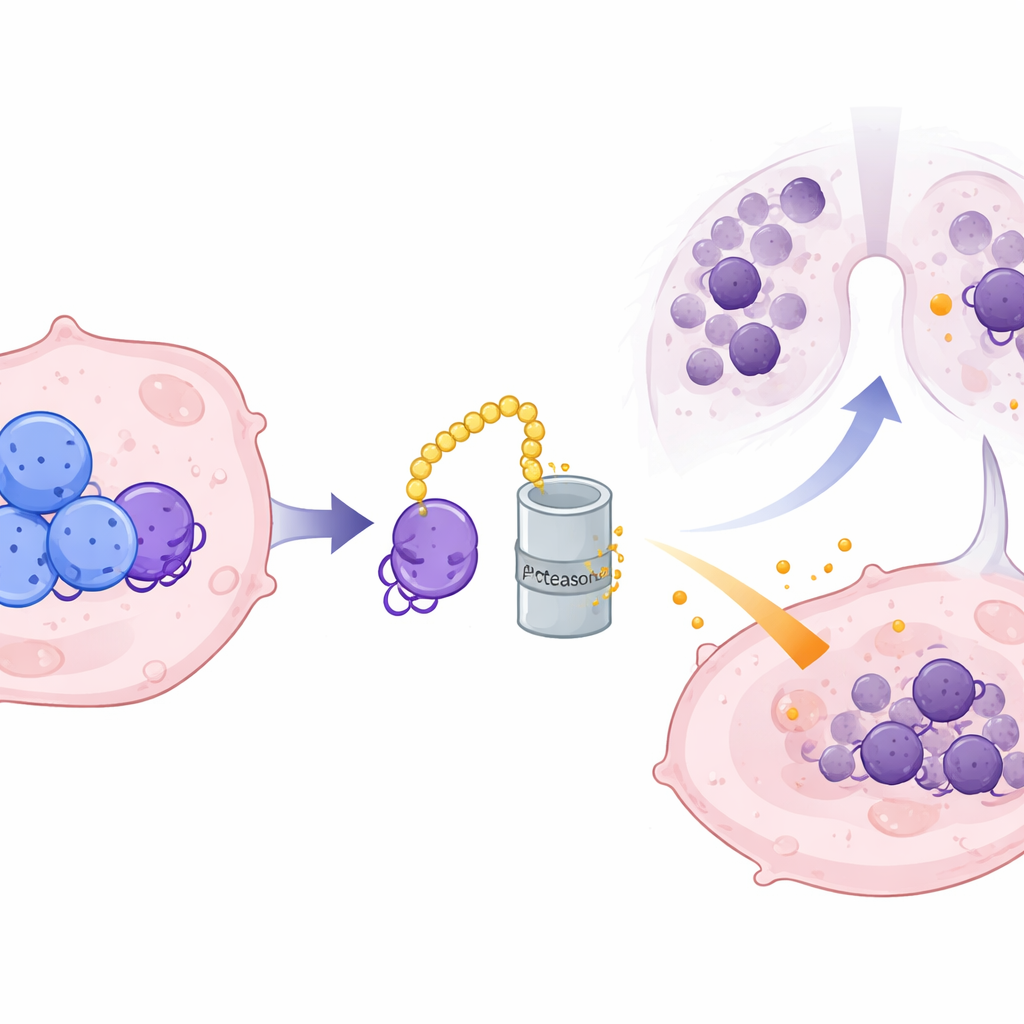
Der verborgene Mittelsmann, der schädliche Signale stabilisiert
Da CRMP2 innerhalb der Zellen lokalisiert ist, CXCL10 aber sezerniert wird, vermutete das Team einen molekularen Mittelsmann. Sie identifizierten ILF3, ein RNA‑bindendes Protein, als direkten Partner von CRMP2. ILF3 bindet an die RNA‑Vorlage für CXCL10 und schützt sie normalerweise vor dem Abbau, wodurch mehr CXCL10‑Protein produziert werden kann. CRMP2 bindet ILF3 an spezifischen Kontaktstellen und markiert es für den Abbau über die zelluläre Protein‑Recycling‑Maschinerie, wodurch die Lebensdauer von ILF3 verkürzt und seine Bindung an die CXCL10‑RNA aufgehoben wird. Wenn CRMP2‑Werte hoch sind, wird ILF3 schneller abgebaut, die CXCL10‑RNA wird instabil und es wird weniger des entzündungsfördernden Chemokins sezerniert. When ILF3 künstlich wiederhergestellt wurde, konnte es die Unterdrückung von CXCL10 durch CRMP2 außer Kraft setzen und bestätigte damit seine Rolle als entscheidende Verbindung in dieser Kette.
Aus einer Pflanzenverbindung einen potenziellen Verbündeten machen
Um zu prüfen, ob dieser Signalweg therapeutisch nutzbar ist, durchsuchten die Forschenden eine Bibliothek natürlicher Verbindungen und fanden Psoralen – ein aus Pflanzen gewonnenes Molekül, das lange in Hautbehandlungen verwendet wird – das direkt an CRMP2 bindet und es stabilisiert. In Zellversuchen erhöhte Psoralen die CRMP2‑Spiegel, senkte ILF3 und CXCL10 und verringerte das invasive Verhalten von Brustkrebszellen, ohne deren generelle Lebensfähigkeit zu schädigen. In mehreren Mausmodellen verkleinerte Psoralen die Primärtumoren zwar nicht, reduzierte aber stark Lungenmetastasen und schwächte die Ausbildung der prä‑metastatischen Nische ab, wiederum in einer Weise, die von CRMP2 abhing. Obwohl Psoralen selbst Leberschäden verursachen kann und noch weiterentwickelt werden muss, zeigen diese Ergebnisse, dass kleine Moleküle die schützende Rolle von CRMP2 stärken können.
Was das für Patientinnen und Patienten bedeutet
In der Summe zeigt diese Arbeit eine schützende Achse innerhalb von Brustkrebszellen auf, in der CRMP2 ILF3 destabilisiert, was wiederum CXCL10 verringert und somit verhindert, dass die Lunge zu fruchtbarem Boden für Metastasen wird. Anstatt Krebszellen direkt anzugreifen, zielt diese Strategie darauf ab, die entfernten Nischen zu entwaffnen, von denen sie abhängen, und so das Gleichgewicht zugunsten der körpereigenen Abwehr zu kippen. Obwohl noch viel zu tun ist, bevor ein solcher Ansatz in die Klinik gelangt, bietet die gezielte Beeinflussung des CRMP2–ILF3–CXCL10‑Wegs – möglicherweise mit sichereren, psoralenähnlichen Wirkstoffen – einen vielversprechenden neuen Ansatz, um die Ausbreitung von Brustkrebs zu verhindern.
Zitation: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Schlüsselwörter: Brustkrebs‑Metastasierung, prä‑metastatische Nische, Chemokin‑Signalgebung, RNA‑bindende Proteine, Therapeutika aus Naturstoffen