Clear Sky Science · de
Forschungsfortschritte zur Kommunikation zwischen tumorumgebungsassoziierten Fibroblasten und Tumorzellen mithilfe von Ko-Kultur-Organoiden
Warum die Nachbarschaft des Tumors wichtig ist
Krebs ist mehr als nur ein Haufen entarteter Zellen; er wächst in einer lebendigen Nachbarschaft aus Stütz- und Gerüstzellen, Blutgefäßen und Immunakteuren. Unter diesen Nachbarn formen eine Gruppe, die als tumorumgebungsassoziierte Fibroblasten (CAFs) bezeichnet wird, stillschweigend, wie Tumore entstehen, sich ausbreiten und auf Behandlungen reagieren. Dieser Übersichtsartikel erklärt, wie Forschende winzige 3D-Mini-Tumoren, so genannte Organoide, gemeinsam mit CAFs kultivieren, um dieses verborgene Gespräch zu enthüllen und klügere, präzisere Therapien zu entwickeln.
Winzige Tumore in der Schale
Die traditionelle Krebsforschung stützte sich häufig auf zweidimensionale Zellschichten in Plastikschalen oder auf Tiermodelle, die beide nur Teile der wirklichen Erkrankung abbilden. Organoide verändern dieses Bild. Es sind drei-dimensionale Cluster patientenabgeleiteter Tumorzellen, die viel von der ursprünglichen Tumorstruktur, der genetischen Ausstattung und dem Verhalten bewahren. Wenn diese Organoide gemeinsam mit CAFs kultiviert werden, beginnen sie, solide Tumore realistisch nachzubilden, einschließlich ihrer Reaktion auf Chemotherapie und Strahlentherapie. Es wurden verschiedene Kulturaufbauten entwickelt: einfache gelbasierte Systeme, in denen Tumorzellen und CAFs dieselbe Matrix teilen, gemischte "hanging drop"-Methoden, die zuerst kompakte Sphäroide bilden, und ausgeklügelte mikrofluidische Chips, die Fluss und Organoidgröße steuern und so Hochdurchsatz-Wirkstofftests ermöglichen. Jeder Ansatz balanciert Realitätsnähe, Kosten und technische Schwierigkeit aus.
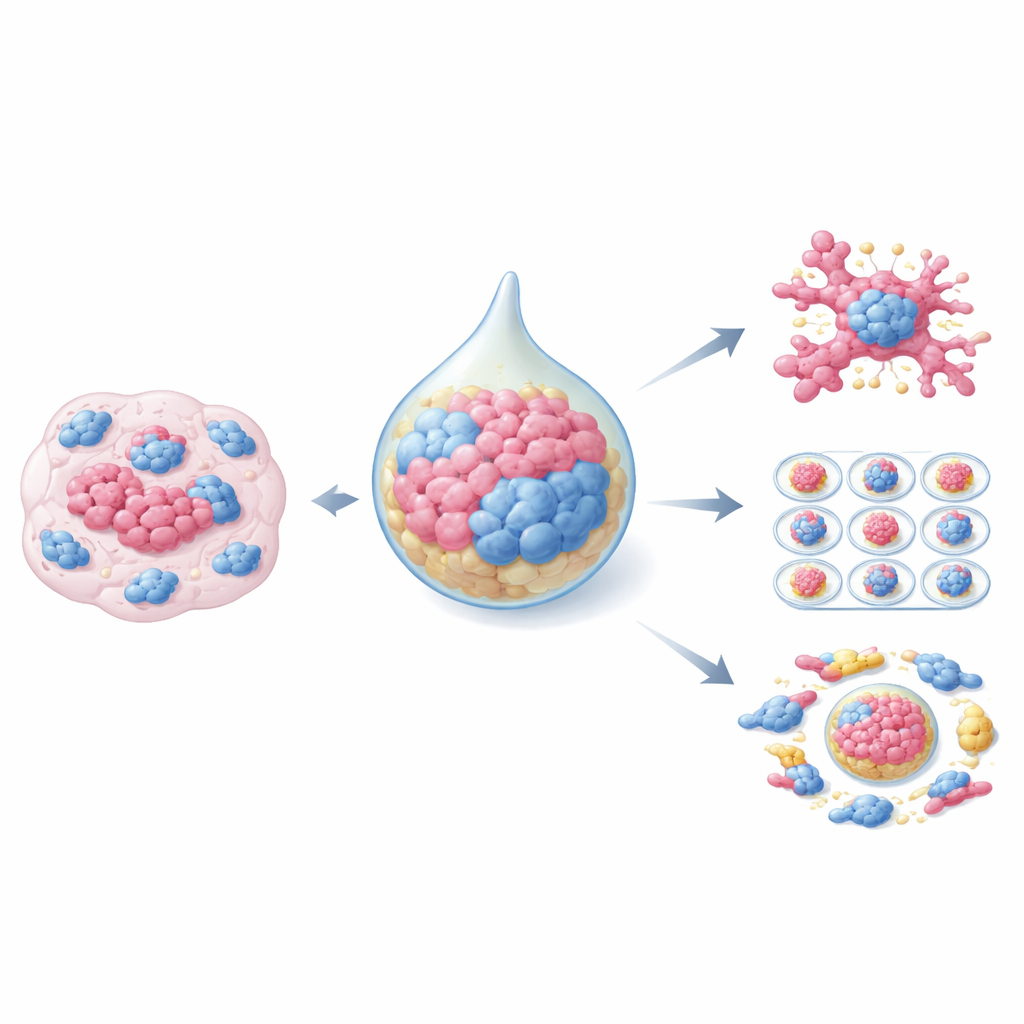
Wie Stützzellen Tumoren zum Gedeihen verhelfen
CAFs sind keine einheitliche Zellpopulation; sie treten in vielen Varianten auf, jede mit eigenen Aufgaben. In Ko-Kultur-Organoiden bauen CAFs das faserige Gerüst um Krebszellen auf und remodellieren es, wodurch Steifigkeit und Struktur so verändert werden, dass Tumorwachstum und Invasion begünstigt werden. Sie setzen ein Gemisch von Signalen frei, das Krebszellen zur Teilung, Bewegung und Invasion in benachbartes Gewebe antreibt, und sie können sogar gewöhnliche Zellen dazu bringen, stammzellähnliche Eigenschaften zu erlangen, die neue Tumore begründen. CAFs verändern auch, wie Krebszellen Energie herstellen und nutzen, indem sie Nährstoffe austauschen, um beide Partner unter Stress am Leben zu erhalten. In vielen Modellen machen CAFs Tumore resistenter gegen Chemotherapeutika und zielgerichtete Medikamente, etwa indem sie Krebszellen innerhalb dichter Kollagenmatrix abschirmen, Überlebenswege aktivieren oder kleine Vesikel mit RNA-Molekülen verschicken, die die DNA-Reparatur stärken.
Immunflucht und Blutversorgung
Über Versorgung und Schutz hinaus beeinflussen CAFs stark die Abwehrkräfte des Körpers. Ko-Kultur-Organoide und Organoid-on-a-Chip-Systeme zeigen, dass CAFs zytotoxische Immunzellen abwehren, immunsuppressive Partner anziehen und Immunzellen in Zustände treiben können, in denen sie nicht mehr angreifen. Einige CAF-Subtypen überladen natürliche Killerzellen mit Eisen und treiben sie in eine Form des Zelltods, während andere tumorunterstützende Makrophagen herbeirufen. Gleichzeitig fördern CAFs das Wachstum neuer Blutgefäße, indem sie Faktoren ausschütten, die gefäßbildende Zellen zum Auskeimen und Kanalbau anregen, sodass Tumore eine gleichmäßige Versorgung mit Sauerstoff und Nährstoffen erhalten. Die Geschichte ist jedoch nicht völlig einseitig: Manche seltenen CAF-Subtypen können die antitumorale Immunität unterstützen, indem sie T-Zellen aktivieren oder andere Immunzellen in einen nützlicheren Zustand umprogrammieren.
Ein zweiseitiges Gespräch mit Tumorzellen
Die Beziehung zwischen CAFs und Krebszellen ist eine Rückkopplungsschleife. Tumorzellen senden Signale aus, die benachbarte normale Fibroblasten in CAFs verwandeln und diese weiter in verschiedene Subgruppen formen, etwa kontraktile, matrixproduzierende Zellen oder entzündungsgetriebene Zellen, die viele Zytokine ausscheiden. Durch lösliche Faktoren und kleine Vesikel können Krebszellen CAFs in Zustände treiben, die das Gewebe versteifen, Invasion fördern und Arzneimittelresistenz antreiben. Ko-Kultur-Organoide haben gezeigt, wie spezifische Signalwege wie Drehregler wirken, die die Identität von CAFs verschieben und Tumoren erlauben, sich an veränderte Bedingungen oder Behandlungen anzupassen. Dieses Hin-und-Her zu verstehen ist entscheidend, denn grobe Ansätze, die einfach alle CAFs entfernen wollen, haben in einigen Tierstudien und klinischen Versuchen unerwartet das Tumorwachstum beschleunigt.
Neue Wege, die Tumornachbarschaft anzugreifen
Mit Organoid-Modellen, die die CAF–Tumor-Kommunikation bewahren, erforschen Wissenschaftlerinnen und Wissenschaftler feinere Behandlungsstrategien. Statt alle Fibroblasten zu vernichten, zielen einige Ansätze darauf ab, schädliche Signale zwischen CAFs und Krebszellen zu blockieren, ihren gemeinsamen Stoffwechsel zu stören oder CAFs behutsam so "umzuprogrammieren", dass sie harmloser oder sogar tumorhemmend werden. Experimentelle Taktiken umfassen kleine Moleküle, die CAF-Signalwege verändern, Wirkstoffe, die die faserige Hülle des Tumors erweichen oder verdünnen, und fortgeschrittene Zelltherapien wie gentechnisch veränderte Immunzellen, die bestimmte CAF-Subsets erkennen und angreifen. Organoid-basierte Plattformen ermöglichen es, diese Ideen an patientenabgeleitetem Gewebe im Labor zu testen und eröffnen einen Weg zu personalisierten Kombinationen, die sowohl Krebszellen als auch ihre unterstützende Nachbarschaft ansprechen.
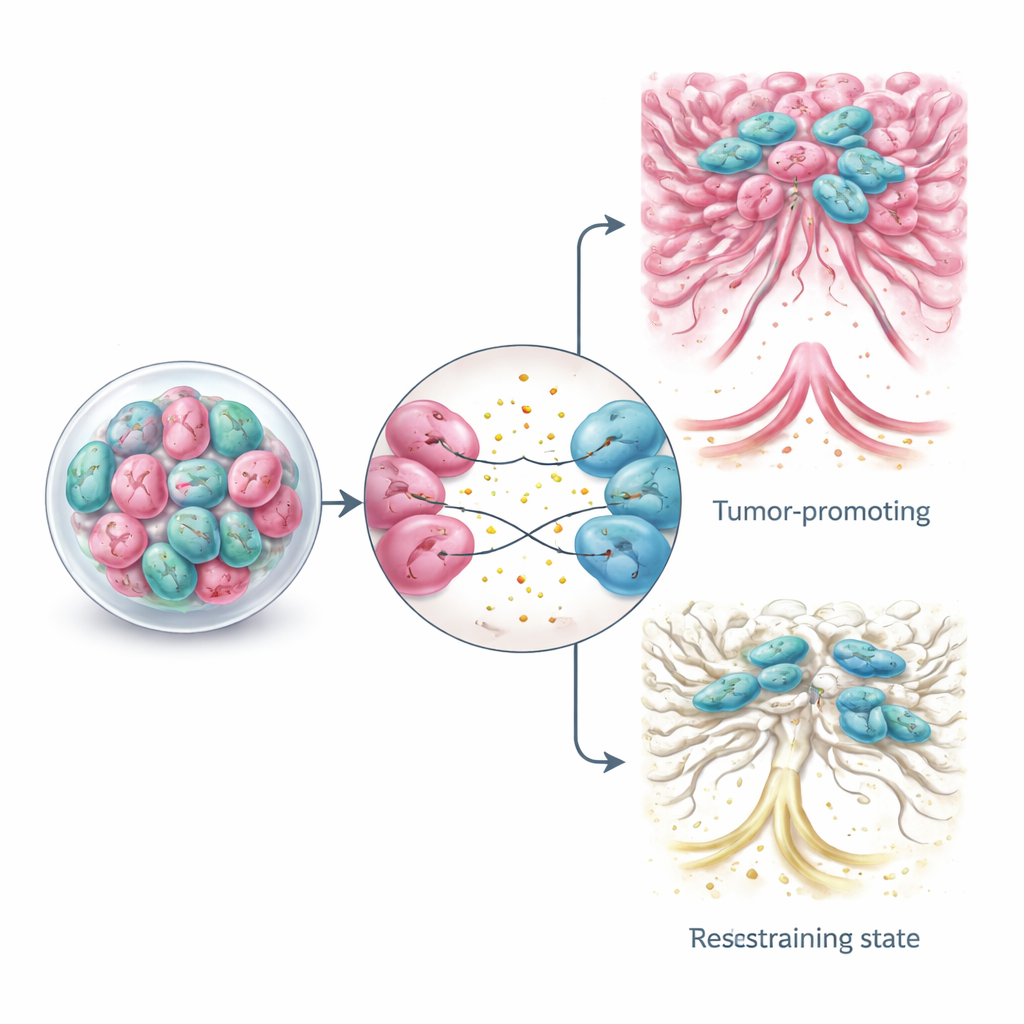
Was das für die künftige Krebsbehandlung bedeutet
Diese Übersichtsarbeit schließt mit der Feststellung, dass CAFs zugleich mächtige Helfer und mitunter stille Gegenspieler des Krebses sind. Ihre Diversität und Flexibilität erklären, warum einfache "CAF-auslöschende" Behandlungen oft versagt haben und mitunter Schaden anrichteten. Indem Ko-Kultur-Organoide als realistische Prüfstände genutzt werden, können Forschende nun gutes von schlechtem CAF-Verhalten trennen, die Signale kartieren, die sie mit Tumorzellen verbinden, und Therapien entwerfen, die tumorfördernde Rollen selektiv blockieren, während schützende Funktionen erhalten oder verstärkt werden. Für Patientinnen und Patienten legt diese Arbeit den Grundstein für genauere Medikamententests und Kombinationsbehandlungen, die nicht nur den Tumor angreifen, sondern auch die Nachbarschaft umgestalten, die sein Gedeihen ermöglicht.
Zitation: Wang, M., Ding, X., Chen, L. et al. The research advances of crosstalk between cancer-associated fibroblasts and tumor cells using co-culture organoids. Cell Death Dis 17, 267 (2026). https://doi.org/10.1038/s41419-026-08512-8
Schlüsselwörter: tumorumgebungsassoziierte Fibroblasten, Tumororganoide, Tumormikroumgebung, Therapieresistenz, 3D-Ko-Kultur-Modelle