Clear Sky Science · de
Ubenimex wirkt synergistisch mit der PD-L1-Blockade bei Magenkrebs durch kompetitive Bindung von LAP3 an UBE3A
Warum diese Forschung wichtig ist
Für viele Menschen mit fortgeschrittenem Magenkrebs haben moderne Immuntherapien, die dem Immunsystem "die Bremsen lösen", neue Hoffnung gebracht — dennoch profitieren weiterhin nur eine Minderheit der Patienten. Diese Studie stellt eine praxisrelevante Frage mit unmittelbarer Wirkung: Kann ein älteres immunstimulierendes Medikament, Ubenimex, umfunktioniert werden, um diese Therapien wirksamer zu machen, und warum würde das helfen? Die Forscher decken einen versteckten molekularen Mechanismus auf, den Tumoren zur Flucht vor der Immunabwehr nutzen, und zeigen, wie Ubenimex diesen Mechanismus rückgängig machen kann, was den Weg für effektivere Kombinationstherapien öffnet.
Ein neuer Partner für die Krebsimmuntherapie
Die Arbeit konzentriert sich auf Magenkrebs, eine Erkrankung, die weiterhin verbreitet und tödlich ist, besonders in China. Medikamente, die PD-1 oder PD-L1 blockieren — Proteine, die Immunantworten dämpfen — sind inzwischen eine Behandlungsgrundlage. Dennoch sprechen die meisten Patienten entweder gar nicht an oder erleiden später Rückfälle. Die Autoren richteten ihr Augenmerk auf Ubenimex, ein seit langem zugelassenes Medikament, das ergänzend zu Chemotherapie und Bestrahlung eingesetzt wird und dafür bekannt ist, Immunzellen zu stimulieren. Sie fragten, ob die Kombination von Ubenimex mit PD-L1-blockierenden Antikörpern Tumoren anfälliger für Angriffe durch zytotoxische T-Zellen machen könnte, jene Immunzellen, die Krebszellen direkt zerstören.
Erprobung der Medikamentenkombination
In einem Mausmodell von Magenkrebs, in dem Tumoren so verändert wurden, dass sie vermehrt das Protein LAP3 produzieren, behandelte das Team die Tiere mit Ubenimex, Anti–PD-L1, beidem oder keinem der Mittel. Jede Monotherapie verkleinerte die Tumoren, doch die Kombination stach hervor: In allen behandelten Mäusen kam es zu kompletter Tumorregression, und das Überleben verbesserte sich stärker als bei alleiniger PD-L1-Blockade. Immunanalysen zeigten, dass die Kombination die Zahl und Aktivität von CD8-"Killer"-T-Zellen deutlich steigerte; diese sezernierten mehr toxische Moleküle und entzündliche Botenstoffe. Wichtig ist, dass die Behandlung keine offensichtlichen Leberschäden oder Gewichtsverluste verursachte, was nahelegt, dass der Ansatz kraftvoll, aber nicht übermäßig belastend sein könnte.
Ein verborgener Schalter, der Tumoren schützt
Um zu verstehen, warum Ubenimex half, fokussierten die Forscher auf LAP3, ein Enzym, das es hemmt. Sie fanden heraus, dass LAP3 in menschlichen Magenstumoren höher ist als in normalem Magengewebe und dass Patienten mit erhöhtem LAP3 tendenziell eine schlechtere Überlebensprognose haben. In Patientenproben und Maus-Tumoren ging ein hoher LAP3-Spiegel mit weniger intratumoralen CD8-T-Zellen einher, während andere Immunzelltypen unverändert blieben. Wenn LAP3 experimentell in Tumorzellen reduziert wurde, wuchsen die Tumoren langsamer, zogen mehr CD8-T-Zellen an und wurden in Labortests leichter von diesen Zellen zerstört. Zusammengenommen sprechen die Daten dafür, dass LAP3 kein zufälliger Begleiter, sondern ein aktiver Förderer der Immunflucht ist.
Wie Tumoren LAP3 nutzen, um die Bremsen anzuziehen
Bei genauerer Untersuchung gelang dem Team, wie LAP3 Tumorzellen vor Immunangriff schützt. Sie entdeckten, dass LAP3 dazu beiträgt, PD-L1 zu stabilisieren, das zentrale "Brems"-Protein auf Krebszellen, das T-Zellen ausschaltet. Normalerweise kann PD-L1 mit kleinen Proteinmarkern versehen werden, die es zur zellulären Abbaumaschinerie schicken. Ein Enzym namens UBE3A heftet diese Marker an und leitet so den Abbau von PD-L1 ein. LAP3 bindet physisch an UBE3A und verhindert dadurch, dass UBE3A PD-L1 markiert. Infolgedessen akkumuliert PD-L1 an der Tumoroberfläche und bildet einen Schutzschild gegen CD8-T-Zellen. Wenn LAP3 gesenkt oder seine Aktivität blockiert wird, wird PD-L1 stärker markiert, schneller abgebaut und seine Oberflächenmenge sinkt — wodurch T-Zellen näher kommen und angreifen können.
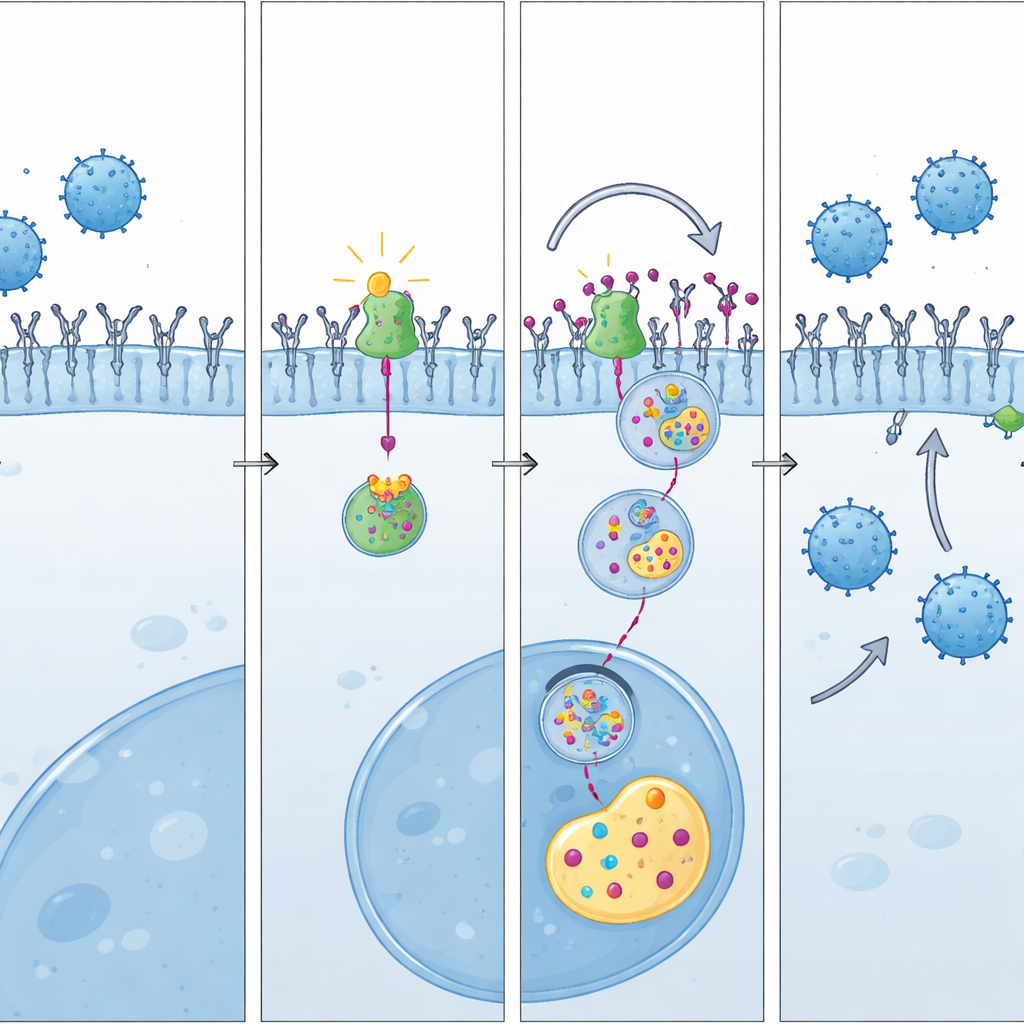
Wie Ubenimex das Gleichgewicht verschiebt
Die Studie zeigt weiter, dass Ubenimex wirkt, indem es die LAP3–UBE3A-Partnerschaft stört. Computermodelle und biochemische Experimente deuten darauf hin, dass Ubenimex sich in LAP3 an derselben Region festsetzt, über die LAP3 normalerweise mit UBE3A interagiert. Diese kompetitive Bindung löst UBE3A von LAP3, sodass UBE3A frei wird, PD-L1 zu markieren und zum Abbau zu führen. In Zellexperimenten verringerte Ubenimex die Menge an PD-L1 auf der Tumoroberfläche, erhöhte die Markierung von PD-L1 für den Abbau und kehrte die PD-L1-steigernden Effekte von überschüssigem LAP3 um. In lebenden Mäusen übersetzte sich diese molekulare Verschiebung in mehr aktive CD8-T-Zellen und eine auffällige Tumorkontrolle, wenn Ubenimex mit einer PD-L1-Blockade kombiniert wurde.
Welche Bedeutung das für Patienten hat
Insgesamt zeichnet die Studie ein klares Bild: Viele Magenstumoren produzieren zu viel LAP3, wodurch sie hohe PD-L1-Spiegel aufrechterhalten und sich so vor dem Immunsystem verbergen. Ubenimex durchbricht diesen Schutz, indem es den Griff von LAP3 auf UBE3A blockiert und dadurch die Entfernung von PD-L1 ermöglicht. Mit weniger Bremsen auf der Oberfläche der Krebszellen können PD-L1-blockierende Medikamente und zytotoxische T-Zellen wesentlich effektiver zusammenarbeiten. Da Ubenimex bereits klinisch verwendet wird und LAP3 in Tumorproben messbar ist, liefert diese Forschung eine konkrete, überprüfbare Strategie zur Verbesserung der Immuntherapie bei Magenkrebs und möglicherweise auch bei anderen Tumoren mit erhöhtem LAP3.
Zitation: Zhao, C., Li, J., Zheng, J. et al. Ubenimex synergizes with the PD-L1 blockade in gastric cancer by competitively binding LAP3 with UBE3A. Cell Death Dis 17, 241 (2026). https://doi.org/10.1038/s41419-026-08509-3
Schlüsselwörter: Magenkrebs, Immuntherapie, PD-L1, Ubenimex, LAP3