Clear Sky Science · de
CCL11 fördert das Wiederauftreten von hepatozellulärem Karzinom nach Operation durch Verstärkung immunsuppressiver CCR5 + CD206 + M2‑ähnlicher Makrophagen und Förderung der Tumorinvasivität
Warum Leberkrebs nach einer Operation zurückkehren kann
Leberoperationen sind oft die beste Hoffnung für Menschen mit Leberkrebs im Frühstadium, doch viele Patientinnen und Patienten erleben ein Wiederauftreten ihres Tumors innerhalb weniger Jahre. Diese Studie stellt eine einfache, aber entscheidende Frage: Unterstützt die körpereigene Entzündungsreaktion nach einer Operation unbeabsichtigt das Wachstum und die Ausbreitung verbleibender Krebszellen? Die Forschenden konzentrieren sich auf ein Signalmolekül namens CCL11 und zeigen, wie ein Anstieg dieses Moleküls nach der Operation sowohl die anti‑tumorale Immunabwehr schwächt als auch überlebende Tumorzellen aggressiver macht.
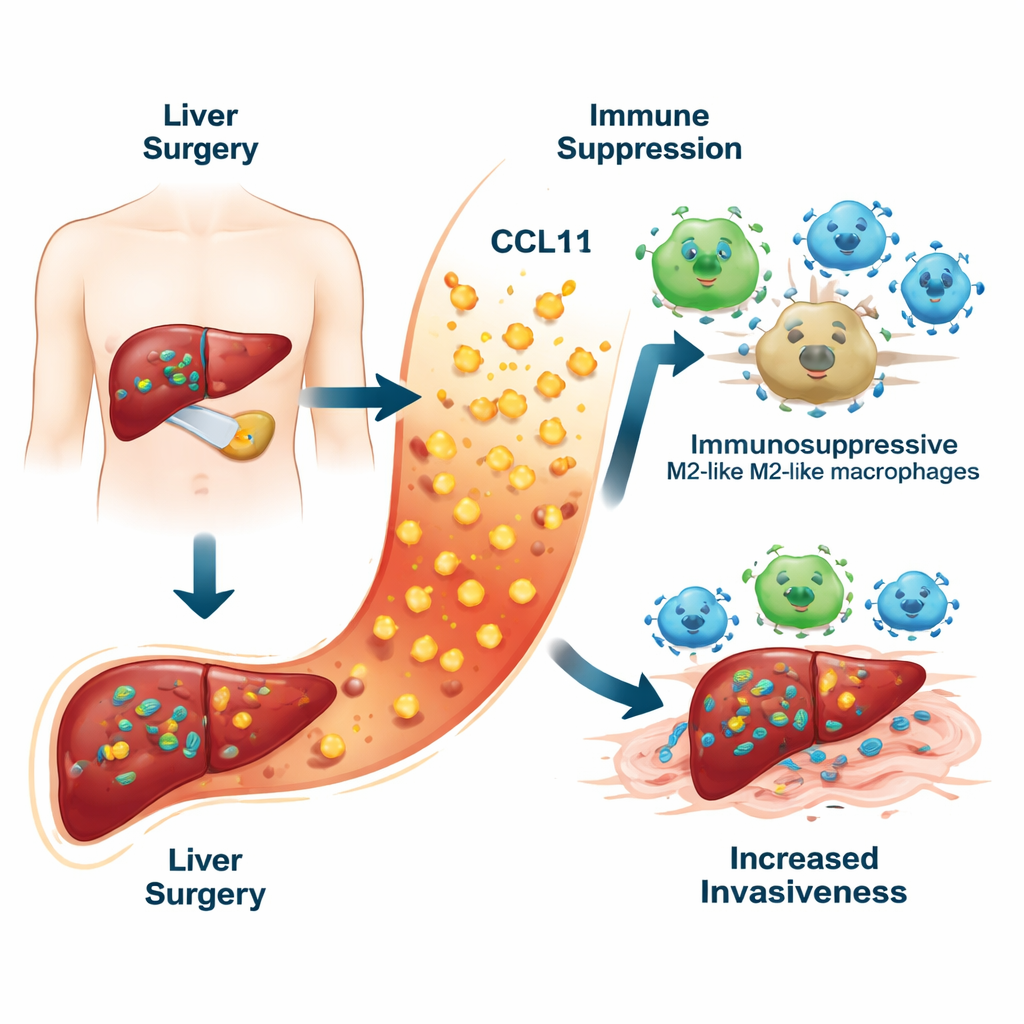
Eine verborgene Gefahr in der Heilungsreaktion
Wenn Chirurgen einen Lebertumor entfernen, müssen sie Blutgefäße klemmen und umliegendes Gewebe verletzen. Diese Schädigung löst eine Entzündungswelle aus, die die Leber bei der Heilung unterstützt. Durch die Messung von zehn verschiedenen Entzündungsmediatoren im Blut von Patientinnen und Patienten eine Woche nach der Operation stellte das Team fest, dass ein Chemokin, CCL11, besonders auffiel. Patientinnen und Patienten, bei denen der Leberkrebs später wiederkehrte, hatten deutlich höhere CCL11‑Spiegel als diejenigen, die krebsfrei blieben. Hohe CCL11‑Werte waren zudem mit schlechterem Überleben verbunden. Kombinierten die Forschenden CCL11 mit routinemäßigen klinischen Daten wie Bluttests und Tumorcharakteristika, entstand eine Risik‑„Scorecard“, die das Fünf‑Jahres‑Rezidiv genauer vorhersagte als traditionelle Modelle.
Das normal aussehende Lebergewebe ist trotzdem wichtig
In der Krebsforschung richtet sich die meiste Aufmerksamkeit auf den Tumor selbst, doch diese Studie zeigt, dass das umgebende „normal“ wirkende Lebergewebe mindestens genauso bedeutsam sein kann. In Proben von über 100 Patientinnen und Patienten war CCL11 tatsächlich in nicht‑tumoralem Lebergewebe höher als in den Krebsknötchen oder in gespendeten, gesunden Lebern. Patientinnen und Patienten, deren angrenzendes Lebergewebe mehr CCL11 produzierte, hatten häufiger fortgeschrittene Erkrankung, Fernmetastasen und Rezidive nach der Operation. In Mausmodellen, die den kurzzeitigen Verlust und die Wiederherstellung der Durchblutung während eines Eingriffs nachahmen, stieg CCL11 nach Leberverletzung rasch an. Unter niedrigen Sauerstoffbedingungen im Labor produzierten leberstützende Zellen wie Myofibroblasten und Endothelzellen ebenfalls mehr CCL11, was nahelegt, dass operativer Stress das gesamte verbleibende Lebergewebe zu einer tumorfördernden Umgebung präpariert.
Wie CCL11 Immunverteidiger zu Beobachtern macht
Um zu untersuchen, wie CCL11 die Immunantwort formt, zoomten die Autorinnen und Autoren auf Makrophagen, vielseitige weiße Blutkörperchen, die Tumoren angreifen oder schützen können. Sie fanden, dass in nicht‑tumoralem Lebergewebe höheres CCL11 mit einem Anstieg eines Makrophagen‑Subtyps einherging, der das Markerprotein CCR5 trägt und ein sogenanntes M2‑ähnliches, tumorförderndes Profil zeigt. Bei Patientinnen und Patienten waren Lebern mit vielen CCR5+ M2‑ähnlichen Makrophagen mit schlechterem Überleben verknüpft. In Zellkulturen trieb die Zugabe von CCL11 Monozyten in diesen immunsuppressiven Makrophagen‑Typ, erhöhte Moleküle wie PD‑L1 und IL‑10 und setzte weitere Signale frei, die zusätzliche Immunzellen anziehen und umlenken. Diese durch CCL11 konditionierten Makrophagen förderten dann, dass naive Helfer‑T‑Zellen sich in regulatorische T‑Zellen umwandeln — eine Population, die anti‑tumorale Reaktionen dämpft. Mechanistische Experimente zeigten, dass CCL11 eine Signalkette in Makrophagen aktiviert, die im NF‑κB‑Weg und in der PD‑L1‑Produktion mündet und so Krebszellen vor Immunangriffen schützt.
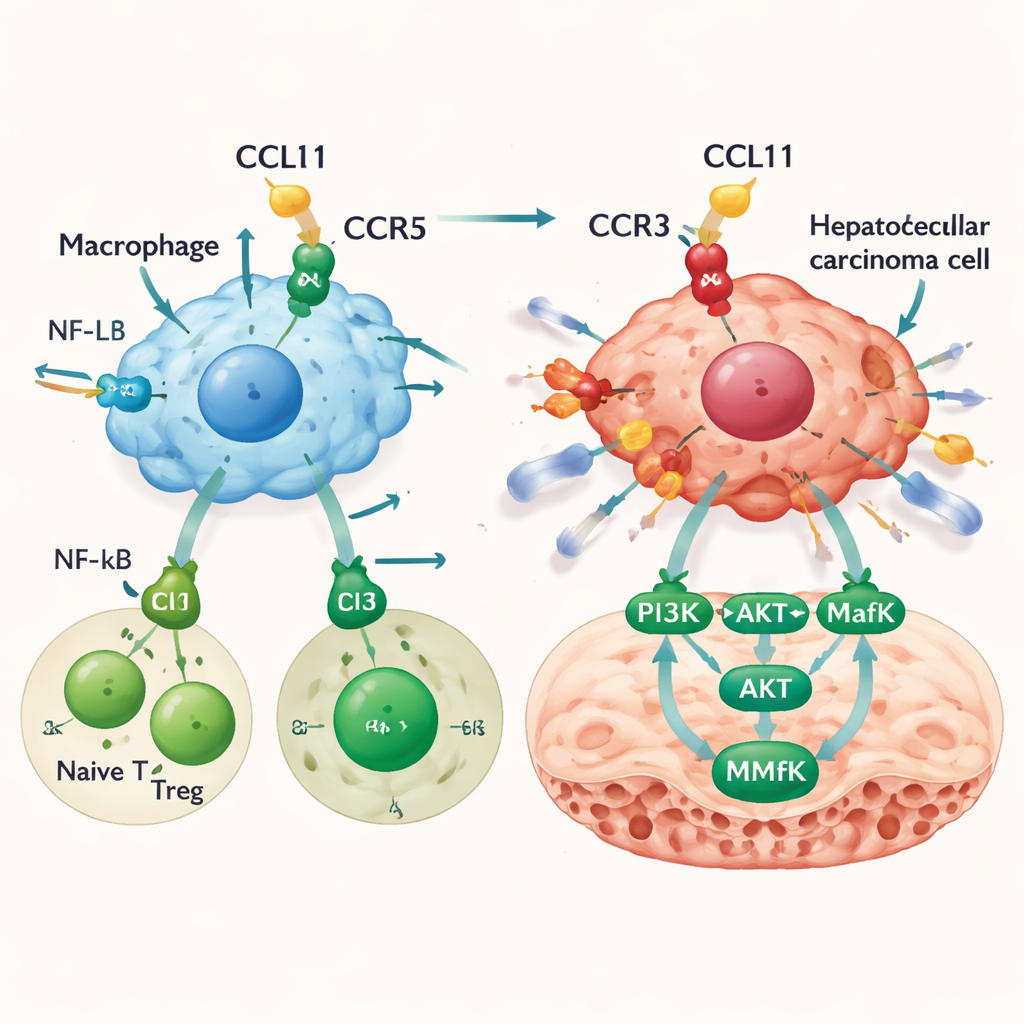
Wie CCL11 verbleibende Krebszellen invasiver macht
CCL11 formt nicht nur die Immunlandschaft, es wirkt auch direkt auf Leberkrebszellen. Obwohl die Krebszellen selbst nur wenig CCL11 produzieren, tragen sie einen seiner Rezeptoren, CCR3. In Laborversuchen beschleunigte CCL11 nicht das Wachstum von Leberkrebszellen, machte sie aber deutlich beweglicher und invasiver — ein Kennzeichen für metastatische Potenz. Die Blockade des CCR3‑Rezeptors hob diesen Effekt größtenteils auf. Genanalysen deuteten auf einen Weg hin, in dem CCL11–CCR3‑Signalgebung PI3K und AKT aktiviert, was dann den Transkriptionsfaktor MafK hochfährt. MafK steigert wiederum die Produktion von MMP13, einem Enzym, das umliegendes Gewebe abbaut und Wege für die Tumorausbreitung öffnet. In Mausmodellen führte die Zuführung von CCL11 in die Leber zu höherer Tumorlast und mehr Metastasen sowie zu erhöhten Aktivitätswerten des PI3K–AKT–MafK–MMP13‑Pfads in den Tumoren.
Aus einem riskanten Signal eine therapeutische Chance machen
Da CCL11 offenbar sowohl die Immunabwehr stumm schaltet als auch verbleibende Krebszellen robuster macht, prüften die Forschenden, ob eine Blockade nach der Operation die Ergebnisse verändern könnte. Bei Mäusen mit zuvor chirurgisch entfernten Lebertumoren reduzierte eine Behandlung mit einem neutralisierenden Antikörper gegen CCL11 die Rückfallrate in der Leber dramatisch und verbesserte das Überleben, ohne offensichtliche Nebenwirkungen wie Gewichtsverlust. Insgesamt präsentieren die Befunde CCL11 als einen Hauptschalter, der operative Verletzung mit einer immunsuppressiven, invasionsfördernden Leberumgebung verknüpft. Für Patientinnen und Patienten legt diese Arbeit nahe, dass die Messung von CCL11 nach der Operation helfen könnte, jene mit dem höchsten Rückfallrisiko zu identifizieren, und dass Medikamente, die die CCL11–CCR5/CCR3‑Achse blockieren, eines Tages Teil von Strategien werden könnten, um ein Wiederauftreten von Leberkrebs zu verhindern.
Zitation: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Schlüsselwörter: Rückfall von Leberkrebs, CCL11 Chemokin, Tumormikroumgebung, Immunsuppression, Krebsmetastasen