Clear Sky Science · de
Mit Krebs assoziierte Fibroblasten fördern Osimertinib‑Resistenz in non‑small cell Lungenkrebszellen über METTL1‑vermittelte NET1‑m7G‑Modifikation
Warum einige Lungenkrebserkrankungen auf ein „intelligentes“ Medikament nicht mehr ansprechen
Gezielte Medikamente wie Osimertinib haben die Behandlung vieler Menschen mit einer häufigen Form von Lungenkrebs verändert und bieten länger Leben mit weniger Nebenwirkungen als die klassische Chemotherapie. Für die meisten Patientinnen und Patienten sind diese Vorteile jedoch nur vorübergehend: Tumore finden schließlich Wege, das Medikament zu umgehen. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Unterstützt das Stützgewebe des Tumors — konkret Zellen, die als mit Krebs assoziierte Fibroblasten bezeichnet werden — heimlich die Krebszellen dabei, der Wirkung von Osimertinib zu entkommen?
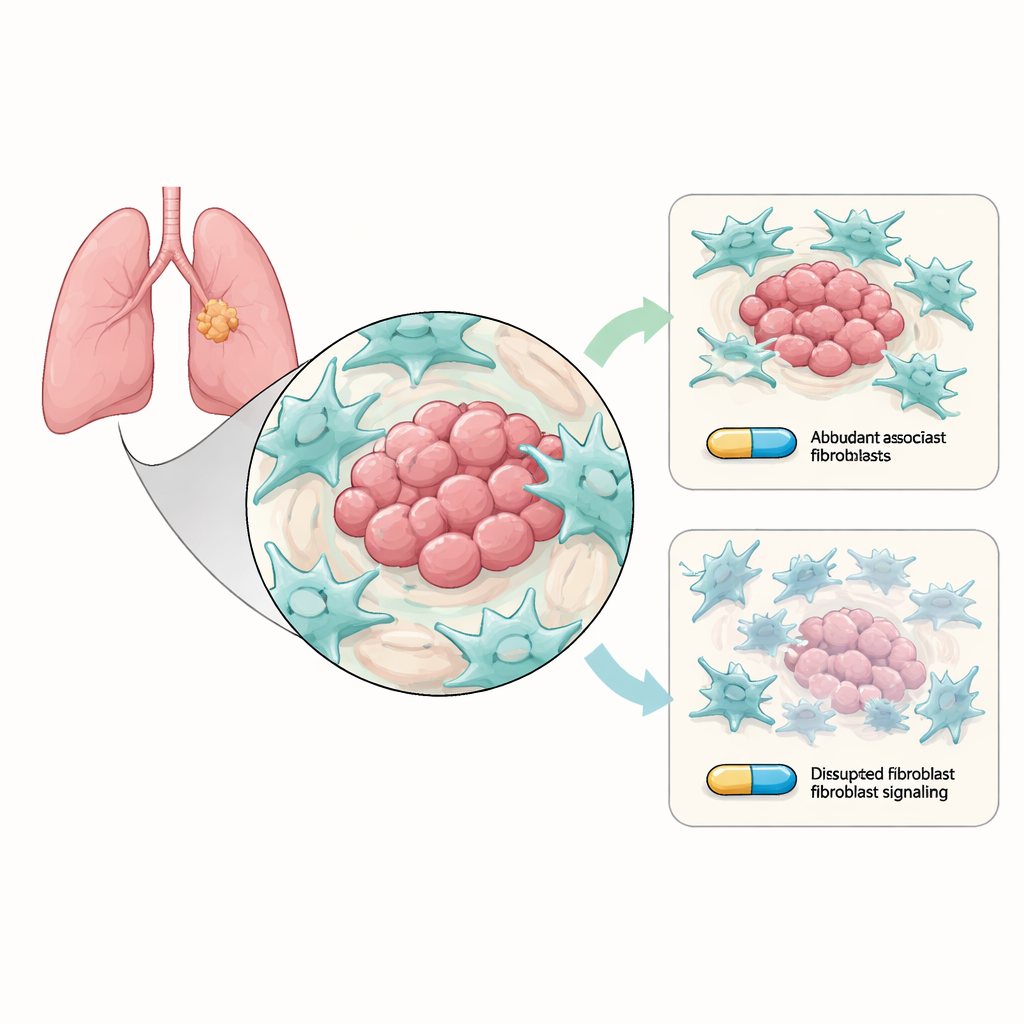
Hilfszellen, die den Tumor heimlich abschirmen
Nicht‑kleinzelliger Lungenkrebs wächst in einer belebten Nachbarschaft aus nicht‑krebsartigen Zellen, der sogenannten Tumormikroumgebung. Zu den häufigsten Bewohnern gehören mit Krebs assoziierte Fibroblasten (CAFs), Bindegewebszellen, die das Umfeld des Tumors umgestalten. Die Forschenden kultivierten Lungenkrebszellen mit den typischen Osimertinib‑empfindlichen EGFR‑Mutationen gemeinsam mit CAFs im Labor. Sie stellten fest, dass Krebszellen in Gegenwart von CAFs schwerer durch Osimertinib zu beseitigen waren: Sie bildeten mehr Kolonien, unterlagen seltener dem programmierten Zelltod und zeigten stärkere „stammzellartige“ Merkmale, die mit Langzeitüberleben und Rückfall in Verbindung stehen. Anders gesagt: Obwohl das Medikament weiterhin die Krebszellen angriff, halfen die umgebenden Fibroblasten ihnen im Stillen, zu überdauern.
Ein chemisches Kennzeichen auf RNA, das die Regeln verändert
Das Team blickte dann über die Gene selbst hinaus auf chemische Kennzeichnungen der RNA — die Arbeitskopien genetischer Information in der Zelle. Eine solche Kennzeichnung, genannt m7G, kann beeinflussen, wie stabil ein RNA‑Molekül ist und wie effizient es in Protein übersetzt wird. Mithilfe biochemischer Tests und genomweiter Kartierungen zeigten die Forschenden, dass CAFs die Gesamtmenge an m7G‑Markierungen auf RNAs in Lungenkrebszellen erhöhen. Dieser Anstieg wurde vor allem von einer Methyltransferase‑Enzym namens METTL1 getragen, das m7G‑Marken auf messenger RNAs anbringt. METTL1‑Spiegel waren in Lungen‑Tumoren höher als im umliegenden Normalgewebe und korrelierten mit fortgeschrittenerer Erkrankung und schlechterer Patient*innen‑Prognose, was darauf hindeutet, dass dieses Enzym mehr bewirkt als nur Feinabstimmung grundlegender Zellfunktionen.
Ein ausgeschüttetes Signal und eine verwundbare molekulare Kette
Wie erhöhen CAFs METTL1 in Krebszellen? Die Studie weist auf ein Protein namens HMGB1 hin, das CAFs in ihr Umfeld abgeben. Im Vergleich zu Krebszellen schütteten CAFs deutlich größere Mengen an HMGB1 aus. Wenn die Forschenden HMGB1 zu Lungenkrebszellen hinzufügten, stiegen METTL1‑Spiegel und m7G‑Marken; wenn sie HMGB1 in CAF‑konditioniertem Medium blockierten, verschwand dieser Effekt wieder. Im Detail identifizierten sie ein zentrales RNA‑Ziel von METTL1: NET1, ein Gen, das Zellwachstum und ‑bewegung fördert. CAFs erhöhten sowohl die m7G‑Markierung als auch die Menge von NET1‑RNA und ‑Protein, und METTL1 band sich physisch an NET1‑RNA, um sie zu stabilisieren. Weniger METTL1 führte zu weniger modifiziertem NET1, abgeschwächten Überlebenssignalen in den Krebszellen und einer höheren Empfindlichkeit gegenüber Osimertinib.
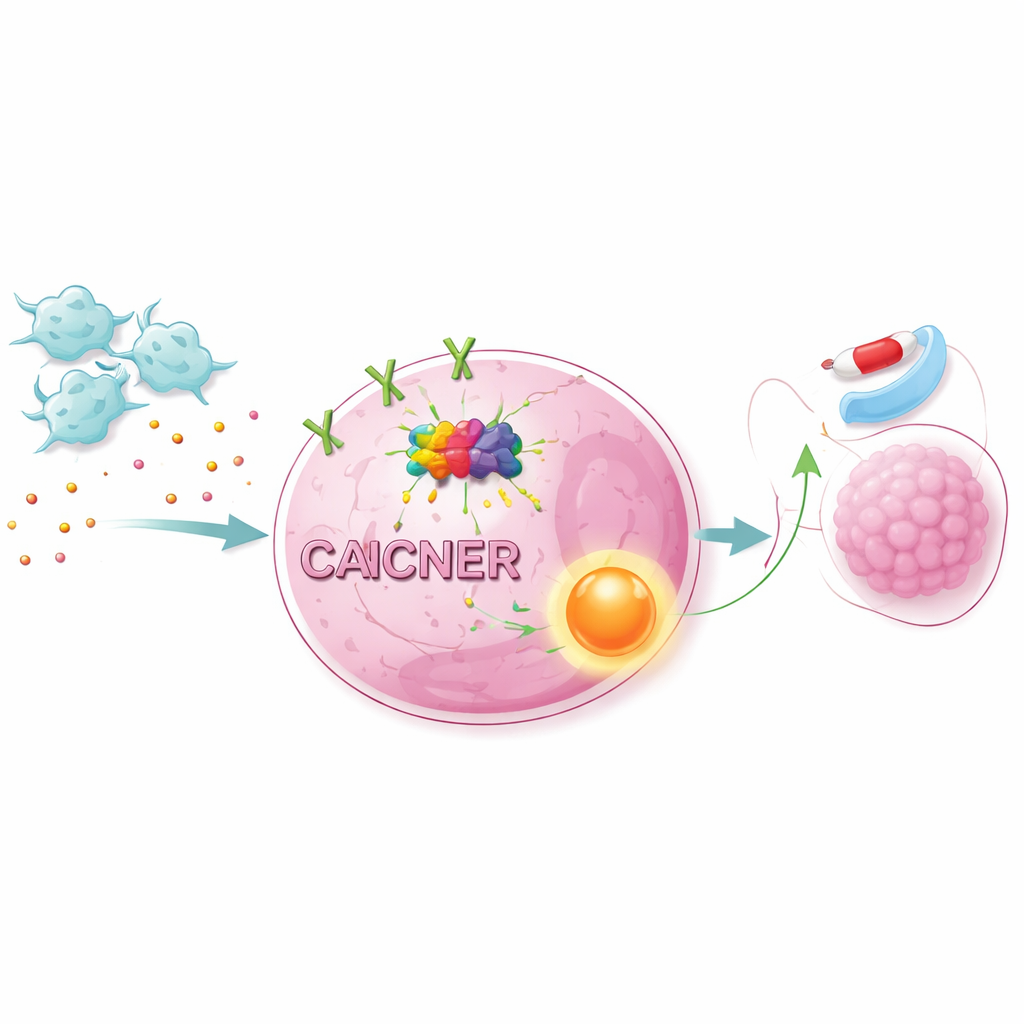
Aktivierung von Überlebenswegen innerhalb der Krebszellen
Das verstärkte NET1‑Signal wirkte nicht allein. Durch die Kombination groß angelegter RNA‑Daten mit Pfadanalyse zeigten die Wissenschaftlerinnen und Wissenschaftler, dass CAFs einen wichtigen Wachstums‑ und Überlebensweg innerhalb der Zellen aktivieren, bekannt als AKT/NF‑κB‑Signalweg. Die Blockade von AKT oder NF‑κB mit spezifischen Inhibitoren machte Lungenkrebszellen anfälliger für Osimertinib, selbst in Anwesenheit von CAFs. Die Veränderung der NET1‑Spiegel hatte ähnliche Effekte: Die Reduktion von NET1 schwächte den CAF‑Schutz, wohingegen eine Erhöhung von NET1 die Resistenz verstärkte. In Mäusen, die mit menschlichen Lungenkrebszellen beimpflanzt waren, führten hinzugefügte CAFs zu schnellerem Tumorwachstum und geringerer Ansprechrate auf Osimertinib. Das Herunterregulieren von METTL1 in den Krebszellen verringerte die m7G‑Marken, senkte NET1 und die Aktivierung des Signalwegs und reduzierte das CAF‑getriebene Tumorwachstum deutlich.
Was das für die zukünftige Behandlung von Lungenkrebs bedeutet
Für Menschen mit EGFR‑mutiertem Lungenkrebs bietet diese Arbeit eine neue Perspektive darauf, warum potente Medikamente wie Osimertinib schließlich versagen. Anstatt nur neue Mutationen in Krebszellen verantwortlich zu machen, hebt sie eine molekulare Kette hervor, die außerhalb der Tumorzelle beginnt — mit CAFs, die HMGB1 freisetzen — und über METTL1, m7G‑Marken auf NET1 und die Aktivierung von Überlebenswegen läuft, die die Wirkung des Medikaments abschwächen. Das Unterbrechen dieser Kette an einem beliebigen Punkt könnte theoretisch die Empfindlichkeit gegenüber der Behandlung wiederherstellen oder verlängern. Während Wirkstoffe, die direkt METTL1, HMGB1 oder spezifische m7G‑markierte RNAs angreifen, noch in frühen Entwicklungsphasen sind, legt die Studie nahe, dass die Kombination von Osimertinib mit Therapien, die auf die unterstützenden Zellen des Tumors oder deren RNA‑modifizierende Signale abzielen, dazu beitragen könnte, diese Form von Lungenkrebs länger unter Kontrolle zu halten.
Zitation: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Schlüsselwörter: Osimertinib-Resistenz, nicht‑kleinzelliger Lungenkrebs, mit Krebs assoziierte Fibroblasten, RNA‑Methylierung, METTL1‑NET1‑Signalweg