Clear Sky Science · de
miR-424(322)~503 beeinträchtigt das Fortschreiten von Darmkrebs, das durch PTEN-Mangel getrieben wird
Warum diese Studie für Darmkrebs wichtig ist
Darmkrebs bleibt eine der weltweit häufigsten und tödlichsten Krebserkrankungen, und viele Patienten entwickeln weiterhin fortgeschrittene Stadien trotz Operation, Chemotherapie und zielgerichteter Medikamente. Diese Studie untersucht eine winzige Gruppe genetischer „Dimmerschalter“, sogenannte microRNAs, die das Tumorwachstum verlangsamen oder beschleunigen können. Indem sie aufdeckt, wie ein spezifischer microRNA‑Cluster mit dem bekannten Tumorsuppressor PTEN interagiert, hilft die Arbeit zu erklären, warum manche Darmkrebserkrankungen aggressiver werden, und weist auf neue Wege hin, Risiko vorherzusagen und Therapien zu entwickeln.
Kleine RNA‑Schalter mit großer Wirkung
MicroRNAs sind kurze RNA‑Moleküle, die keine Proteine kodieren, aber fein regulieren, wie hunderte Gene in einer Zelle genutzt werden. Der Cluster miR‑424(322)~503, bestehend aus zwei verwandten microRNAs, beschäftigt Forscher, weil er in verschiedenen Krebsarten entweder als Bremse oder als Beschleuniger wirken kann. Bei Darmkrebs war seine Rolle unklar. Die Autoren konzentrierten sich auf Tumoren, die durch den Verlust von PTEN angetrieben werden — einem Gen, das normalerweise Wachstumssignale unter Kontrolle hält und in Darmtumoren häufig verändert ist. Sie stellten eine einfache, aber aussagekräftige Frage: Was passiert mit der Entwicklung von Darmkrebs, wenn sowohl PTEN als auch dieser microRNA‑Cluster fehlen?
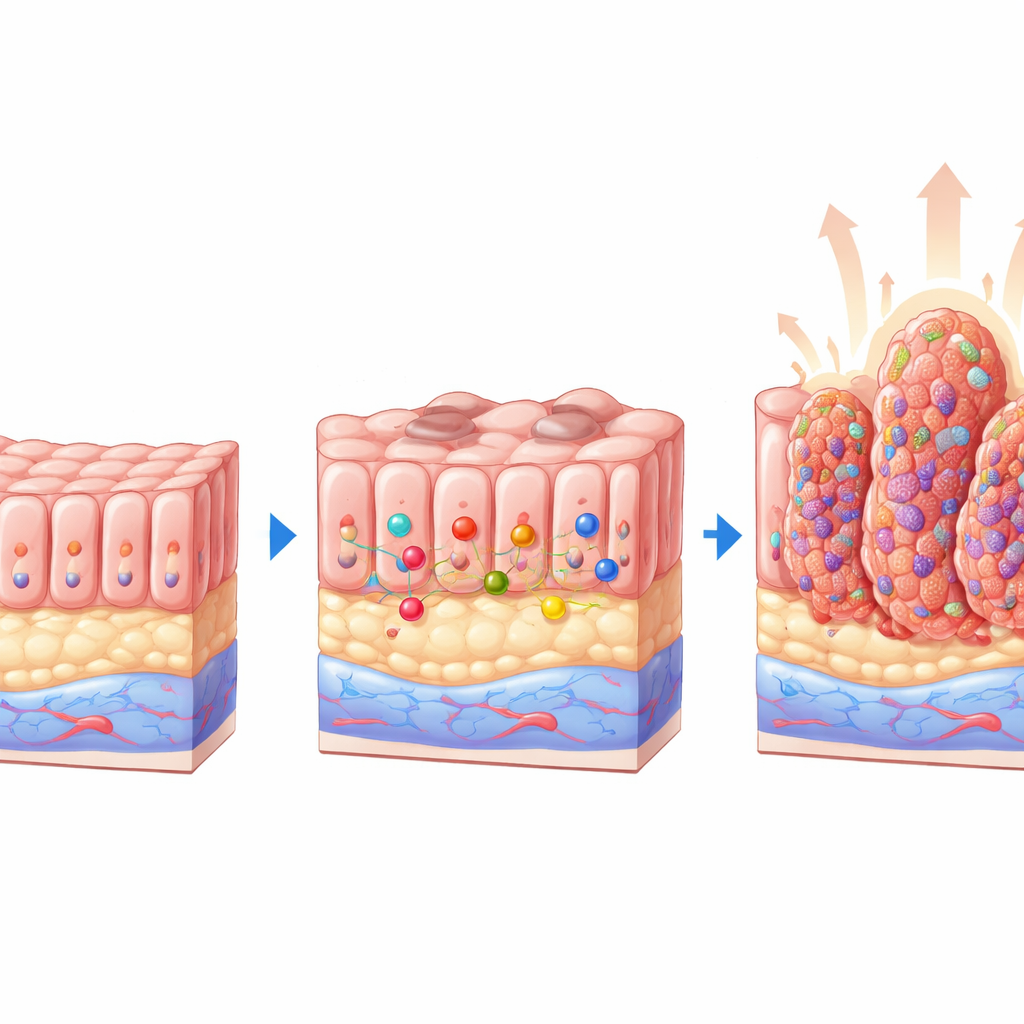
Mausmodelle zeigen eine schützende Rolle
Um das zu beantworten, nutzte das Team genetisch veränderte Mäuse, bei denen PTEN im Darmepithel abgeschaltet werden kann, und kreuzte sie mit Mäusen, denen der miR‑424(322)~503‑Cluster fehlt. So entstanden vier Gruppen: normale Tiere, Mäuse, denen nur die microRNAs fehlen, Mäuse mit alleinigem PTEN‑Verlust und doppelte Knockout‑Tiere, denen beide fehlen. Nach dem Auslösen des PTEN‑Verlusts untersuchten sie die Därme gründlich. Tiere mit nur PTEN‑Verlust entwickelten mehrere kleine Polypen, viele mit frühem Gewebeverfall. Im auffälligen Kontrast dazu hatten Mäuse ohne sowohl PTEN als auch den microRNA‑Cluster deutlich mehr Läsionen, größere Polypen und einen höheren Anteil fortgeschrittener Veränderungen, einschließlich hochgradiger Dysplasie und offensichtlichem Adenokarzinom. Der microRNA‑Cluster allein verursachte keine Krankheit, was zeigt, dass sein Verlust besonders schädlich ist, wenn PTEN bereits fehlt.
Unveränderte klassische Bahn, Hinwendung zu neuen Verdächtigen
Darmkrebs wird häufig durch Überaktivierung des Wnt/β‑Catenin‑Signals getrieben, einem zentralen Weg zur Kontrolle von Stammzellen im Darm. Weil dieser microRNA‑Cluster dieses System im Brustgewebe beeinflussen kann, prüften die Autoren, ob dies hier ebenfalls der Fall ist. Überraschenderweise änderten sich Niveau und Lokalisation von β‑Catenin und seinem Korezeptor LRP6 im Darm nicht nach Entfernen des microRNA‑Clusters, selbst in den Doppel‑Knockouts. Stattdessen wies groß angelegte Genexpressionsanalyse in eine andere Richtung: Tumoren ohne PTEN und die microRNAs zeigten starke Signaturen von Gewebeumbau, Wundantwort und epithelial‑mesenchymaler Transition — einem Programm, das mit Invasion und Metastasierung verbunden ist. Signalkaskaden, die von MAP‑Kinasen (ERK1/2 und p38) und dem Wachstumsfaktor TGFβ gesteuert werden, waren besonders angereichert.
Wie Wachstumssignale außer Kontrolle geraten
Bei näherer Untersuchung der Proteine im Darmgewebe fanden die Forscher, dass während alleiniger PTEN‑Verlust die PI3K/AKT‑Achse verstärkte, der zusätzliche Wegfall des microRNA‑Clusters einen weiteren Anstieg der MAPK‑Aktivität verursachte: mehr aktiviertes JNK, p38, MKK4 und besonders ERK1/2. Diese hochaktiven Signale gingen mit erhöhten Werten von Cyclin D1 einher, einem Schlüsseltreiber der Zellteilung. Gleichzeitig stiegen Komponenten der TGFβ‑Signalgebung, die deren Aktivität fördern (SMAD3 und SMAD4), während eine interne Bremse (SMAD7) fiel, und Krebszellen zeigten stärkere nukleäre SMAD2/3‑Färbung, konsistent mit einer Aktivierung des Weges. Durch den Vergleich von Maus‑Tumorgenen mit vorhergesagten microRNA‑Zielen identifizierte das Team IGF1, einen potenten Wachstumsfaktor, der in MAPK‑Kaskaden einspeist, als direktes Ziel des miR‑424(322)~503‑Clusters. Wenn die microRNAs fehlten, entkam IGF1 der Repression und trieb die MAPK‑Signalgebung weiter an. Analysen menschlicher Darmkrebsdatensätze spiegelten diese Befunde wider: IGF1 war in Tumoren mit niedrigem miR‑424‑ oder miR‑503‑Spiegel höher, und die längere nicht‑kodierende RNA, die diese microRNAs beherbergt, MIR503HG, sowie die microRNAs selbst waren bei Patiententumoren koordiniert verändert.
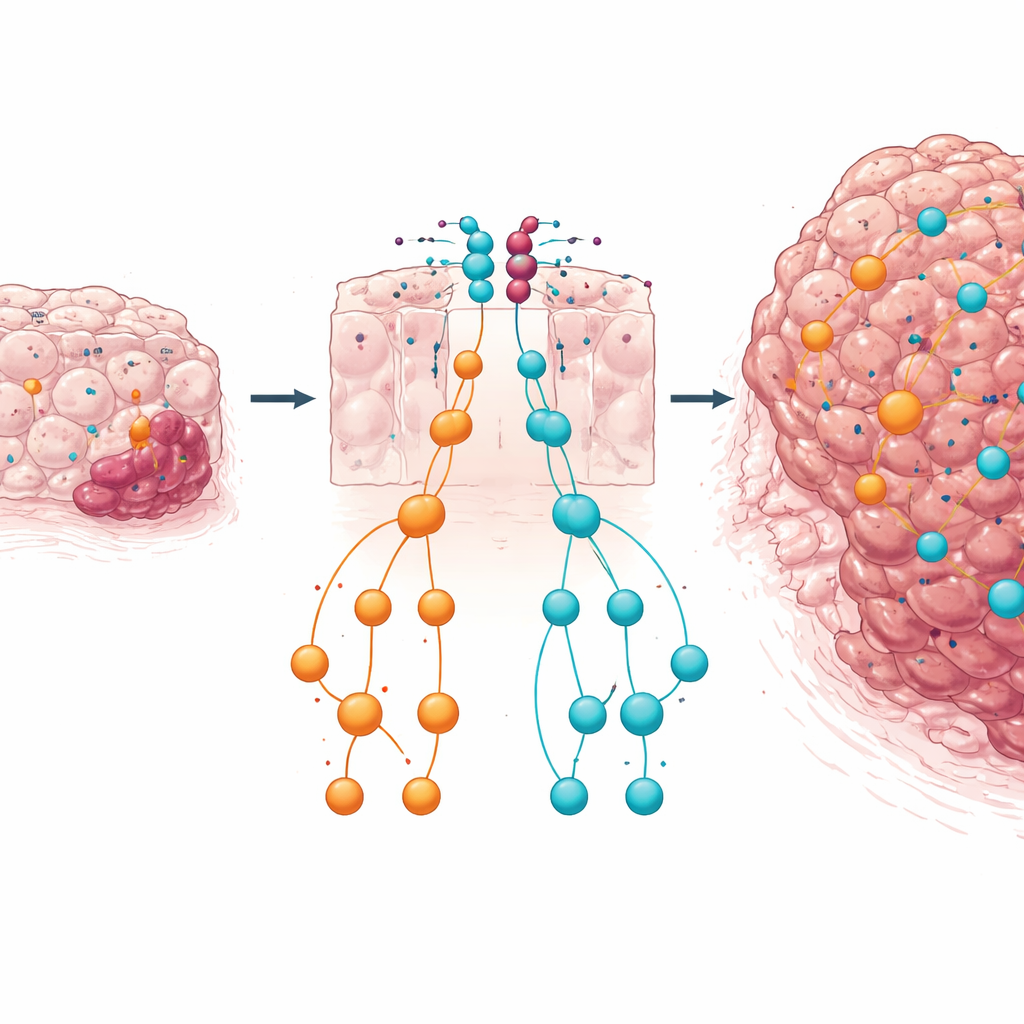
Ein doppeltes Sicherheitsnetz und was das für Patienten bedeutet
Insgesamt legen die Ergebnisse nahe, dass der miR‑424(322)~503‑Cluster in PTEN‑defizientem Darmgewebe wie ein zweites Sicherheitsnetz wirkt. Wenn PTEN verloren geht, werden diese microRNAs unter anderem durch Signale wie TGFβ hochreguliert und arbeiten daran, starke Wachstumswege wie IGF1–MAPK und TGFβ–SMAD zu dämpfen. Wird diese microRNA‑Bremse entfernt, laufen Wachstums‑ und Umbau‑Signale ungehindert ab und beschleunigen den Übergang von gutartigen Polypen zu invasivem Krebs. Für Laien lautet die Kernbotschaft: Nicht alle genetischen Veränderungen in einem Tumor wirken in dieselbe Richtung — einige sind eingebaute Schutzmechanismen. Zu verstehen, wie PTEN und dieser microRNA‑Cluster zusammenarbeiten, um das Zellwachstum im Gleichgewicht zu halten, könnte helfen, Hochrisikopatienten zu identifizieren und kombinierte Behandlungen zu inspirieren, die sowohl die PI3K/AKT‑ als auch die MAPK/TGFβ‑Achsen beim kolorektalen Krebs ansprechen.
Zitation: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Schlüsselwörter: kolorektales Karzinom, PTEN, microRNA, MAPK-Signalübertragung, TGF-beta