Clear Sky Science · de
ERRα-KDM5C dämpft die STING-Enhancer-Aktivität, um die Typ‑I‑Interferon‑Signalgebung beim Fortschreiten von Brustkrebs zu modulieren
Krebszellen am Verstecken hindern
Krebszellen tun mehr, als nur unkontrolliert zu wachsen — sie lernen auch, sich vor dem Immunsystem des Körpers zu verbergen. Diese Studie zeigt, wie bestimmte Brustkrebszellen ein wichtiges internes Alarmsystem, den STING‑Signalweg, herunterregulieren, das normalerweise das Immunsystem auf Gefahren aufmerksam macht. Indem Forschende diesen „Aus‑Schalter“ verstehen, erhofft man sich neue Ansätze, Tumoren für das Immunsystem sichtbarer zu machen und die Wirksamkeit bestehender Therapien, einschließlich Chemotherapie, zu verbessern.
Ein zelluläres Alarmsystem unter Druck
Der STING‑Signalweg funktioniert wie eine eingebaute Sicherheitsanlage in unseren Zellen. Wenn DNA‑Schäden oder virenähnliche Signale erkannt werden, löst STING die Produktion von Typ‑I‑Interferonen aus — starke Immunbotenstoffe, die Abwehrkräfte wie zytotoxische T‑Zellen anlocken. Viele Tumoren finden Wege, diesen Alarm stummzuschalten, was ihr ungehindertes Wachstum erleichtert. Die Autorinnen und Autoren dieser Arbeit richteten ihr Augenmerk auf Brustkrebszellen und fragten: Welche Moleküle sind dafür verantwortlich, STING gedämpft zu halten, und wie ist diese Kontrolle in das genetische „Schaltbrett“ der Enhancer eingebettet — kurze DNA‑Abschnitte, die die Aktivität benachbarter Gene verstärken?
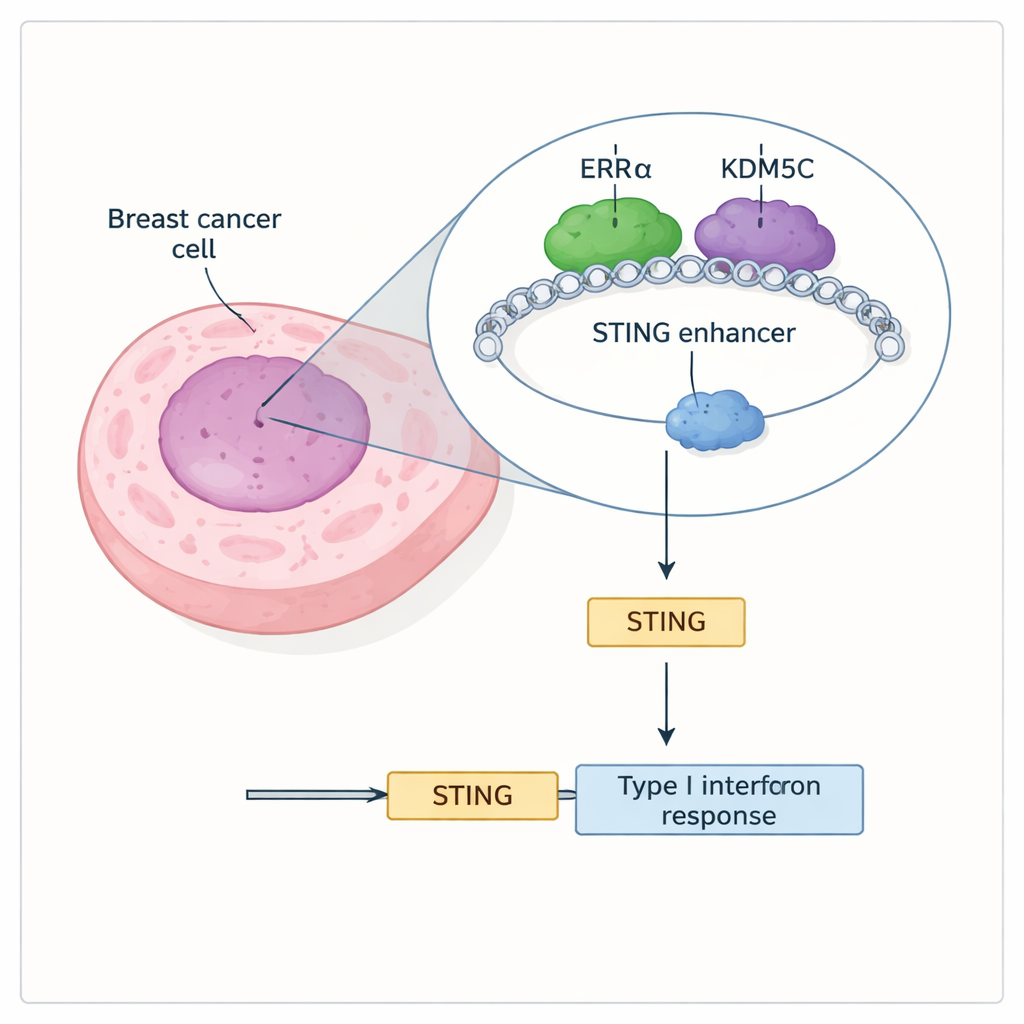
Zwei Proteine dämpfen STING gemeinsam
Die Forschenden entdeckten, dass ein nukleärer Rezeptor namens ERRα und ein Enzym namens KDM5C physisch interagieren und gemeinsam an vielen aktiven Enhancer‑Regionen sitzen, einschließlich eines Enhancers, der das STING‑Gen kontrolliert. ERRα ist dafür bekannt, Krebszellen bei der Umprogrammierung ihres Stoffwechsels und der Resistenz gegen Zelltod zu unterstützen, während KDM5C ein „Chromatin‑Editor“ ist, der eine chemische Markierung (H3K4me3) entfernt, die mit starker Genaktivierung assoziiert ist. Mithilfe genomweiter Bindungskarten zeigten die Forschenden, dass ERRα und KDM5C häufig Enhancer‑Stellen gemeinsam besetzen, die Aktivitätszeichen tragen und Enhancer‑RNA produzieren — ein Hinweis darauf, dass diese Schalter eingeschaltet sind. Besonders am STING‑Enhancer sind beide Proteine präsent, und ihre Anwesenheit geht mit einer gedämpften STING‑Antwort einher.
Die Bremse für Immun‑Signale lösen
Wenn die Wissenschaftlerinnen und Wissenschaftler die ERRα‑ oder KDM5C‑Spiegel in Brustkrebszellen reduzierten, wurde der STING‑Enhancer überaktiv. Chemische Markierungen, die mit starker Aktivierung verbunden sind, nahmen zu, solche, die einen schwächeren Zustand kennzeichnen, gingen zurück, und die Produktion von Enhancer‑RNA stieg. Darauf folgte ein Anstieg der STING‑Gen‑ und Proteinmengen sowie eine stärkere Aktivierung des nachgeschalteten Signalwegs, einschließlich TBK1 und IRF3 — zentrale Relay‑Proteine, die die Produktion von Typ‑I‑Interferonen vorantreiben. Dadurch begannen die Zellen, höhere Mengen an Interferonen und interferon‑stimulierenden Genen zu exprimieren, die für antivirale Abwehr und Anti‑Tumor‑Immunität zentral sind. Anders ausgedrückt: Durch das Entfernen von ERRα oder KDM5C wurde ein gedämpfter Alarm in den Krebszellen zu einer lauten Sirene.
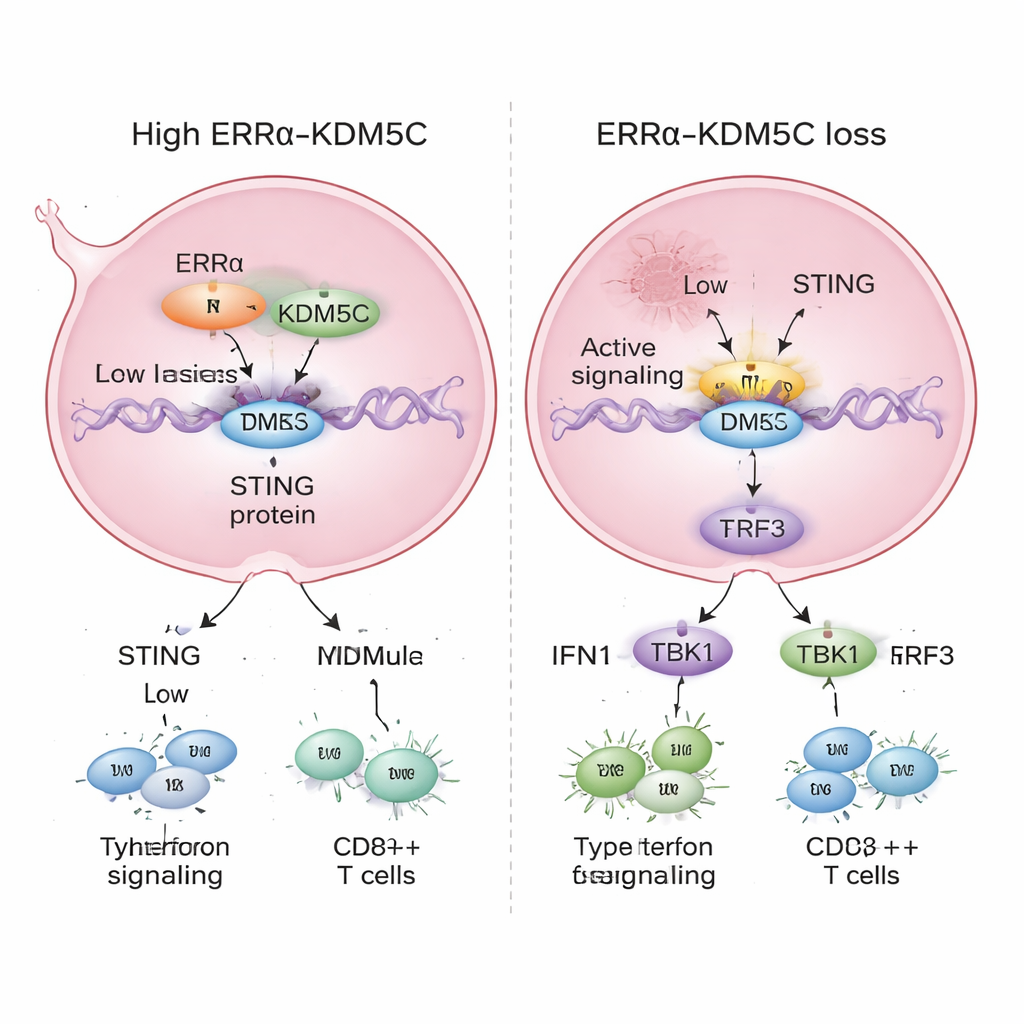
Wachstumsverzögerung des Tumors und verbesserte Therapie
Diese molekularen Veränderungen hatten deutliche Auswirkungen auf das Verhalten der Krebszellen. Brustkrebszellen mit reduzierten ERRα‑ oder KDM5C‑Werten wuchsen langsamer und bildeten in Kultur weniger Kolonien. In Mausmodellen waren Tumoren, die aus ERRα‑depletierten Zellen hervorgingen, kleiner und leichter, was auf ein abgeschwächtes Wachstum im lebenden Organismus hindeutet. Wichtig ist: Wurde STING ebenfalls ausgeschaltet, kehrte ein Großteil dieser Wachstumshemmung zurück, was zeigt, dass die Aktivierung von STING ein zentraler Bestandteil der tumordämpfenden Wirkung durch den Verlust von ERRα und KDM5C ist. Das Team testete außerdem das Chemotherapeutikum Etoposid, das DNA‑Schäden verursacht und bekanntermaßen STING aktiviert. Das Blockieren von ERRα machte Etoposid in der Tumorschrumpfung wirksamer, was darauf hindeutet, dass das Lösen dieser Bremse Standardbehandlungen durch Verstärkung immunstimulierender Signale verbessert.
Was das für Patientinnen und Patienten bedeutet
Durch die Analyse von Patientendaten fanden die Forschenden heraus, dass ERRα‑Spiegel in menschlichen Brustkrebserkrankungen höher sind als im normalen Brustgewebe und dass hohe ERRα‑Expression mit schlechterem Überleben und geringerer Präsenz krebsbekämpfender CD8+‑T‑Zellen in Tumoren einhergeht. Insgesamt zeichnet die Arbeit ein klares Bild: ERRα und KDM5C bilden ein Kontrollmodul, das den STING‑Alarm leise hält und Brusttumoren hilft, zu wachsen und einer Immunattacke zu entgehen. Für Laien lautet die Kernaussage, dass einige Brustkrebse dieses Duo nutzen, um sich vor den Abwehrkräften des Körpers zu verbergen. Das gezielte Ansprechen von ERRα, KDM5C oder ihrer Bindung am STING‑Enhancer könnte Tumoren „entmaskieren“, die Immunantwort stärken und die Wirkung bestehender Therapien erhöhen.
Zitation: Xu, ZH., Chen, J., He, Y. et al. ERRα-KDM5C restrains STING enhancer activity to modulate type I interferon signaling in breast cancer progression. Cell Death Dis 17, 228 (2026). https://doi.org/10.1038/s41419-026-08499-2
Schlüsselwörter: Brustkrebs, STING‑Signalweg, Typ‑I‑Interferon, epigenetische Regulation, Tumorimmunität