Clear Sky Science · de
mTOR‑vermittelte Unterdrückung der Autophagie definiert metabolische Verwundbarkeit bei CDK4/6‑Inhibitor‑resistentem HR+/HER2− Brustkrebs
Warum das für Brustkrebspatientinnen wichtig ist
Viele Frauen mit fortgeschrittenem Brustkrebs leben heute dank Medikamenten, die CDK4/6‑Inhibitoren genannt werden, länger, weil diese die Teilungsrate der Tumorzellen verlangsamen. Leider finden die meisten Tumoren früher oder später Wege, diesen Medikamenten zu entkommen. Diese Studie stellt eine hoffnungsvolle Frage: Wenn Brustkrebs gegenüber CDK4/6‑Medikamenten resistent wird, entsteht dann eine neue Schwäche, die Ärzte mit bereits verfügbaren, vergleichsweise einfachen metabolischen Medikamenten wie Metformin oder Dichloressigsäure (DCA) ausnutzen könnten?
Wenn Zellzyklus‑Medikamente nicht mehr wirken
Ärzte behandeln die häufigste Form von Brustkrebs – hormonrezeptorpositives, HER2‑negatives Krankheitsbild – oft mit Hormontherapie plus CDK4/6‑Inhibitoren wie Palbociclib oder Ribociclib. Diese Wirkstoffe zielen auf Proteine, die Zellen durch den Teilungszyklus treiben. Mit der Zeit passen sich jedoch einige Krebszellen an und werden stark resistent, sodass sie auch bei hohen Dosen weiterwachsen. Die Forschenden stellten dieses Problem im Labor nach, indem sie Brustkrebszelllinien (T47D und MCF7) schrittweise steigenden Konzentrationen von CDK4/6‑Inhibitoren aussetzten. Es entstanden zwei Arten von Überlebenden: teilweise resistente Zellen und eine kleinere Gruppe hochresistenter Klone, die nicht mehr gut auf die Behandlung ansprachen.
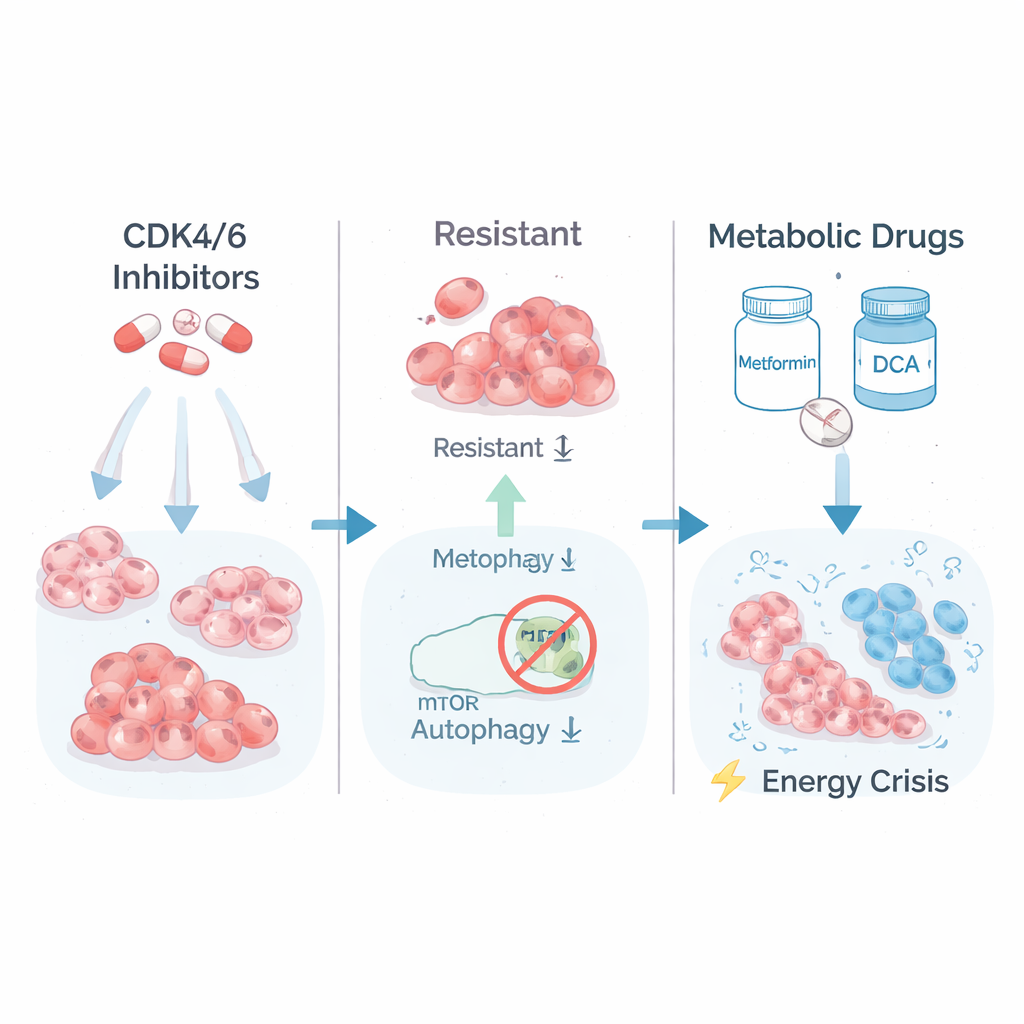
Eine verborgene Schwäche im Tumor‑Energiehaushalt
Um zu verstehen, was die hochresistenten Zellen anders machte, untersuchten die Forscher, welche Gene ein‑ oder ausgeschaltet waren. Sie entdeckten, dass die am stärksten resistenten Zellen Stoffwechselwege für verstärkte Zuckerverbrennung (Glykolyse) und Wachstumssignale unter Kontrolle des Proteincomplexes mTORC1 hochgefahren hatten. Anders gesagt: Diese Zellen liefen auf Hochtouren und verbrauchten Brennstoff in hoher Geschwindigkeit, um weiter zu wachsen. Die Wissenschaftler prüften dann, ob sich dieser "Hochleistungs"‑Metabolismus gegen die Zellen wenden ließ. Sie behandelten die resistenten und die ursprünglichen Zellen mit Metformin, einem verbreiteten Diabetesmedikament, das die Energie‑Fabriken der Zelle belastet, und mit DCA, das Zellen dazu zwingt, Brennstoffe effizienter zu verarbeiten. Auffallend war, dass gerade die am stärksten medikamentenresistenten Klone nun am verwundbarsten waren: Ihr langfristiges Wachstum in Kultur brach unter der metabolischen Behandlung zusammen, während die Elternlinien und nur teilweise resistenten Zellen deutlich weniger betroffen waren.
Blockierte Selbstreinigung und ein Energieabsturz
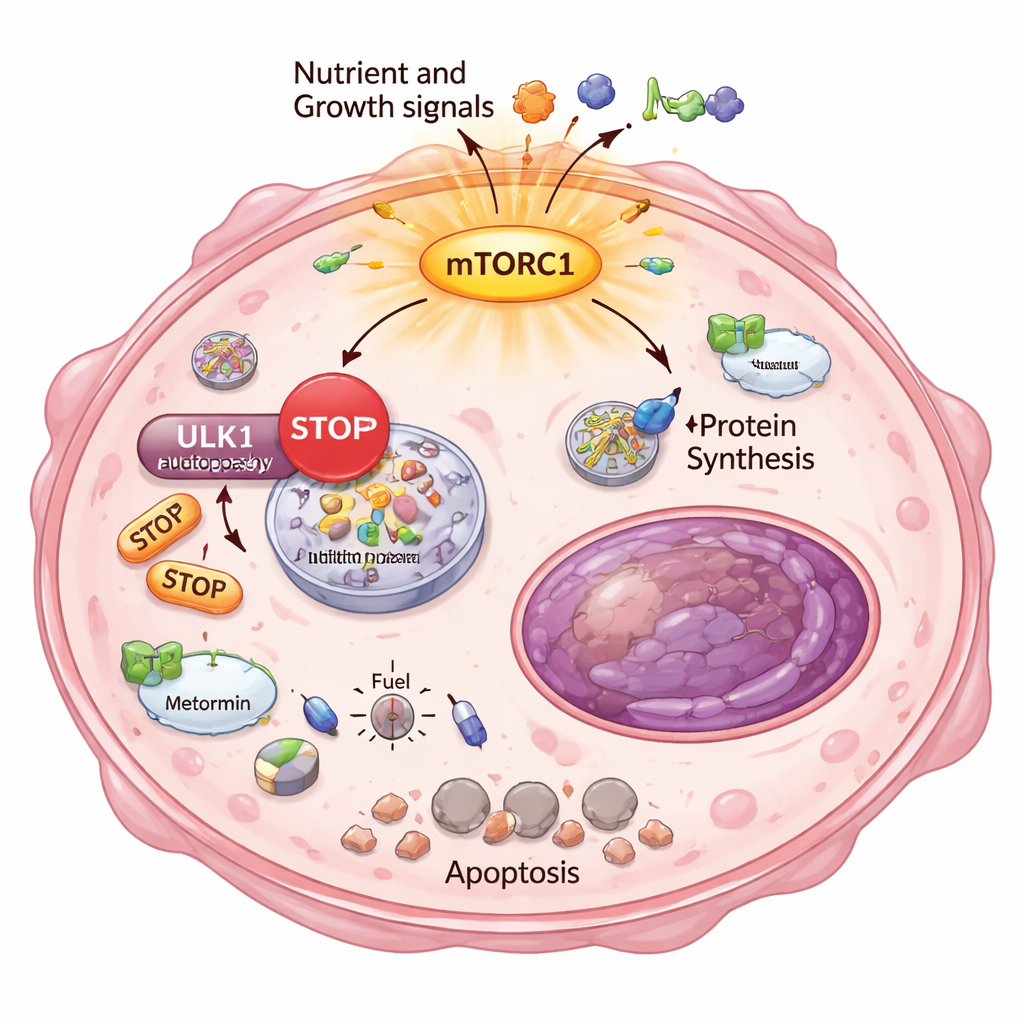
Warum sollten diese entkommenen Krebszellen so empfindlich gegenüber Energiestress sein? Die Antwort lag in einem weiteren grundlegenden Überlebensprozess: Autophagie, dem zellinternen "Recycling‑ und Reinigungs"‑System. Normalerweise bauen Zellen bei Energiemangel eigene Bestandteile ab und verwerten sie wieder, um zu überleben. Die Forschenden zeigten, dass in den hochresistenten Klonen mTORC1 überaktiv war und eine chemische Bremse auf ULK1 legte, einen wichtigen Startpunkt der Autophagie. Mit einem sensiblen Reporter‑Assay demonstrierten sie, dass diese Zellen Autophagie nicht mehr richtig einschalten oder hochfahren konnten, selbst wenn sie durch metabolische Medikamente dazu gezwungen wurden. Infolgedessen erzeugten Metformin und DCA eine schwere Energiemangellage: Energie‑Sensoren signalisierten Alarm, die Fettproduktion wurde eingestellt und Marker für irreversible Zellschädigung traten auf — spezifisch in den stark resistenten Zellen.
Hinweise aus echten Patienten‑Tumoren
Labor‑Modelle spiegeln nicht immer das Geschehen beim Menschen wider, daher untersuchten die Wissenschaftler Proben menschlicher Brusttumoren. Sie färbten über hundert Tumoren für einen Marker mTORC1‑Aktivität (phosphoryliertes 4E‑BP1) und für p62, ein Protein, das sich anreichert, wenn Autophagie blockiert ist. Tumoren mit hoher mTORC1‑Aktivität zeigten tendenziell mehr p62, was die Idee stützt, dass ein Muster aus "übersteuertem Wachstumssignal plus schlechtem Recycling" in echten Brustkrebserkrankungen existiert und nicht nur in Zelllinien. Das legt nahe, dass eine Untergruppe von Patientinnen Tumoren besitzen könnte, die dieselbe metabolische Verwundbarkeit wie im Labor aufweisen.
Was das für künftige Behandlungen bedeuten könnte
Für Laien ist die Kernbotschaft: Wenn Brustkrebserkrankungen sich so weiterentwickeln, dass sie mächtigen CDK4/6‑Medikamenten entkommen, geraten sie möglicherweise auch in einen metabolischen Engpass. Indem sie Wachstumssignale dauerhaft anschalten und das zelluläre Recycling abschalten, werden diese Tumoren stark abhängig von einer kontinuierlichen Energiezufuhr. Die Studie zeigt, dass dieses System mit metabolischen Medikamenten wie Metformin und DCA, die in anderen Erkrankungen bereits gut bekannt sind, ausgenutzt werden kann. Wichtig ist, dass die Autorinnen und Autoren vorschlagen, einfache Gewebetests für mTORC1‑Aktivität und Autophagie‑Marker zu nutzen, um Patientinnen zu identifizieren, deren resistente Tumoren für eine solche metabolische Therapie anfällig sind — und damit den Weg zu personalisierteren Rettungsbehandlungen nach Versagen von CDK4/6‑Inhibitoren zu öffnen.
Zitation: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Schlüsselwörter: Brustkrebs, Resistenz gegen CDK4/6‑Inhibitoren, mTOR, Autophagie, metabolische Therapie