Clear Sky Science · de
Umschalten des Spleißens der onkogenen BCS1L-Isoform unterdrückt das Fortschreiten von Eierstockkrebs durch Störung der mitochondrialen Funktion
Kraftwerke innerhalb von Krebszellen
Jede Zelle in unserem Körper ist auf winzige Kraftwerke angewiesen, die Mitochondrien genannt werden. Krebszellen, die schnell wachsen und sich ausbreiten, benötigen besonders viel Energie. Diese Studie zeigt, wie Eierstockkrebs einen seiner wichtigen mitochondrialen Helfer umprogrammiert und dass ein behutsames Umlegen eines molekularen „Schalters“ an diesem Helfer Tumoren aushungern kann, während gesundes Gewebe größtenteils verschont bleibt.
Warum Tumoren auf ihre Motoren angewiesen sind
Eierstockkrebszellen können, wie viele Krebsarten, flexibel verschiedene Energiequellen anzapfen. Beim Durchforsten umfangreicher Patientendatenbanken und Einzelzellprofile fanden die Forscher, dass viele Eierstocktumoren ihre Mitochondrien im Hochgang betreiben, bekannt als oxidative Phosphorylierung (OXPHOS). Tumoren mit dieser gesteigerten mitochondrialen Aktivität waren aggressiver und häufiger in fortgeschrittenen Stadien. Unter den zahlreichen Proteinen, die die mitochondriale Energieausrüstung aufbauen, stach eines hervor: BCS1L, ein Chaperon, das beim Zusammenbau von Komplex III hilft, einem zentralen Knoten in der Energiepipeline der Zelle. In OXPHOS-starken Tumoren und bestimmten Tumorzelltypen war die BCS1L-Aktivität besonders hoch, was darauf hindeutet, dass Krebszellen stark auf diesen Helfer angewiesen sind, um ihre Motoren am Laufen zu halten.
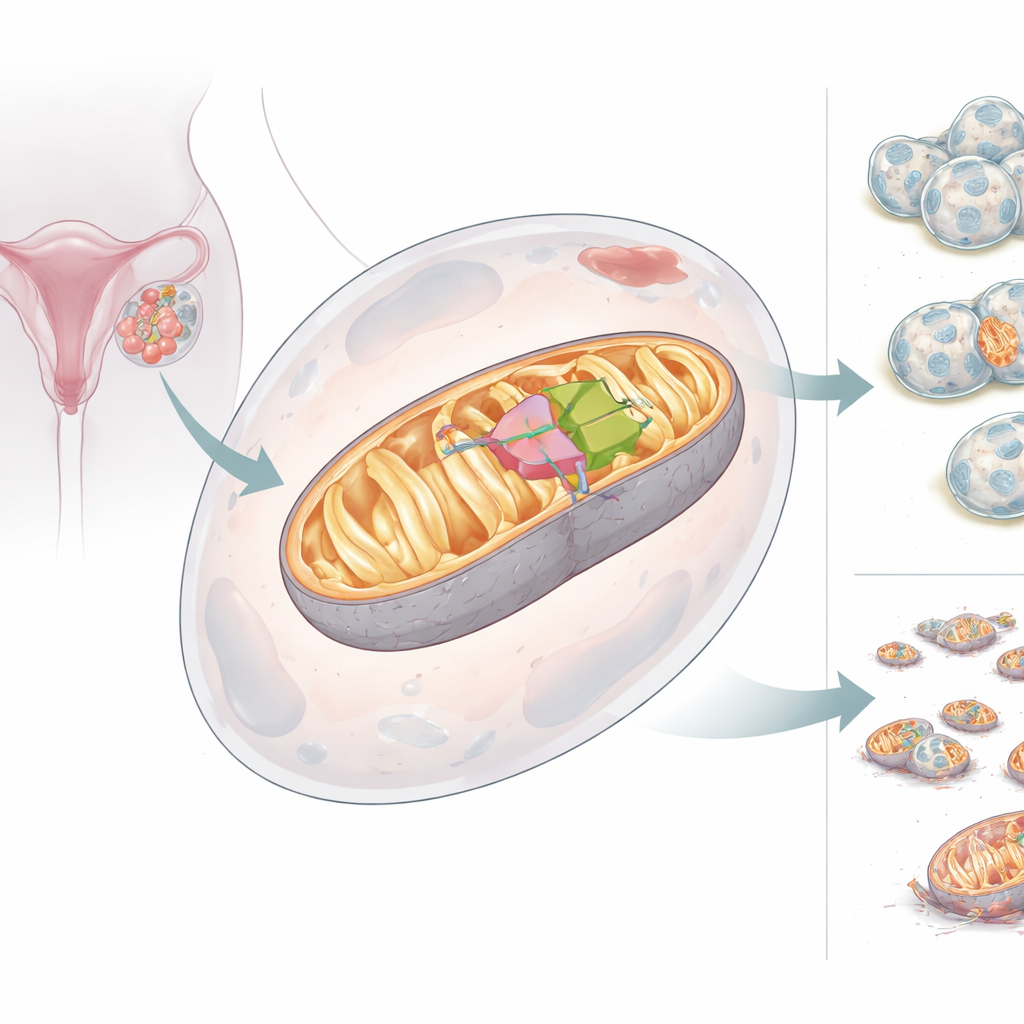
Zwei Gesichter eines mitochondrialen Helfers
Das Team entdeckte, dass das BCS1L-Gen zwei Versionen bzw. Isoformen seines Proteins produzieren kann. Die Vollform, BCS1L-L, trägt ein eingebautes Adressetikett, das sie in die Mitochondrien schickt, wo sie den korrekten Zusammenbau von Komplex III und eine hohe Energieproduktion unterstützt. Die kürzere Form, BCS1L-S, fehlt ein entscheidendes Segment und kann die Mitochondrien nicht erreichen; stattdessen liegt sie im Zellplasma und Zellkern und unterstützt die Energieproduktion nicht. In gesundem Gewebe ist die kurze Version verbreitet, doch bei Eierstockkrebserkrankungen kippt das Gleichgewicht: Die lange, mitochondriengebundene Form dominiert. Wenn Zellen gezwungen wurden, mehr BCS1L-L zu produzieren, erzeugten ihre Mitochondrien mehr Energie, hielten ein stärkeres Membranpotenzial aufrecht, produzierten weniger schädliche Sauerstoffnebenprodukte und widerstanden dem Zelltod. Bei Reduktion von BCS1L fragmentierten die Mitochondrien, die Energieproduktion sank, schädliche Sauerstoffmoleküle stiegen an und Krebszellen starben vermehrt.
Wie Krebs die Botschaft umlenkt
Die Produktion der langen oder kurzen BCS1L-Version hängt davon ab, wie die Zelle ihre RNA-Botschaft bearbeitet, ein Prozess, der als Spleißen bezeichnet wird. Die Forscher suchten nach Proteinen, die an die BCS1L-RNA binden und diese Wahl beeinflussen. Sie konzentrierten sich auf USP39, einen Spleißfaktor, der bereits mit mehreren Krebsarten in Verbindung gebracht wurde. In Eierstockkrebszellen bindet USP39 in der Nähe des RNA-Abschnitts, der zu Exon 2 von BCS1L wird, und fördert dessen Einbeziehung, wodurch die lange, an Mitochondrien gerichtete Version bevorzugt wird. Wenn USP39 stillgelegt wurde, übersprangen die Zellen diesen Abschnitt häufiger und stellten verstärkt die kurze BCS1L-S-Form her. Dieser Wechsel schwächte Komplex III, verringerte die mitochondriale Atmung und ATP-Produktion, erhöhte oxidativen Stress und löste den Zelltod von Krebszellen aus. Die Wiederherstellung von BCS1L-L in diesen Zellen rettete einen Großteil ihrer mitochondrialen Funktion und ihres Überlebens, was zeigt, dass USP39 einen kritischen mitochondrialen Schalter weitgehend über BCS1L steuert.
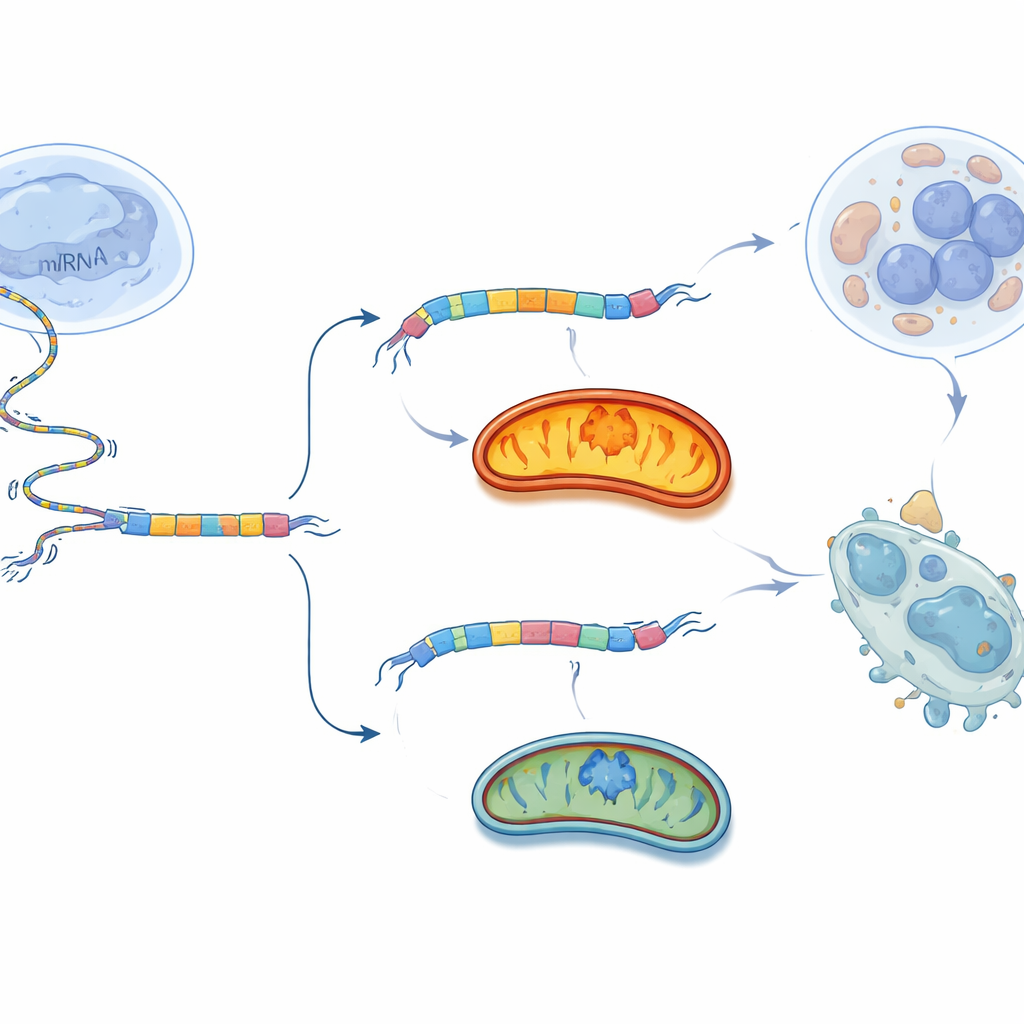
Den Schalter gegen den Tumor umlegen
Anstatt die Mitochondrien allgemein zu blockieren, was vielen Geweben schaden könnte, verfolgte das Team eine gezieltere Taktik: sie beeinflussten direkt die Spleißentscheidung von BCS1L. Sie entwickelten kurze genetische Stücke, sogenannte Antisense-Oligonukleotide (ASOs), die genau um Exon 2 der BCS1L-RNA binden. Diese ASOs wirken wie winzige Wäscheklammern, ändern, wie die Spleißmaschinerie die Botschaft liest, und fördern das Überspringen von Exon 2. In in vitro kultivierten Eierstockkrebszellen reduzierte das effektivste ASO stark die lange BCS1L-L-Form und steigerte die kurze BCS1L-S-Form. Infolgedessen sanken die mitochondriale Atmung und ATP-Produktion, die schädlichen Sauerstoffwerte stiegen und deutlich mehr Zellen durch programmierten Zelltod eliminiert wurden. Als dasselbe ASO in Eierstockkrebstumoren von Mäusen injiziert wurde, verlangsamte sich das Tumorwachstum und das Tumorgewicht nahm ab, wobei die Wirkung auf Krebszellen deutlich stärker war als auf normale Fibroblasten.
Was das für Patientinnen bedeuten könnte
Vereinfacht gesagt zeigt diese Arbeit, dass viele Eierstocktumoren von einer „Turbo“-Version eines mitochondrialen Helferproteins abhängen, um ihr Wachstum zu befeuern. Ein Spleißfaktor, USP39, verschiebt die RNA-Bearbeitungsmaschinerie der Zelle so, dass mehr von dieser Turbo-Version hergestellt wird und die Tumor-Kraftwerke in Bestform bleiben. Durch präzise entworfene ASOs, die die Spleißwahl wieder zugunsten der schwächeren Version umlenken, können Forscher die Mitochondrien von Krebszellen selektiv lahmlegen, deren Tod auslösen und die meisten normalen Zellen weniger beeinträchtigen. Obwohl die Verabreichung solcher ASO-Wirkstoffe an Tumoren weiterhin eine große Herausforderung darstellt, macht diese Studie den BCS1L-Spleißschalter zu einem vielversprechenden und hochspezifischen Ansatzpunkt für die Behandlung von Eierstockkrebs.
Zitation: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Schlüsselwörter: Eierstockkrebs, Mitochondrien, RNA-Spleißen, BCS1L, Antisense-Oligonukleotide