Clear Sky Science · de
NSD2 hemmt die Expression von PD-L1 über oxidative Phosphorylierung und steuert die Immunüberwachung beim hepatozellulären Karzinom
Warum diese Geschichte über Leberkrebs wichtig ist
Das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, wird oft spät entdeckt und ist gegen viele Behandlungen resistent. Immuntherapeutika, die den PD-L1‑„Unsichtbarkeitsmantel“ von Tumorzellen blockieren, helfen einigen Patientinnen und Patienten, bei den meisten jedoch nicht. Diese Studie bringt einen unerwarteten Akteur ans Licht: das Protein NSD2, das die Energieerzeugung von Leberkrebszellen mit ihrer Sichtbarkeit für das Immunsystem verknüpft. Das Verständnis dieser Verbindung könnte neue Wege eröffnen, bestehende Therapien zu stärken und vorherzusagen, welche Patienten profitieren.
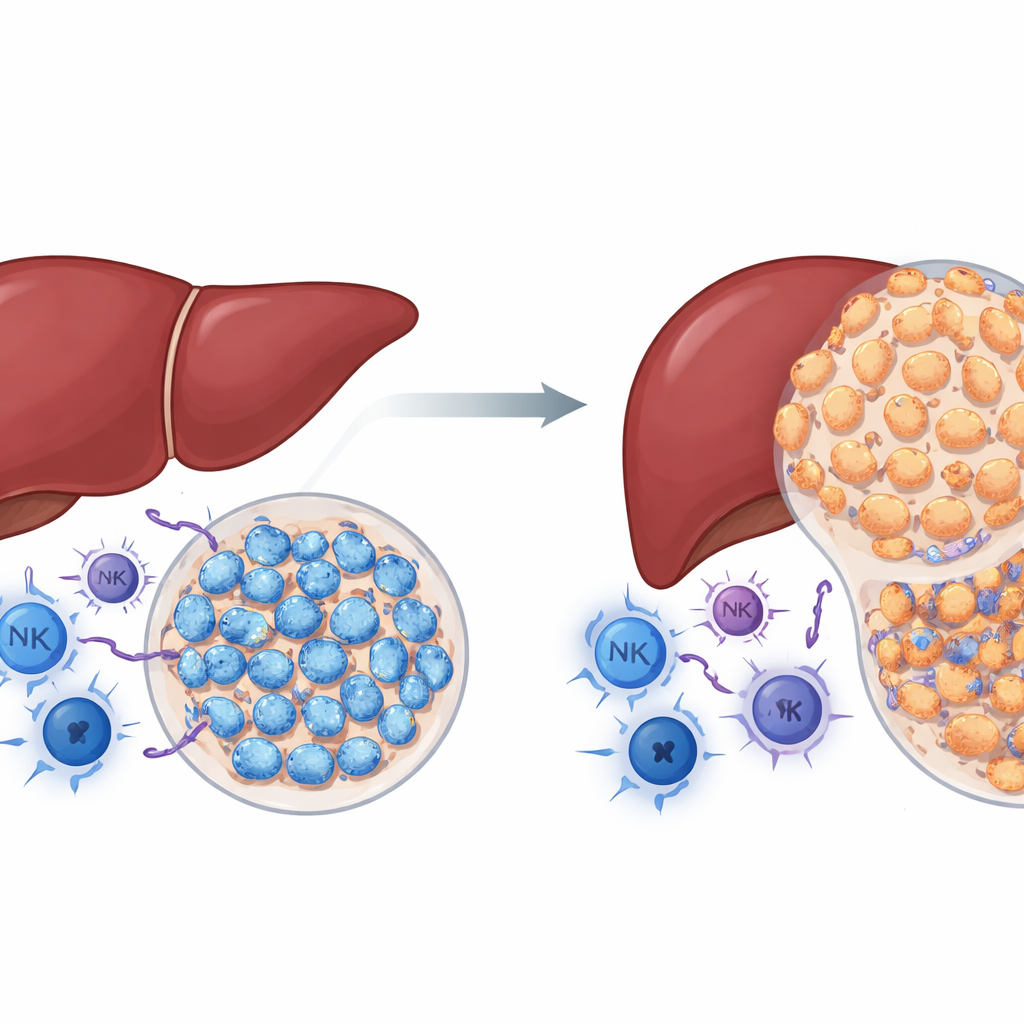
Eine überraschende Rolle für ein bekanntes Krebsprotein
NSD2 ist ein Enzym, das Histone verändert, also die Proteine, um die die DNA gewickelt ist. In vielen Krebsarten gilt NSD2 als Treiber des Tumorwachstums. Die Autorinnen und Autoren fragten, ob das auch für Leberkrebs gilt. Mit genetisch veränderten Mäusen, bei denen NSD2 gezielt in Leberzellen aktiviert wurde, setzten sie ein chemisches Mittel ein, das zuverlässig Lebertumoren hervorruft. Entgegen den Erwartungen entwickelten Mäuse mit zusätzlichem NSD2 deutlich weniger und kleinere Tumoren als normale Mäuse, und ihre Lebern zeigten weniger Schäden, Vernarbung und Zellproliferation. Gleichzeitig enthielten Tumoren aus NSD2‑überexprimierenden Lebern mehr krebsbekämpfende Immunzellen, darunter Helfer‑ und Killer‑T‑Zellen sowie natürliche Killerzellen. Diese Befunde deuten darauf hin, dass NSD2 im intakten Immunsystem weniger als Beschleuniger und eher als Bremse für Leberkrebs wirkt.
Energie‑fabriken und Brennstoffnutzung in Tumorzellen
Um zu verstehen, wie NSD2 Tumoren bremst, analysierte das Team die Genaktivität im Lebergewebe. Sie fanden, dass NSD2‑Überexpression Gene, die an der oxidativen Phosphorylierung beteiligt sind, stark dämpft — dem Prozess, mit dem Mitochondrien, die „Kraftwerke“ der Zelle, mithilfe von Sauerstoff Energie erzeugen. Folgeexperimente in Maus‑ und menschlichen Leberkrebszelllinien zeigten, dass eine Erhöhung von NSD2 die Expression vieler Gene der oxidativen Phosphorylierung senkte, den Sauerstoffverbrauch und die ATP‑Produktion reduzierte und das mitochondriale Membranpotenzial verringerte, ein Zeichen schwächerer mitochondrialer Aktivität. Gleichzeitig verbrauchten diese Zellen weniger Glukose, ohne jedoch ihre Abhängigkeit zugunsten der Glykolyse zu verlagern, was auf eine netto verringerte Energieleistung hinweist. Der Verlust von NSD2 hatte die gegenteiligen Effekte und stärkte mitochondriale Leistung und Brennstoffnutzung.
Wie NSD2 Energie und immunologische Sichtbarkeit umprogrammiert
Bei tiefergehender Analyse kombinierten die Forschenden genomweite Chromatin‑Kartierungen mit Expressionsdaten und identifizierten eine Gruppe von Genen, die direkt aktiviert werden, wenn NSD2 vorhanden ist. Zwei davon, Camk2d und Prkce, sind dafür bekannt, die mitochondriale Aktivität zu bremsen. NSD2 erhöhte eine bestimmte Histonmarkierung (H3K36me2) an ihren Promotoren und steigerte so ihre Expression. Die Wiedereinführung dieser Gene in NSD2‑defiziente Leberkrebszellen reduzierte den mitochondrialen Sauerstoffverbrauch und die ATP‑Produktion und bestätigte damit, dass sie als nachgeschaltete Bremsen der oxidativen Phosphorylierung wirken. Wichtig ist, dass frühere Arbeiten nahelegten, dass hochaktive Mitochondrien zu hoher PD-L1‑Darstellung auf Tumorzellen beitragen. In Übereinstimmung damit fanden die Autorinnen und Autoren, dass NSD2‑Überexpression die PD-L1‑Werte senkte, während NSD2‑Verlust PD-L1 auf Leberkrebszellen und im Tumorgewebe erhöhte.
Den Schild abschwächen und die Immunabwehr wecken
Die funktionalen Auswirkungen dieser molekularen Verschiebungen prüften die Forschenden an Mäusen, die Leberinjektionen mit Krebszellen erhielten, denen NSD2 hinzugefügt oder entzogen worden war. Zellen ohne NSD2 bildeten schnell größere Tumoren, exprimierten mehr PD-L1 und waren von weniger T‑Zellen und natürlichen Killerzellen durchdrungen, insbesondere von aktivierten Killer‑T‑Zellen. Als die Forschenden chemisch den mitochondrialen Komplex V blockierten, eine Schlüsselkomponente der oxidativen Phosphorylierung, sanken die PD-L1‑Werte in NSD2‑defizienten Zellen wieder in Richtung Normalwerte und Immunzellen konnten Tumorzellen besser abtöten. Ebenso reduzierten die Überexpression von Camk2d oder Prkce in NSD2‑losen Zellen oder die Behandlung von Tumoren mit einem PD-L1‑blockierenden Antikörper die Tumorgröße und stellten die Infiltration durch Immunzellen wieder her. In Patientendatensätzen war niedrige NSD2‑Expression mit schlechterem Überleben verknüpft, aber auffälligerweise mit einer besseren Ansprechrate auf PD-L1‑gerichtete Therapien, was nahelegt, dass der NSD2‑Status helfen könnte vorherzusagen, wer von solchen Medikamenten profitiert.
Was das für die zukünftige Versorgung von Leberkrebspatienten bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft: Diese Studie definiert NSD2 beim Leberkrebs neu als tumorunterdrückenden Faktor, zumindest in Gegenwart eines funktionierenden Immunsystems. Indem NSD2 die sauerstoffbasierte Energieproduktion der Zelle drosselt, senkt es indirekt PD-L1 auf Tumorzellen, entfernt damit einen Teil ihres Unsichtbarkeitsmantels und ermöglicht es Immunzellen, sie zu erkennen und anzugreifen. Diese neu beschriebene NSD2–Energie–PD-L1‑Kette liefert zwei praktische Ideen: Erstens könnten Patienten, deren Tumoren kein NSD2 aufweisen, besonders geeignete Kandidaten für PD-L1‑blockierende Medikamente sein; zweitens könnte die Kombination von Wirkstoffen, die die mitochondriale Energieproduktion hemmen, mit Immuntherapie einen wirksamen Doppelangriff gegen Leberkrebs darstellen.
Zitation: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Schlüsselwörter: hepatozelluläres Karzinom, NSD2, oxidative Phosphorylierung, PD-L1, Tumorimmuntherapie