Clear Sky Science · de
SNRPD2-vermittelte Regulation des Spleißens von DDX39B fördert das Fortschreiten des Endometriumkarzinoms durch Unterdrückung der Aktivierung cryptischer Exons von CTSC
Warum versteckte Botschaften in Krebsgenen wichtig sind
Endometriumkarzinom, ein häufiger Gebärmutterkrebs, nimmt weltweit zu, doch viele Patientinnen mit fortgeschrittener Erkrankung haben weiterhin nur wenige wirksame Behandlungsoptionen. Diese Studie zeigt, wie ein feiner zellulärer Prozess – das Ausschneiden und Zusammensetzen genetischer Botschaften – das Wachstum und die Ausbreitung von Endometriumtumoren antreiben kann. Indem sie eine verletzliche "Schaltplan"-Verbindung offenlegt, auf die Krebszellen angewiesen sind, deutet die Arbeit auf neue Wege hin, Tumoren mit präzisen genetischen Therapeutika auszuschalten.
Ein wachsender Krebs, der neue Antworten braucht
Das Endometriumkarzinom ist in vielen westlichen Ländern inzwischen der häufigste gynäkologische Krebs, mit stetig steigenden Fallzahlen und Todesfällen sowohl im Westen als auch in China. Operation, Bestrahlung, Chemotherapie, Hormontherapie und Immuntherapie kommen zum Einsatz, sind aber weit davon entfernt, perfekt zu sein. Die Entfernung der Gebärmutter beendet die Fertilität, hormonelle Behandlungen versagen häufig, und aggressive Tumoren treten oft wieder auf. Diese Herausforderungen haben Forscher dazu veranlasst, tiefer in Krebszellen nach molekularen Schwachstellen zu suchen, die sich mit präziseren Therapien angreifen lassen.
Die Spleißmaschinerie der Zelle als Schwachstelle
Damit Gene funktionieren, werden sie zunächst in lange RNA-Moleküle kopiert, die in einem Prozess namens Spleißen zugeschnitten und zusammengesetzt werden müssen. Spezialisierte Proteinkomplexe, die Spliceosomen, entscheiden, welche Abschnitte behalten und welche verworfen werden, und bearbeiten damit das Skript, das Zellen zur Proteinproduktion nutzen. Das Team konzentrierte sich auf eine Komponente des Spliceosoms namens SNRPD2, die zu einer Familie von „Sm“-Proteinen gehört und beim Aufbau der Spleißmaschinerie hilft. Durch Auswertung großer Krebsgen- und Proteindatenbanken sowie Untersuchungen an Patientenproben fanden sie heraus, dass die SNRPD2-Spiegel in Endometriumtumoren auffallend höher sind als in normaler Gebärmutterschleimhaut und dass Patientinnen mit tumoraler Überexpression von SNRPD2 schlechtere Prognosen haben.
Das Ausschalten eines Master-Editors verlangsamt Tumoren
Um zu prüfen, ob SNRPD2 nur ein Beobachter oder ein aktiver Treiber ist, reduzierten die Forschenden dessen Expression in im Labor gezüchteten Endometriumkarzinom-Zelllinien. Nach Silencing von SNRPD2 teilten sich die Zellen langsamer, bildeten weniger Kolonien und waren weniger beweglich und invasiv – Verhaltensweisen, die mit Metastasenbildung verbunden sind. Wurden diese veränderten Zellen in Mäuse implantiert, entstanden deutlich kleinere Tumoren mit weniger sich teilenden Zellen. Wichtig ist, dass das Team antisense Oligonukleotide entwickelte – kurze, arzneimittelähnliche synthetische DNA-Stücke –, die spezifisch die SNRPD2-RNA ansprechen. In einem patientenabgeleiteten Xenograft-Modell, in dem menschliche Tumorfragmente in immundefizienten Mäusen wachsen, senkten diese Antisense-Medikamente SNRPD2-Spiegel und Tumorgröße deutlich, was darauf hindeutet, dass SNRPD2 auf klinisch relevante Weise angreifbar sein könnte.
Eine dreistufige Kette vom Spleißfehler zum Tumorwachstum
Bei der Analyse der Genomdaten fragten die Forschenden, wie der Verlust von SNRPD2 die RNA-Botschaften im gesamten Genom umverdrahten könnte. Sie entdeckten, dass bei Reduktion von SNRPD2 ein wichtiges RNA-verarbeitendes Enzym, DDX39B, fehlreguliert wird. Normalerweise hilft DDX39B, ein bestimmtes Intron – ein zu entfernender RNA-Abschnitt – aus seiner eigenen Nachricht zu entfernen. Fehlt genügend SNRPD2, bleibt dieses Intron erhalten und erzeugt eine fehlerhafte DDX39B-RNA-Version, die die Zelle rasch abbaut. Weniger DDX39B hat dann Auswirkungen auf ein anderes Gen, CTSC, das ein proteolytisches Enzym kodiert und für Tumorwachstum und -ausbreitung unterstützend wirkt. Unter gesunden Bedingungen wird ein verborgenes "cryptic" Exon in der CTSC-RNA ignoriert, sodass die Zellen ein vollständiges, aktives CTSC-Protein herstellen. Bei reduzierten DDX39B-Spiegeln wird dieses cryptische Exon fälschlich inkludiert und führt zu vorzeitigen Stoppsignalen in der RNA. Die missgebildete CTSC-Nachricht wird abgebaut, bevor viel Protein produziert wird, und Krebszellen verlieren einen Teil ihrer Aggressivität.
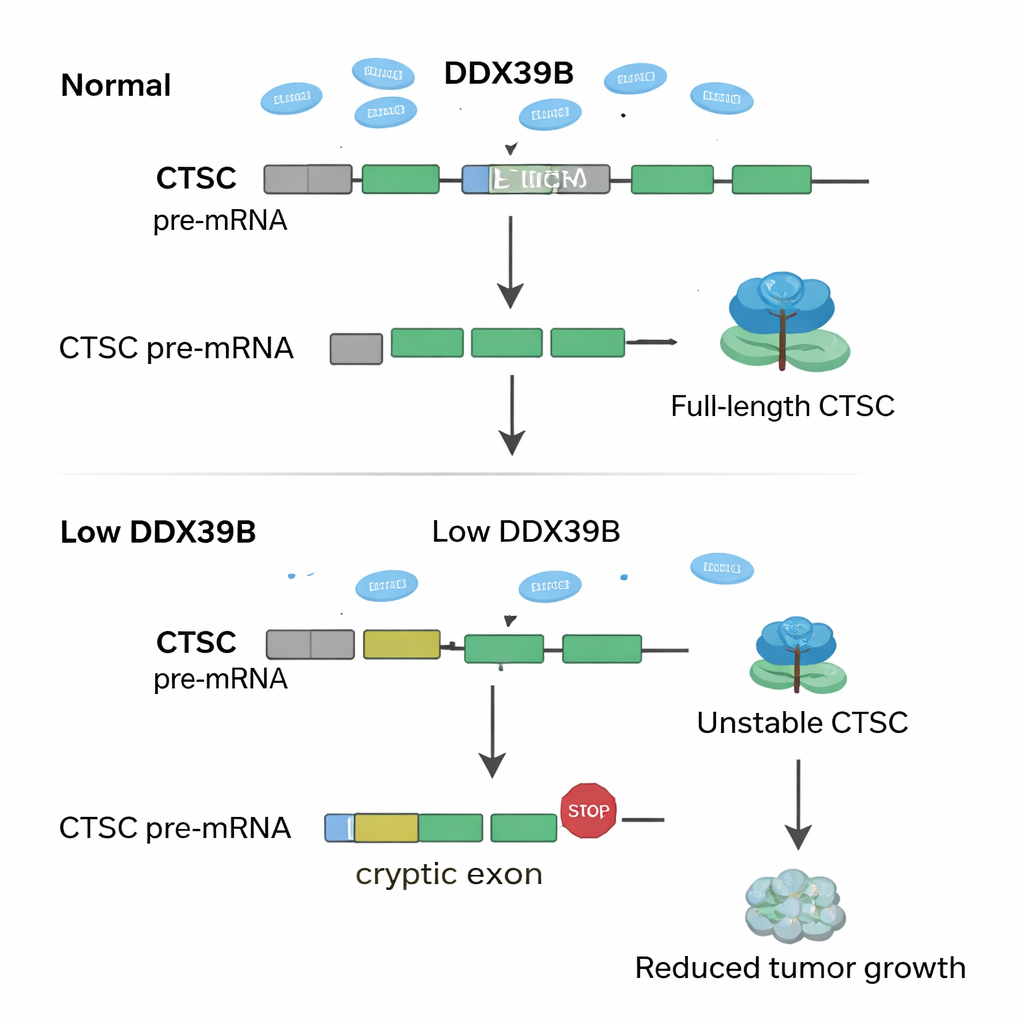
Was das für zukünftige Behandlungen bedeutet
Kurz gesagt decken die Autorinnen und Autoren ein Relay-System auf – SNRPD2 → DDX39B → CTSC –, das Endometriumkrebszellen nutzen, um zu gedeihen. Hohe SNRPD2-Spiegel erhalten DDX39B, und DDX39B verhindert wiederum, dass CTSC schädliche cryptische Exons benutzt, womit ein voll funktionsfähiges CTSC-Protein erhalten bleibt, das Tumoren beim Wachsen und Ausbreiten unterstützt. Wenn SNRPD2 blockiert wird, bricht diese Kette zusammen, CTSC-Spiegel fallen und die Tumoren schwächen sich. Für Nichtfachleute ist die zentrale Idee, dass Krebszellen auf sehr präzises RNA-Editing angewiesen sind und schon kleine erzwungene „Fehler“ ihr Wachstum selektiv vergiften können. Das Anvisieren von SNRPD2 mit Antisense-Medikamenten oder das direkte Erzwingen der Nutzung cryptischer Exons in CTSC könnte neue, maßgeschneiderte Therapien für Patientinnen mit Endometriumkarzinom bieten.
Zitation: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Schlüsselwörter: Endometriumkarzinom, RNA-Spleißen, SNRPD2, DDX39B, CTSC