Clear Sky Science · de
DNMT2 bremst das Fortschreiten von anaplastischem Schilddrüsenkrebs durch Herunterregulierung der Produktion von 5’tiRNAGly-GCC
Warum diese verborgene RNA-Chemie wichtig ist
Anaplastischer Schilddrüsenkrebs gehört zu den tödlichsten menschlichen Tumoren und tötet Patientinnen und Patienten oft innerhalb weniger Monate, trotz Operation, Strahlentherapie und Chemotherapie. Diese Studie deckt einen überraschenden Übeltäter tief innerhalb der Krebszellen auf: winzige chemische Markierungen auf Transfer-RNA, den Molekülen, die beim Aufbau von Proteinen helfen. Die Autorinnen und Autoren zeigen, dass bei Verlust oder Reduktion eines bestimmten Enzyms, DNMT2, Schilddrüsentumoren schneller wachsen, leichter streuen und dem üblichen Chemotherapeutikum Doxorubicin widerstehen. Noch spannender ist, dass sie ein kleines RNA‑Fragment identifizieren, das bei niedrigem DNMT2 entsteht, und nachweisen, dass das Blockieren dieses Fragments eine neue Behandlungsstrategie werden könnte.
Ein schützendes Enzym, das fehlt
Transfer‑RNAs (tRNAs) transportieren normalerweise Aminosäuren zur zellulären Proteinfabrik, und ihre Stabilität hängt von feinen chemischen Verzierungen ab. DNMT2 ist ein Enzym, das eine solche Markierung — eine Methylgruppe — an spezifische Stellen auf tRNA anfügt. In vielen Krebsarten ist DNMT2 erhöht und wird als förderlich für Tumoren betrachtet, doch hier ist die Situation umgekehrt. Anhand großer Patientendatensätze und Tumorproben fanden die Forschenden heraus, dass die DNMT2‑Spiegel im Gewebe des anaplastischen Schilddrüsenkrebses deutlich niedriger sind als in normaler Schilddrüse. Patientinnen und Patienten, deren Tumoren mehr DNMT2 enthielten, lebten tendenziell länger ohne Fortschreiten der Erkrankung, was darauf hindeutet, dass DNMT2 in dieser Krankheit eher wie eine Bremse wirkt als wie ein Beschleuniger.
Wie niedriges DNMT2 aggressives Verhalten antreibt
Um zu verstehen, was DNMT2 in Krebszellen tatsächlich bewirkt, manipulierte das Team dessen Spiegel in in vitro gezüchteten Zelllinien des anaplastischen Schilddrüsenkrebses und in Mausmodellen. Bei reduziertem DNMT2 vermehrten sich die Zellen schneller, drangen leichter durch Membranen und bildeten mehr Kolonien — alles Kennzeichen eines aggressiven Tumors. Diese Zellen wurden außerdem weniger empfindlich gegenüber Doxorubicin, einem Standardmedikament bei dieser Krebsart. In Mäusen wuchsen Tumoren mit reduziertem DNMT2 größer und streuten leichter in die Lunge, während eine Erhöhung der DNMT2‑Expression den gegenteiligen Effekt hatte. Die Forschenden führten diese Veränderungen teilweise auf die Aktivierung eines zellulären Programms zurück, das als epithelial–mesenchymale Transition bekannt ist und Krebszellen mobiler und invasiver macht.
Von beschädigter tRNA zu schädlichen kleinen Fragmenten
Bei genauerer Untersuchung zeigt die Studie, dass DNMT2 an einer bestimmten Position (genannt C38) nur drei tRNA‑Typen mit einer Methylmarkierung versieht. Ohne diesen Schutz werden die tRNAs anfälliger für das Schneiden durch ein anderes Enzym, Angiogenin. Dieser Schnitt erzeugt ein kurzes RNA‑Stück, das von tRNA‑Gly‑GCC abstammt und als 5’tiRNAGly‑GCC bezeichnet wird. Sequenzierungs‑ und biochemische Tests ergaben, dass dieses Fragment bei niedrigem DNMT2 verstärkt akkumuliert, besonders aus der Glycin‑transportierenden tRNA. In Reagenzglas‑Experimenten schützte das Anbringen der Methylmarke die tRNA stark vor dem Zerschneiden, was bestätigt, dass DNMT2 diese Moleküle normalerweise davor bewahrt, in kleinere, potenziell schädliche Stücke zerlegt zu werden.
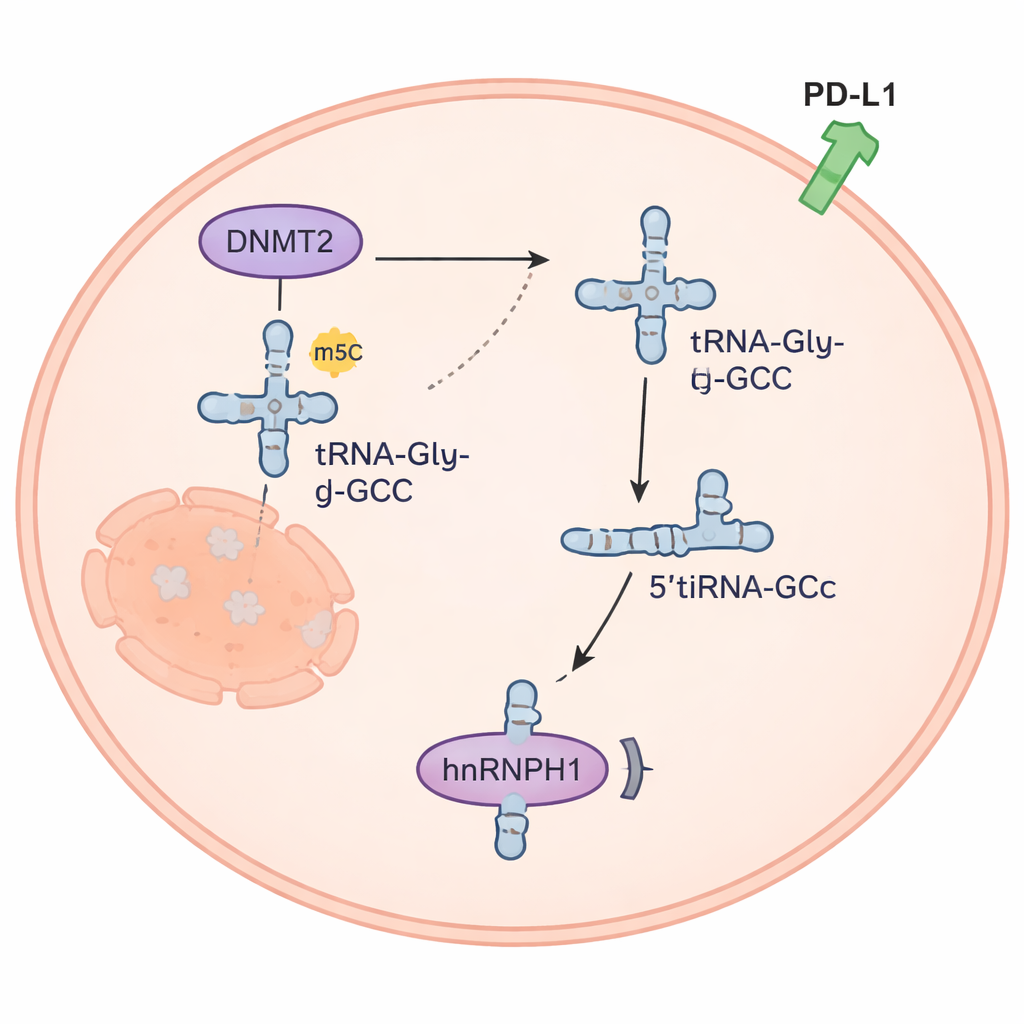
Ein winziges RNA‑Fragment verschaltet Krebs‑Signale
Das 5’tiRNAGly‑GCC‑Fragment erwies sich als mehr als molekularer Abfall. Es war reichlich in Zellen des anaplastischen Schilddrüsenkrebses vorhanden, aber selten in normaler Schilddrüse. Als die Forschenden seinen Spiegel künstlich erhöhten, proliferierten Krebszellen schneller, drangen stärker ein und wurden resistenter gegen Doxorubicin; eine Senkung des Fragments hatte den gegenteiligen Effekt. In Mäusen verlangsamte ein chemisch entwickelter Inhibitor von 5’tiRNAGly‑GCC das Tumorwachstum, und die Kombination dieses Inhibitors mit Doxorubicin wirkte besser als jede Behandlung allein. Das Team fand heraus, dass 5’tiRNAGly‑GCC an ein Protein namens hnRNPH1 bindet und dessen Menge in den Zellen reduziert. Da hnRNPH1 normalerweise hilft, die Spiegel des immunrelevanten Proteins PD‑L1 in Schach zu halten, führt der Verlust von hnRNPH1 zu einem Anstieg von PD‑L1 — eine Veränderung, die Tumoren hilft, der Immunabwehr zu entkommen und mit einer Ansammlung regulatorischer T‑Zellen um Tumoren herum verknüpft ist.
Was das für zukünftige Therapien bedeutet
Vereinfacht gesagt offenbart die Studie eine Kettenreaktion: Wenn DNMT2 niedrig ist, verlieren bestimmte tRNAs ihre Schutzmarke, werden in kleine Fragmente zerschnitten, und eines dieser Fragmente (5’tiRNAGly‑GCC) schaltet ein Protein aus, das PD‑L1 zurückhält. Das Ergebnis ist ein aggressiverer, medikamentenresistenter und immunflüchtiger Tumor. Anstatt zu versuchen, DNMT2 direkt zu erhöhen — was in anderen Geweben riskant sein könnte — schlagen die Autorinnen und Autoren vor, das schädliche RNA‑Fragment selbst ins Visier zu nehmen. Ihre Mausversuche mit einem 5’tiRNAGly‑GCC‑Inhibitor, besonders in Kombination mit Doxorubicin, liefern erste Belege dafür, dass die Unterbrechung dieser mikroskopischen RNA‑Verschaltung helfen könnte, eine der tödlichsten Formen von Schilddrüsenkrebs zu zähmen.
Zitation: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Schlüsselwörter: anaplastischer Schilddrüsenkrebs, DNMT2, tRNA-Fragmente, Chemoresistenz, PD-L1