Clear Sky Science · de
Enthüllung von ZNF124 als neuem Faktor bei Neurodegeneration: Steuerung der Photorezeptor-Homöostase durch transkriptionelle Regulation von MSX2
Warum diese Entdeckung für das Sehen Bedeutung hat
Retinitis pigmentosa ist eine der Hauptursachen für vererbte Erblindung, doch bei fast 40 Prozent der Patientinnen und Patienten kann die verantwortliche Genvariante noch nicht identifiziert werden. Diese Studie beschreibt einen neuen genetischen Akteur, ZNF124, der dazu beiträgt, lichtempfindliche Zellen im Auge am Leben zu erhalten. Indem die Forschenden zeigen, wie eine Mutation in diesem Gen eine Kaskade molekularer „Schalter“ in der Netzhaut stört, eröffnen sie neue Wege für Diagnosen und womöglich zielgerichtete Therapien für Menschen mit fortschreitendem Sehverlust.
Eine verborgene Ursache vererbten Sehverlusts
Die Forschenden untersuchten eine große Familie, in der mehrere Kinder typische Zeichen einer Retinitis pigmentosa entwickelten: frühzeitige Nachtblindheit, zunehmender Einengung des Gesichtsfelds und schrittweiser Verlust des zentralen Sehens. Detaillierte Augenuntersuchungen zeigten eine Ausdünnung der Netzhaut und schwache elektrische Reaktionen auf Licht, beides Kennzeichen einer Schädigung von Stäbchen- und Zapfenphotorezeptoren. Dennoch wiesen keines der mehr als 80 bekannten Retinitis-pigmentosa-Gene bei diesen Patientinnen und Patienten auffällige Defekte auf, was darauf hindeutete, dass ein bisher unentdecktes Gen für ihre Erkrankung verantwortlich sein könnte.
Ein fehlerhafter genetischer Schalter wird gefunden
Mithilfe von Whole-Exome-Sequenzierung, die die protein-codierenden Bereiche der DNA liest, identifizierte das Team eine seltene, bislang nicht beschriebene Mutation im ZNF124-Gen. Diese Mutation verändert die Art und Weise, wie die RNA des Gens zusammengesetzt wird, sodass an einer kritischen Stelle ein paar Basen fehlen. Infolgedessen wird das ZNF124-Protein verkürzt und verliert seine Zinkfingerregion, eine Struktur, die normalerweise zur Erkennung und Bindung spezifischer DNA-Sequenzen dient. Da Zinkfingerproteine häufig als Hauptschalter fungieren, die viele andere Gene ein- oder ausschalten, könnte ein geschädigtes ZNF124 weitreichende Folgen in Netzhautzellen haben.
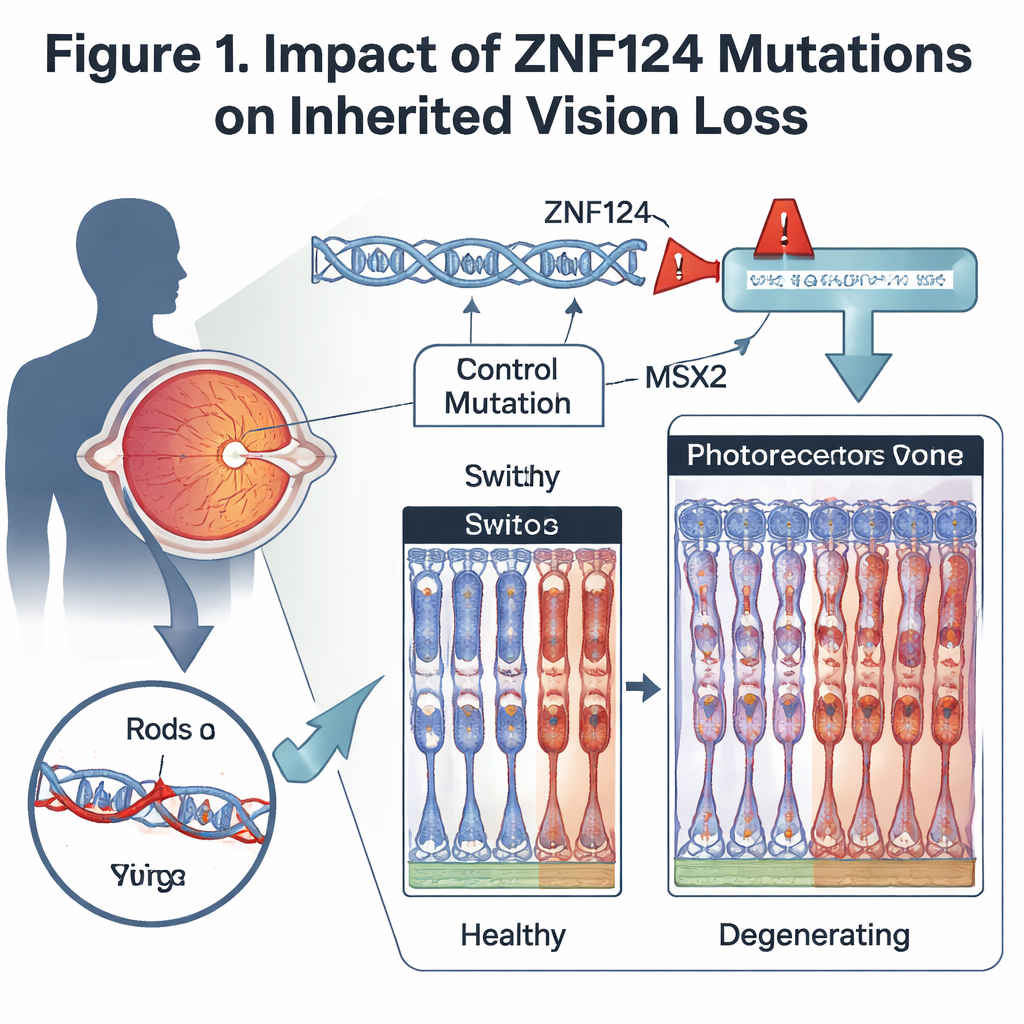
Prüfung des Gens in Tiermodellen
Um zu untersuchen, wie der Verlust dieses Schalters das Auge beeinflusst, erzeugten die Wissenschaftler Mäuse, denen Gm20541 fehlte — das nächstverwandte Mausäquivalent zu ZNF124 — und zwar spezifisch in der Netzhaut. Diese Tiere entwickelten altersabhängige Sehstörungen: ihre elektrischen Reaktionen auf schwaches und helles Licht schwächten sich ab, und die mikroskopische Untersuchung zeigte eine progressive Ausdünnung der Netzhautschicht, die die Photorezeptoren enthält. Sowohl Stäbchen, die das Nachtsehen unterstützen, als auch Zapfen, die Farbe und Tagsehen ermöglichen, zeigten verkürzte äußere Segmente und Verlust wichtiger Sehproteine. Auch andere Netzhautzellen, wie bestimmte Bipolarzellen, waren vermindert, und Stützzellen wurden aktiviert — eine übliche Reaktion auf chronische Netzhautschädigung.
Aufdeckung des ZNF124–MSX2-Kontrollwegs
Die nächste Frage war, welche Gene ZNF124 normalerweise reguliert. Durch biochemische Methoden, die zeigen, wo Proteine auf der DNA sitzen, kombiniert mit globalen RNA-Analysen aus Mausnetzhäuten, fand das Team, dass ZNF124 an ein anderes Gen namens MSX2 bindet und dessen Aktivität fördert. In gesunden Zellen heftet sich ZNF124 an eine kurze, spezifische Sequenz in der „An-Schalter“-Region von MSX2 und steigert dessen Aktivität. In Mäusen ohne Gm20541 sanken die MSX2-Spiegel um mehr als die Hälfte. Als die Forschenden MSX2 gezielt in Stäbchenzellen entfernten, entwickelten auch diese Tiere eine Ausdünnung der Photorezeptorschicht und verkürzte äußere Segmente — ein Spiegelbild der Defekte, die bei den ZNF124-ähnlichen Knockout-Mäusen beobachtet wurden. Damit wurde MSX2 direkt unterhalb von ZNF124 in einem für das Überleben der Photorezeptoren essenziellen Signalweg eingeordnet.
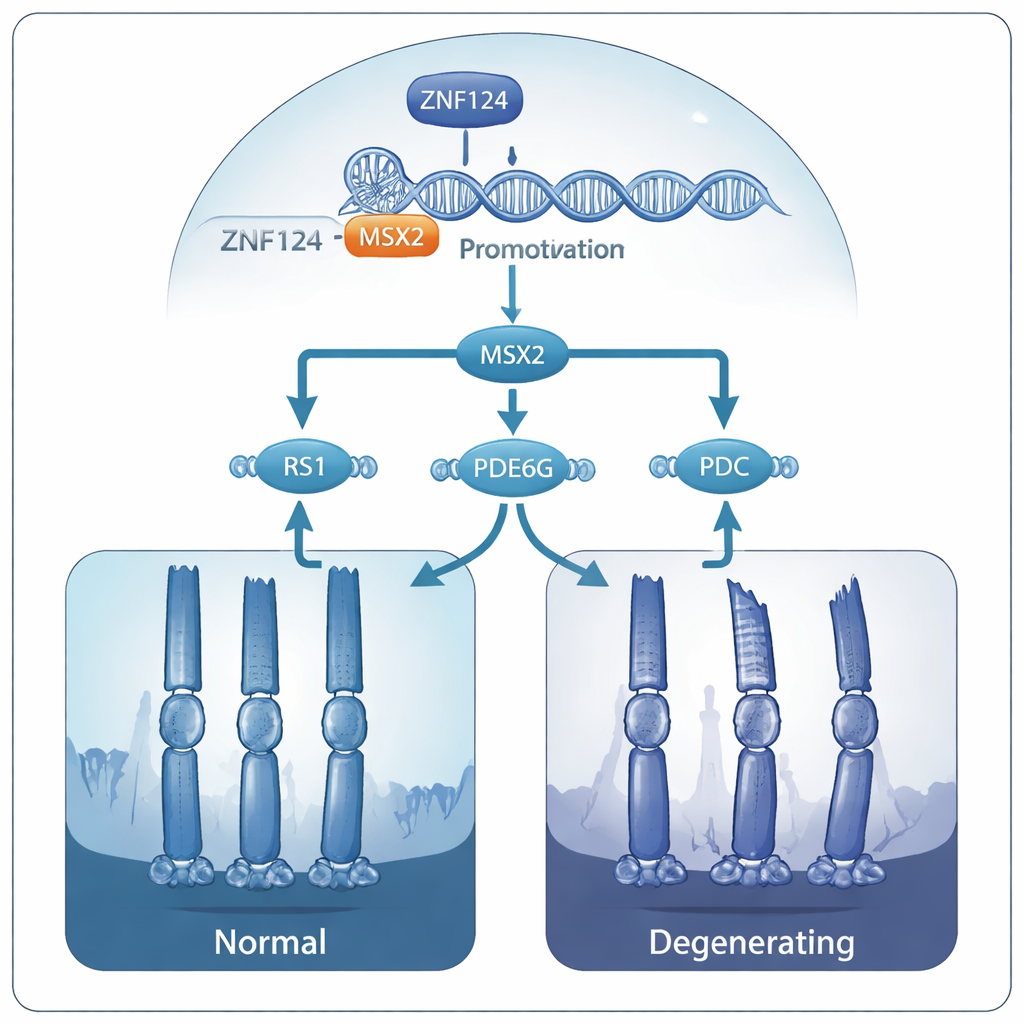
Von genetischen Schaltern zu fragilen Photorezeptoren
Weitere Analysen zeigten, dass MSX2 wiederum mehrere andere Gene unterstützt, die bereits mit erblichen Netzhauterkrankungen in Verbindung gebracht wurden: RS1, PDE6G und PDC. Diese Gene tragen zur Struktur der Netzhaut und zur Chemie der visuellen Signalübertragung bei. Bei reduziertem MSX2 wurden alle drei Gene weniger aktiv und ihre Proteinprodukte gingen zurück. Die Autorinnen und Autoren schlagen vor, dass bei Menschen mit schädigenden ZNF124-Mutationen diese gesamte Kaskade geschwächt ist: ZNF124 kann MSX2 nicht mehr vollständig aktivieren, MSX2 kann RS1, PDE6G und PDC nicht mehr aufrechterhalten, und im Laufe der Zeit verlieren die Photorezeptoren ihre strukturelle Integrität und sterben ab, was zu fortschreitendem Sehverlust führt.
Was das für Patientinnen, Patienten und Therapien bedeutet
Für Nicht-Spezialisten lautet die zentrale Botschaft, dass die Netzhaut von einer fein abgestimmten Hierarchie genetischer Schalter abhängt. Diese Arbeit identifiziert ZNF124 als neuen obersten Schalter, dessen Ausfall vererbte Erblindung über einen spezifischen nachgeschalteten Partner, MSX2, und dessen Zielgene verursachen kann. Klinisch kann ZNF124 nun in genetische Testpanels aufgenommen werden, wodurch mehr Familien präzise Diagnosen erhalten können. Langfristig könnten Therapien, die die Aktivität von ZNF124, MSX2 oder der betroffenen downstream-Gene wiederherstellen, dazu beitragen, lichtempfindliche Zellen zu stabilisieren oder zu retten und so neue Hoffnung für Menschen mit bislang ungeklärten Formen der Retinitis pigmentosa bieten.
Zitation: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Schlüsselwörter: retinitis pigmentosa, Photorezeptoren, ZNF124, MSX2, erbliche Netzhauterkrankung