Clear Sky Science · de
TIGAR erhält die Regeneration des intestinalen Epithels durch Stabilisierung von HMGCL und Förderung der β‑Catenin-β‑Hydroxybutyrylier ung bei Brandverletzungs‑induziertem Sepsis
Warum Darmreparatur nach schweren Verbrennungen wichtig ist
Schwere Verbrennungen schädigen nicht nur die Haut; sie können auch im Inneren des Körpers großen Schaden anrichten, besonders im Darm. Wenn die innere Auskleidung des Darms zusammenbricht, können Bakterien und Toxine ins Blut gelangen und gefährliche Infektionen sowie Organversagen auslösen. Diese Studie untersucht, wie ein natürlicher metabolischer „Schalter“ in Darmzellen der Darmreparatur nach burn‑induziertem Sepsis hilft und wie die Störung dieses Schalters eine beherrschbare Verletzung in eine lebensbedrohliche Krise verwandeln kann.
Eine verborgene Reparaturtruppe in der Darmschleimhaut
Die Innenseite des Dünndarms ist mit winzigen fingerartigen Ausstülpungen, den Zotten, bedeckt, die sich ständig erneuern. Diese Erneuerung hängt von Darmstammzellen ab, die in Taschen an der Basis der Zotten liegen. Nach schweren Verbrennungen und Sepsis stellten die Forschenden fest, dass die Struktur des Darms bei Mäusen stark beschädigt war: Zotten schrumpften, regenerative Nischen gingen verloren und Marker für Zellwachstum fielen ab. Gleichzeitig sanken die Werte eines Proteins namens TIGAR, das sonst in diesen regenerativen Bereichen angereichert ist, deutlich. Mäuse mit reduziertem TIGAR in ihren Darmzellen zeigten stärkere Schäden und schlechtere Stammzellaktivität, was darauf hindeutet, dass TIGAR als interner Schutzfaktor für die Darmregeneration bei schweren Erkrankungen wirkt. 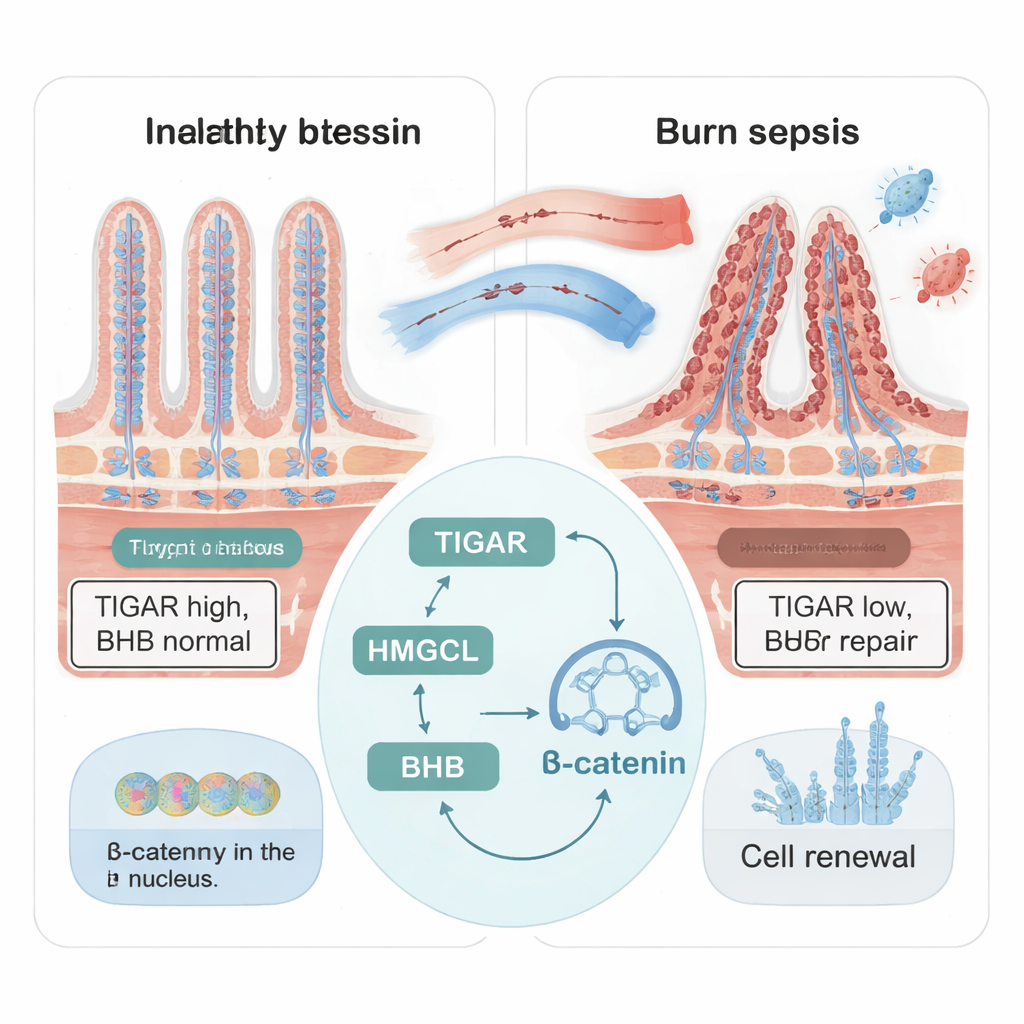
Reparatur mit einem speziellen fettabgeleiteten Molekül antreiben
Darmzellen können nicht nur Zucker und Aminosäuren als Energiequelle nutzen, sondern auch Ketonkörper—fettabgeleitete Moleküle, die hauptsächlich in der Leber und in geringerem Maße im Darm gebildet werden. Das Team konzentrierte sich auf Beta‑Hydroxybutyrat (BHB), den häufigsten Ketonkörper, der dafür bekannt ist, Stammzellen und Gewebeerneuerung zu unterstützen. Bei burn‑sepsis‑Mäusen stiegen die intestinalen BHB‑Werte zunächst an und fielen dann bis zum siebten Tag auf etwa ein Drittel des Normalwerts, passend zur Phase der schwersten Schädigung. Wenn TIGAR in Darmzellen reduziert war, sanken die BHB‑Spiegel ebenfalls. Die Zugabe von zusätzlichem BHB in Zell‑ und Mini‑Darm‑(Organoid‑)Modellen rettete das Zellwachstum, stellte Stammzellmarker wieder her und hielt den schädigenden Effekten inflammatorischen Stresses entgegen, was zeigt, dass BHB ein zentraler Treibstoff und Signalstoff für die Darmreparatur ist.
Wie TIGAR den Ketonmotor am Laufen hält
Bei tieferer Untersuchung entdeckten die Forschenden, wie TIGAR die BHB‑Produktion aufrechterhält. Innerhalb der Darmzellen ist das Enzym HMGCL ein entscheidender Schritt bei der Herstellung von Ketonkörpern. TIGAR bindet direkt an HMGCL innerhalb der Mitochondrien, den Energiemanufakturen der Zelle. Diese Bindung schützt HMGCL vor einem anderen Protein, Park2, das HMGCL normalerweise mit Ubiquitin‑Ketten markiert und so zum Abbau durch das zelluläre „Schredder“-System führt. Indem TIGAR diese Markierung blockiert, verhindert es den Abbau von HMGCL und hält die Ketonsynthese aktiv. Wenn TIGAR entfernt wurde oder Zellen mit bakteriellen Toxinen gestresst wurden, wurde HMGCL instabil, die BHB‑Produktion sank und die Zellproliferation verlangsamte sich; die Wiederherstellung von HMGCL oder die Zugabe von BHB kehrte viele dieser Defekte um.
Ein molekularer Stoß, der Wachstumssignale in den Zellkern sendet
BHB liefert nicht nur Energie; es modifiziert auch Proteine. Die Studie zeigt, dass BHB eine kleine chemische Markierung, die β‑Hydroxybutyrylier ung, an einer spezifischen Stelle (Lysin 335) von β‑Catenin anbringt, einem zentralen Schalter, der Gene für Zellwachstum und Stammzellrenewal steuert. Bei ausreichendem BHB wandert β‑Catenin mit dieser Markierung in den Zellkern und arbeitet dort mit einem weiteren Faktor, TCF4, zusammen, um wachstumsfördernde Gene einzuschalten. Wenn BHB niedrig ist oder diese spezifische Stelle auf β‑Catenin mutiert ist, fällt es β‑Catenin schwer, in den Kern zu gelangen, und das Wachstumsprogramm stockt. TIGAR kontrolliert also indirekt, indem es HMGCL und BHB erhält, ob β‑Catenin den Kern erreichen kann und die Erneuerung der Darmschleimhaut fortsetzt. 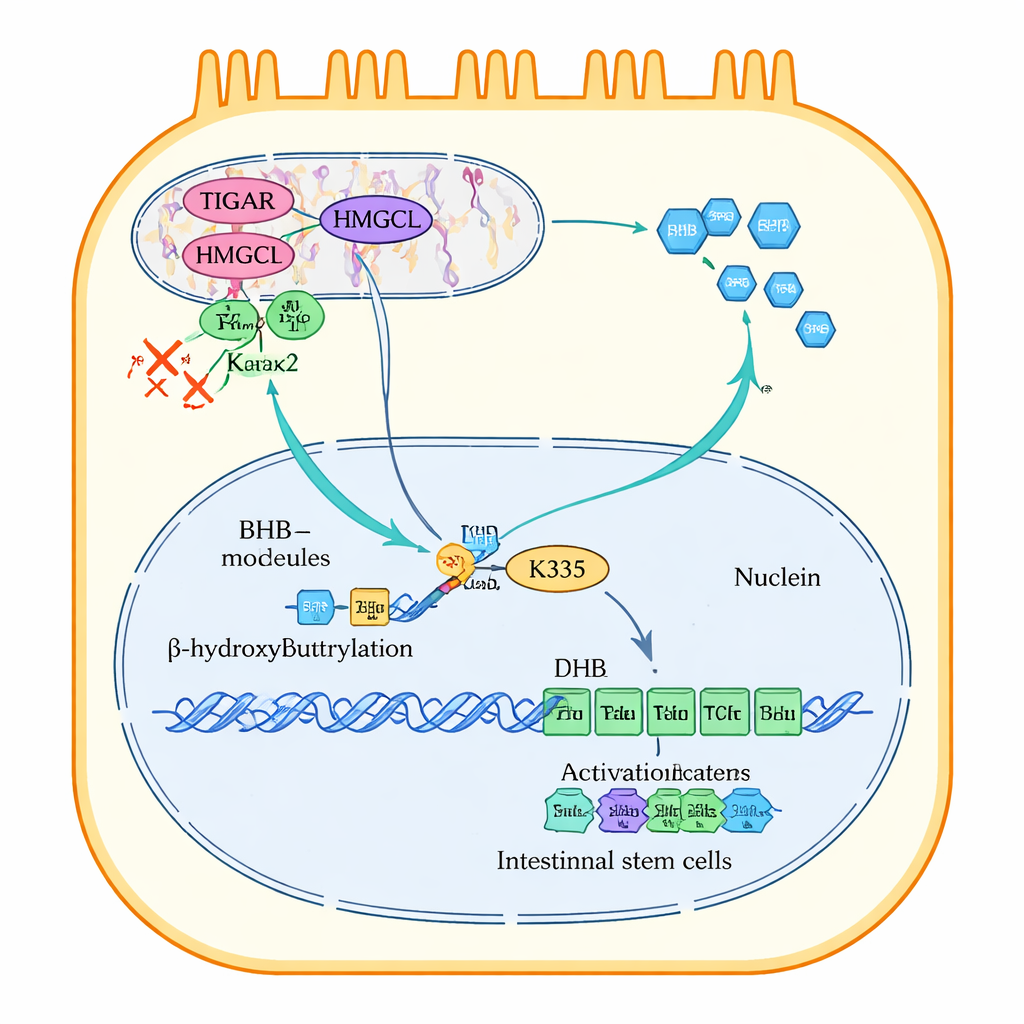
Was das für Brandpatienten bedeutet
Vereinfacht gesagt zeigt diese Arbeit eine Kettenreaktion: TIGAR schützt ein ketonproduzierendes Enzym (HMGCL), das die BHB‑Spiegel hoch hält; BHB justiert dann einen Wachstumsschalter (β‑Catenin), der Darmstammzellen zur Teilung und zum Wiederaufbau der Darmbarriere anregt. Fällt der TIGAR‑Spiegel nach schweren Verbrennungen und Sepsis, bricht diese Schutzkette zusammen, die Darmreparatur scheitert und Barrierenversagen verschlimmert Infektionen. Die gezielte Beeinflussung dieser TIGAR–HMGCL–BHB–β‑Catenin‑Achse—etwa durch Stärkung der TIGAR‑Funktion, Stabilisierung von HMGCL oder sichere Supplementierung von BHB—könnte neue Wege eröffnen, die Darmintegrität zu bewahren und das Überleben von Patienten mit schweren Verbrennungen und anderen kritischen Erkrankungen, die die intestinale Barriere bedrohen, zu verbessern.
Zitation: Zhang, P., Wu, D., Wei, Y. et al. TIGAR maintains intestinal epithelial regeneration by stabilizing HMGCL and promoting β-catenin β-hydroxybutyrylation in burn-induced sepsis. Cell Death Dis 17, 233 (2026). https://doi.org/10.1038/s41419-026-08486-7
Schlüsselwörter: Reparatur der Darmbarriere, Ketonkörper, TIGAR, Brandsepsis, Darmstammzellen