Clear Sky Science · de
HIF2α-induzierte Lysyloxidase schützt eine erfolgreiche Schwangerschaft durch Umgestaltung von Kollagenen an der fetomaternalen Grenzfläche
Warum sich die Gebärmutter auf neuen Nachwuchs vorbereiten muss
Bevor eine Schwangerschaft Fuß fassen kann, muss ein früher Embryo etwas Bemerkenswertes leisten: sich in die Gebärmutterschleimhaut einnisten und ein Lebenserhaltungssystem — die Plazenta — aufbauen. Dieser Artikel untersucht, wie das Gewebe der Mutter sich still verändert, um den Embryo aufzunehmen, und konzentriert sich dabei darauf, wie niedrige Sauerstoffwerte und ein wenig bekanntes Enzym die Gebärmutterschleimhaut vorbereiten. Das Verständnis dieses fein abgestimmten Zusammenspiels könnte erklären, warum einige Schwangerschaften sehr früh scheitern, und neue Ansätze zur Vorbeugung von Unfruchtbarkeit und Komplikationen in der Schwangerschaft nahelegen.
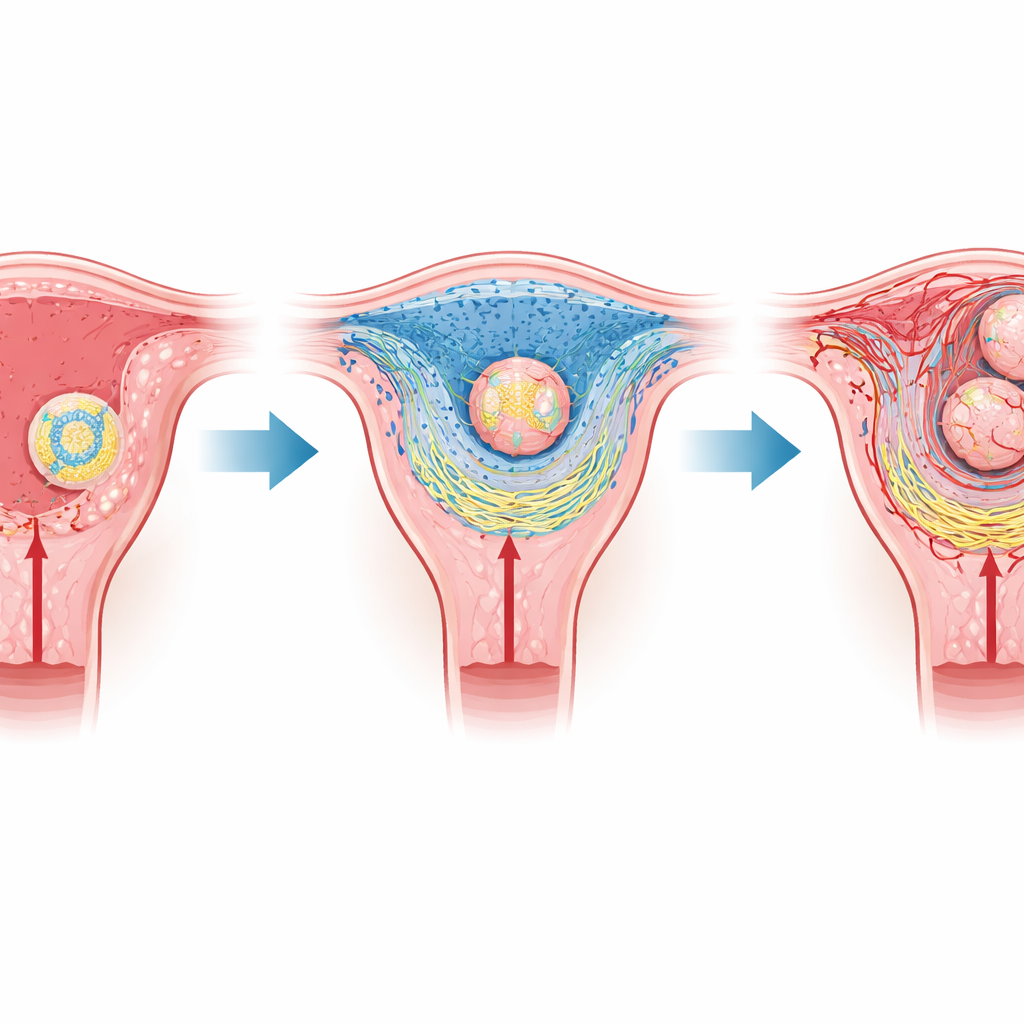
Ein empfindsames Treffen zwischen Mutter und Embryo
Bei Säugetieren wie Mäusen und Menschen hängt die früheste Phase der Schwangerschaft von der Implantation ab, wenn sich der Embryo an die Gebärmutterschleimhaut anheftet und diese dann durchdringt. Der Embryo ist von einer Hülle spezialisierter Zellen umgeben, die später die Plazenta bilden werden, während das Gewebe der Mutter sich in eine polsterartige Schicht, das Deziduum, verwandelt. Am nächsten zum Embryo liegt eine dünne Region, die als primäre deziduale Zone bezeichnet wird; sie ist gefäßfrei und enthält daher wenig Sauerstoff. Frühere Arbeiten zeigten, dass diese natürlich sauerstoffarme Nische die Implantation fördert, doch war bislang unklar, wie ein so einfacher physikalischer Zustand ganze Gewebe umorganisieren kann.
Niedriger Sauerstoff als versteckter Schalter
Die Autoren nutzten eine leistungsfähige Methode namens räumliche Transkriptomik, die Genaktivität direkt auf Gewebeschnitte abbildet, um die Uteri von Mäusen in den Tagen zu untersuchen, in denen sich Embryonen anheften und eindringen. Sie konzentrierten sich auf ein Protein namens HIF2α, das unter niedrigen Sauerstoffbedingungen aktiviert wird und als genetischer Schalter wirkt. Bei normalen Mäusen zeigten Zellen in der primären dezidualen Zone eine starke Aktivität von Genen, die mit Hypoxie und mit dem Aufbau der umgebenden Gerüstsubstanz, einschließlich der Kollagene der extrazellulären Matrix, verknüpft sind. Wurde HIF2α jedoch nur in der Gebärmutter entfernt, erschien die Gesamtanordnung der Zelltypen auf den ersten Blick überraschend normal. Auf höherer Auflösung war das Kollagennetzwerk jedoch desorganisiert, die epitheliale Oberfläche öffnete sich nicht richtig, und embryonale Zellen hatten Schwierigkeiten, in das mütterliche Gewebe einzudringen.
Ein Enzym, das das Gerüst vernetzt
Bei tiefergehenden Untersuchungen identifizierte das Team einen Schlüsselakteur stromabwärts von HIF2α: Lysyloxidase, kurz Lox, ein Enzym, das Kollagenfasern chemisch vernetzt und so Gewebe versteift und stabilisiert. In normalen Schwangerschaften stiegen die Lox-Spiegel rund um die Embryonen genau dann scharf an, als diese zu invasivem Verhalten übergingen. In Uteri ohne HIF2α fiel die Lox-Expression ab, und Kollagenfasern erschienen fragmentiert statt als dichtes Geflecht. Um die Bedeutung von Lox direkt zu testen, erzeugten die Forscher Mäuse, bei denen Lox nur in der Gebärmutter entfernt wurde. Diese Weibchen wurden seltener trächtig, trugen weniger Embryonen und zeigten häufig Anzeichen von Embryoverlust und Blutungen später in der Schwangerschaft, obwohl die frühesten Schritte der Anheftung und Gewebsvermehrung zunächst normal wirkten.
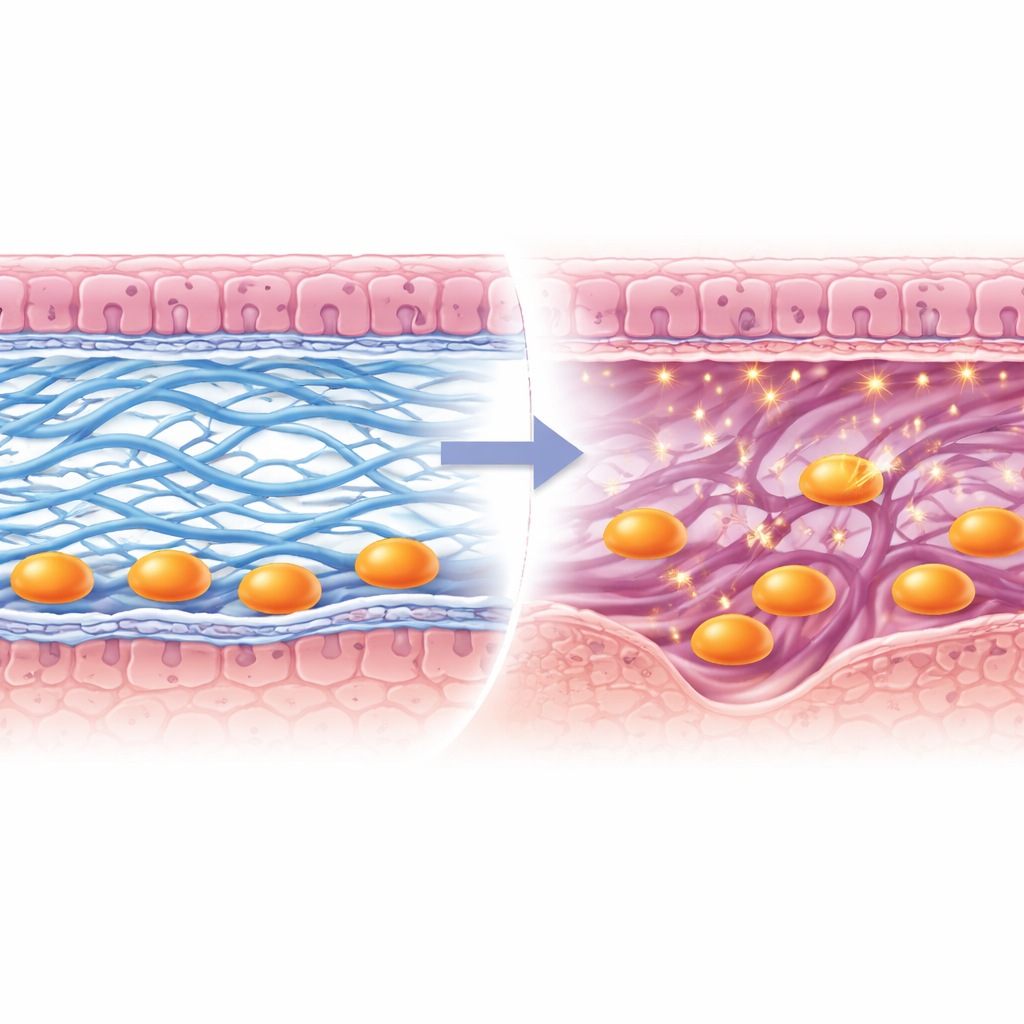
Ein Weg für die Plazenta wird geöffnet
Feinere Bildgebungen zeigten, was schieflief, wenn Lox fehlte. Eine dünne, proteinreiche Schicht namens Basalmembran, die normal abgebaut wird, um embryonalen Zellen Passage zu gewähren, blieb weitgehend intakt. Kollagen Typ I-Fasern im darunterliegenden Stroma bildeten keine robusten, kontinuierlichen Bündel, während Kollagen Typ IV in der Basalmembran in der Nähe eindringender Zellen nicht richtig entfernt wurde. Als Folge blieben Trophoblastzellen — die embryonalen Vorreiter, die die Plazenta aufbauen — an der Oberfläche gefangen, statt in die mütterliche Schicht zu tunneln. Das Team fand außerdem, dass ein kollagenabbauendes Enzym, Mmp9, in diesen Trophoblasten nicht hochreguliert wurde, was ihr Fortkommen weiter behinderte. Mit der Zeit bildeten sich Plazentastrukturen schlecht, Embryonen wuchsen ungewöhnlich, und der Schwangerschaftserfolg nahm ab.
Was das für die Gesundheit von Schwangerschaften bedeutet
Zusammengefasst zeichnen die Ergebnisse eine Ereigniskette nach, in der niedriger Sauerstoff in der frühen Implantationszone HIF2α aktiviert, welches wiederum Lox hochfährt. Lox formt und vernetzt dann Kollagenfasern und trägt zum Abbau der Basalmembran bei, während es zugleich Enzyme wie Mmp9 ermöglicht, einen Weg freizuräumen. Diese Umgestaltung liefert sowohl ein strukturelles Gerüst als auch eine geöffnete Pforte für Trophoblastzellen, damit sie eindringen und die Plazenta konstruieren können. Für Laien lautet die Botschaft, dass eine erfolgreiche Schwangerschaft nicht nur von gesunden Embryonen und Hormonen abhängt, sondern auch von der stillen Umgestaltung der Gewebearchitektur der Mutter. Störungen in dieser Hypoxie–HIF2α–Lox-Achse könnten einigen Fällen unerklärter Unfruchtbarkeit, Fehlgeburten und Erkrankungen mit schlechter placentärer Invasion zugrunde liegen und damit neue diagnostische Marker sowie therapeutische Ziele zur Unterstützung früher Schwangerschaften nahelegen.
Zitation: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Schlüsselwörter: Embryonale Implantation, uterine extrazelluläre Matrix, Lysyloxidase, Trophoblastinvasion, plazentare Entwicklung